水体离子强度、pH值和腐殖酸浓度对石墨相氮化碳沉降的影响
董姝楠,夏继红,王为木,刘 慧,盛丽婷
(河海大学农业科学与工程学院,南京 210098)
0 引 言
石墨相氮化碳(Graphitic Carbon Nitride,g-C3N4)是一种新型光催化材料,能够直接利用可见光催化分解有机污染物,具有制备工艺简单、生产成本低、结构稳定性强等特点[1-3]。g-C3N4能够广泛应用于催化降解农业污染水体及土壤中的农药、多环芳烃、抗生素等有机污染物,表现出较高的催化效率[4-6]。然而,He等[7]研究发现环境中的g-C3N4具有一定生物毒性,能够降低微生物的细胞活性,导致微生物死亡。在生产及使用过程中,g-C3N4会不可避免地进入农业水土环境,对环境安全及生态健康造成潜在威胁。近年来,g-C3N4的环境行为逐渐引起研究人员的重视[7-9]。水体是g-C3N4的主要赋存环境,水体中的g-C3N4主要以悬浮颗粒的形式存在[9]。研究表明,沉降与分散稳定性是影响水环境中悬浮颗粒生物毒性的重要因素[10]。此外,水环境中g-C3N4的催化效率也受其沉降与分散稳定性的影响[1]。因此,研究不同水环境条件对g-C3N4的沉降与分散稳定性的影响,对于准确评估其在农业环境的生物毒性及环境风险,分析其催化效率等具有重要意义。
目前,水体中g-C3N4的沉降与分散研究相对较少。Ong等[1]研究表明,水体中g-C3N4的分散稳定性通常较差。经酸化处理后,g-C3N4颗粒表面亲水官能团含量增加,其在水体中的稳定性会随之上升。水体中有机溶剂(如丙酮、乙醇、异丙醇等)的存在能够一定程度上增强g-C3N4的分散稳定性,然而随着有机溶剂的蒸发,g-C3N4的分散稳定性会逐渐随之下降[11]。另一方面,Dong等[9]发现,离子条件、pH值等水环境因素能够明显影响水体中g-C3N4悬浮颗粒的团聚程度。然而,典型水环境因素对g-C3N4沉降与分散行为的影响机制尚未明晰,亟需推进相关研究。
综上,为解决农业水环境中g-C3N4的风险评估、污染预测等问题,本研究以g-C3N4颗粒为主要研究对象,通过室内沉降试验、沉降模型计算、DLVO(Derjaguine Landaue Verweye Overbeek)理论计算相结合的研究方法,考察离子强度(Ionic Strength,IS)、pH值以及腐殖酸(Humic Acid,HA)几种典型水环境因素对g-C3N4沉降及分散稳定的影响。本研究结果旨在补充农业环境中g-C3N4的行为理论,为预测和评价其农业生态安全提供科学依据。
1 材料与方法
1.1 石墨相氮化碳(g-C3N4)的制备
尿素(分析纯,国药集团化学试剂有限公司)作为反应物,通过热聚合法制备试验所需的g-C3N4[12]:首先,称取20 g尿素,用锡纸包裹后放置于坩埚中,坩埚加盖闭合;将坩埚放置于马弗炉(SX2-2.5-10T,上海锦玟仪器设备有限公司)中,以5 ℃/min的加热速率加热至550 ℃,维持该恒定温度2 h后,以10 ℃/min的冷却速率将马弗炉系统冷却至室温,获得所需的g-C3N4;使用去离子水(Deionized Water,DIW)将制备的g-C3N4润洗5遍以去除可溶性杂质,然后在40 ℃条件下烘干,放置于棕色试剂瓶中密封储存。
1.2 石墨相氮化碳(g-C3N4)沉降试验
对于每一组沉降试验,通过DIW配制不同IS、pH值和HA浓度条件的背景溶液。称取1 mg的g-C3N4粉末与100 mL对应背景溶液混合,通过超声仪(XY10-200E,上海析宇仪器有限公司)超声混合物60 min,使g-C3N4均匀分散,形成悬液。使用NaCl(分析纯,国药集团化学试剂有限公司)作为背景电解质,所用浓度分别为0、0.5、1.0、10.0、20.0、50.0 mmol/L。本研究使用的HA购自美国Sigma-Aldrich试剂公司,所用浓度分别为0、1、5、10 mg/L。使用NaOH溶液(1 mol/L)和HCl溶液(1 mol/L)将g-C3N4悬液的pH值分别调为2、4、6、8、10,获得待测g-C3N4悬液。上述NaCl浓度、pH值和HA浓度梯度的设置方式有助于呈现试验结果趋势,在水体中悬浮颗粒的环境行为研究领域被广泛应用[9,13]。其中,研究IS对g-C3N4沉降与分散稳定性的影响时,设置pH值为6(接近二氧化碳饱和时水环境的pH值),HA浓度为0 mg/L(避免HA干扰);研究pH值对g-C3N4沉降与分散稳定性的影响时,设置IS为1.0 mmol/L(接近天然淡水IS),HA浓度为0 mg/L;研究HA对g-C3N4沉降与分散稳定性的影响时,设置IS为1.0 mmol/L,pH值为6。本研究共设13组试验,每组设置2组平行试验,试验条件如表1所示。
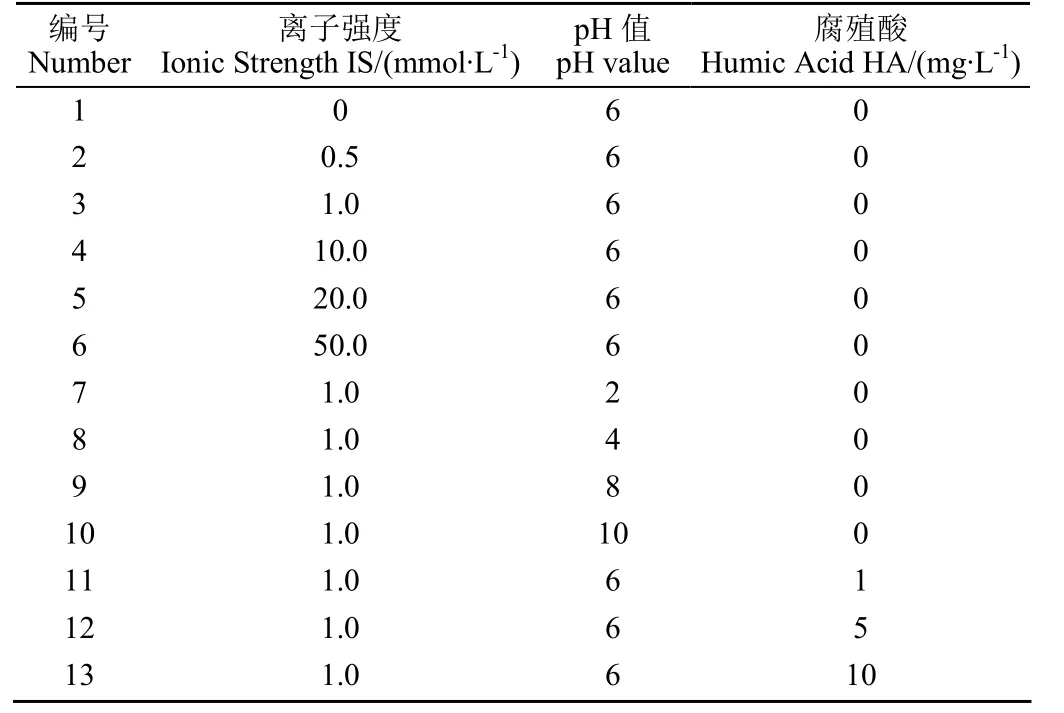
?
使用紫外-可见分光光度计(UV-2000,尤尼柯仪器有限公司)在345 nm波长处动态监测g-C3N4悬液浓度变化,监测时间间隔为5 min,监测时长为360 min[9]。将试验数据转化为g-C3N4悬液的标准化浓度(C/C0),将其作为时间(t,min)的函数绘制g-C3N4沉降动力学曲线,从而描述不同水环境因素影响下g-C3N4的沉降行为与分散稳定性。使用纳米粒度和Zeta电位分析仪(Nanotrac Wave Ⅱ,美国Microtrac)对不同条件下g-C3N4的水动力学半径(r,nm)和表面Zeta电位(ξ,mV)进行测定,用于辅助分析水环境因素对g-C3N4沉降及分散稳定的影响机制。
1.3 一阶动力学沉降模型
本研究采用一阶动力学沉降模型对不同水环境条件下g-C3N4的沉降动力学曲线进行模拟[13],如式(1)所示:
式中Ct为时间t时g-C3N4悬液的浓度,mg/L;C0为g-C3N4悬液的初始浓度,mg/L;Cf为试验结束时g-C3N4悬液的残余浓度,mg/L;sv为沉降速率,cm/min;H为g-C3N4的沉降高度,cm;t为时间,min。
1.4 DLVO理论
本研究采用球-球碰撞模式,通过DLVO理论计算不同条件下g-C3N4颗粒之间的势能,绘制势能随颗粒之间距离变化的曲线,即DLVO势能曲线,用于深入分析水环境因素对g-C3N4沉降及分散稳定的影响机制。DLVO势能曲线的极小值为第二极小势能值。为便于分析,本研究中将DLVO计算结果标准化为玻尔兹曼常数k与绝对温度T(273.15 K)乘积的倍数。DLVO总势能(Wtotal)主要包括静电斥力(Wedl)和范德华引力(Wvdw)两部分[13]。特别的,当背景溶液存在HA时,势能计算体系需要考虑空间排斥力(Wsteric),主要包括渗透排斥(Wosm)和弹性空间排斥(Welas)[14]。其计算如式(2)~式(7)所示:
式中ε0为真空介电常数,F/m;εr为水的介电常数,F/m;r为g-C3N4的水动力学半径,nm;k为玻尔兹曼常数,J/K;T为绝对温度,K;v为电解质价态;e为电子电荷,C;δ为德拜-休克尔参数;ξ为Zeta电位,mV;h为颗粒之间的距离,nm;A121为哈梅克常数,J;λ为特征波长,nm;χ为弗洛里-哈金斯溶解参数;V为溶质分子的体积,nm3;φ为HA覆盖分数;d为HA吸附层厚度,nm;Mw为HA分子量;ρ为HA密度,mg/cm3。
2 结果与分析
2.1 离子强度对g-C3N4沉降与分散稳定性的影响
pH值为6、HA浓度为0 mg/L时,不同IS条件下g-C3N4的ξ、水动力学半径见表2,沉降动力学曲线如图1a所示。试验结果表明,即使背景溶液中不含离子,360 min后g-C3N4仍然发生明显沉降,其悬液的C/C0由1.00下降至0.86,表明水体中g-C3N4的分散稳定性较差。一阶动力学模型结果与试验结果拟合度较高(决定系数均大于0.96),计算得到该条件下g-C3N4的沉降速率(sv)值为0.014 4 cm/min。测量结果显示,g-C3N4具有较大的水动力学半径,为770 nm(表2)。表面电位测定结果显示,该试验条件下g-C3N4的表面ξ值为-37.1 mV,呈电负性。Zhu等[15]研究表明,g-C3N4表面的伯胺、仲胺官能团能与水中的氢氧根离子反应,使g-C3N4表面带负电。
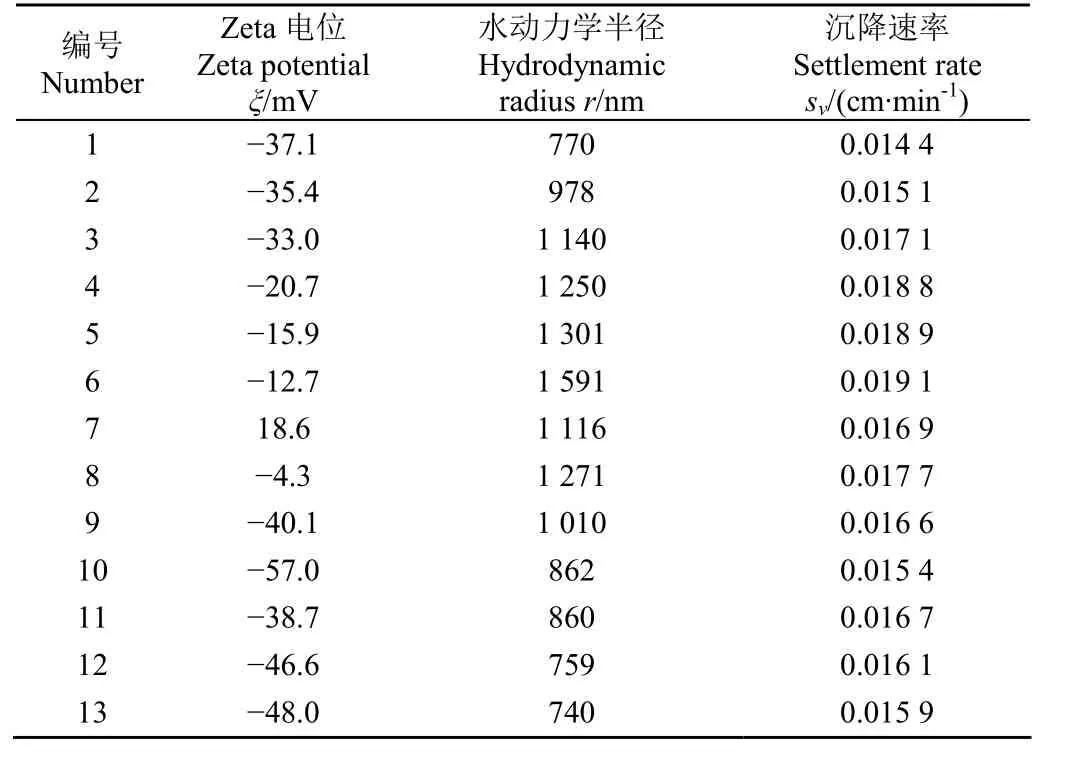
表2 不同试验条件下g-C3N4的Zeta电位、水动力学半径及模型结果汇总Table 2 Summary of Zeta potential, hydrodynamic radius, and model results of g-C3N4 under different experiment conditions
水环境IS是影响g-C3N4沉降及分散稳定的敏感因素,当水环境IS仅为1.0 mmol/L时,g-C3N4的沉降程度仍明显增强。g-C3N4悬液浓度随水环境IS的升高而明显降低(图1a)。随着水环境IS的升高,g-C3N4的沉降明显增强,其分散稳定性随之降低。随着IS由0上升至50.0 mmol/L,360 min后g-C3N4悬液的终点C/C0由0.86变为0.58。一阶动力学沉降模型可以很好地模拟试验结果(图1a),相关系数R2均大于0.96(表2)。模型结果显示,随着水环境IS的升高,g-C3N4的sv值逐渐增大,由最低0.0144上升至最高0.019 1 cm/min。模型结果表明,g-C3N4的沉降速率随水溶液IS的升高而不断增大,沉降程度逐渐增强,与试验结果相符。
水动力学半径测量结果显示,随着水环境IS的升高,g-C3N4的水动力学半径不断增大,由770上升至1 591 nm(表2)。表面电位测定结果显示,g-C3N4的表面电负性随水环境IS的升高而减弱,ξ绝对值逐渐减小。随着水环境IS由上升至50.0 mmol/L,g-C3N4的ξ值由-37.1升高至-12.7 mV。水环境IS升高,g-C3N4颗粒表面的双电层受到压缩而变薄,其表面电荷被屏蔽,ξ绝对值降低[16-18]。随着ξ绝对值降低,g-C3N4颗粒之间的静电排斥作用将随IS的升高而减弱,导致g-C3N4颗粒更容易受到范德华引力影响发生团聚,形成更大的团聚体[9],从而更容易在重力作用下发生沉降,分散稳定性随之降低。
此外,DLVO计算结果表明,随着水环境IS的升高,g-C3N4颗粒间的总势能(Wtotal)逐渐降低,其第二极小势能值则逐渐增大(图1b)。随着水环境IS由0.5上升至50.0 mmol/L,g-C3N4颗粒之间的第二极小势能值由-1.49×10-6变为-3.84×10-4。颗粒间的Wtotal越小,水体中的g-C3N4颗粒越容易跃过此势垒而发生团聚,从而更容易沉降,分散稳定性降低[19-21]。另一方面,g-C3N4颗粒也可能在第二极小势能处团聚,且第二极小势能值越大,团聚效应越明显,沉降程度越强[19-21]。DLVO理论计算结果同样表明,g-C3N4的沉降程度会随水环境IS的升高而逐渐增大,与沉降动力学研究结果相符。
2.2 pH值对g-C3N4沉降与分散稳定性的影响
IS为1.0 mmol/L、HA浓度为0 mg/L时,不同pH值条件下g-C3N4的沉降动力学曲线如图2a所示。试验结果表明,与IS相比,水环境pH值的变化对g-C3N4沉降和分散稳定性影响较小,g-C3N4悬液的终点C/C0均小于0.78。随着水环境pH值由2上升至10,g-C3N4的终点C/C0出现先升高后降低的情况(图2a)。随着水环境pH值由2上升至4,360 min后g-C3N4悬液的终点C/C0由0.63变为0.57,表明g-C3N4的沉降程度增强。而随着水环境pH值由4上升至10,360 min后g-C3N4悬液的终点C/C0由0.57变为0.78,表明g-C3N4的沉降程度降低。一阶动力学沉降模型结果显示,随着水环境pH值的升高,g-C3N4的sv值同样出现先升高后降低的情况(表2),模拟结果与试验结果相类似(决定系数均大于0.98)。
与沉降动力学研究结果类似,g-C3N4的水动力学半径也随水环境pH值的升高出现先增大后减小的现象(表2中编号为3、7、8、9、10的处理)。随着水环境pH值由2上升至4,g-C3N4的水动力学半径由1 116上升至1 271 nm;而随着水环境pH值由4上升至10,g-C3N4的水动力学半径则由1 271逐渐下降至862 nm。表面电位测定结果显示,水环境pH值为2时,g-C3N4的表面呈电正性。随着水环境pH值的升高,g-C3N4颗粒的表面ξ降低,由18.6逐渐变为-57.0 mV。已有研究结果表明,g-C3N4的等电点接近4[15,22]。水环境pH值为4的条件下,g-C3N4的表面ξ绝对值最小,颗粒间的静电排斥作用最弱,因而极易发生团聚,导致g-C3N4发生快速沉降。随着水环境pH值的进一步升高,g-C3N4表面的部分官能团去质子化程度增强,负电荷含量升高,表面ξ由-4.3逐渐变为-57.0 mV,颗粒间的静电排斥作用由弱变强,使得颗粒不容易发生团聚,沉降程度降低,分散稳定性随之升高[9,18,21]。水环境pH值对微/纳米颗粒的沉降和分散稳定性影响受颗粒自身性质的影响。研究表明,pH值的变化会影响多壁碳纳米管、微塑料的沉降、纳米二氧化钛(nTiO2)沉降及分散行为[23-25],而对氧化石墨烯、纳米二氧化铈(nCeO2)的沉降及分散行为影响不大[21,26]。
DLVO计算结果显示,当水环境IS为1.0 mmol/L时,g-C3N4颗粒间的第二极小势能值不明显,且随pH值变化较小(图2b),表明g-C3N4颗粒在第二极小势能处发生团聚的可能性较低。然而,随着水环境pH值由2上升至4,g-C3N4颗粒间的Wtotal由789明显下降至48.2,表明水体中的g-C3N4颗粒更容易越过能量势垒而发生团聚,团聚体在重力作用下失稳沉降,分散稳定性随之降低。随着水环境pH值进一步由4上升至10,g-C3N4颗粒间的Wtotal由48.2明显升高至4 870 kT,能量势垒明显增大,g-C3N4颗粒越过势垒团聚的可能性降低,其团聚受到抑制,沉降程度减弱而分散稳定性增强。
2.3 腐殖酸浓度对g-C3N4沉降与分散稳定性的影响
IS为1.0 mmol/L、pH值为6时,不同HA浓度条件下g-C3N4的沉降动力学曲线如图3a所示。试验结果表明,水环境中HA的存在能够明显降低g-C3N4的沉降程度,提高其分散稳定性。g-C3N4的沉降能够一定程度上随HA浓度的升高而降低,然而HA浓度变化对g-C3N4的沉降和分散稳定性的影响存在阈值。随着水环境HA浓度值由0提升至5 mg/L,360 min后g-C3N4悬液的终点C/C0由0.60变为0.87,表明g-C3N4的沉降程度大幅下降,其分散稳定性明显升高。然而,随着HA浓度值由5 mg/L进一步提升至10 mg/L,360 min后g-C3N4悬液的终点C/C0变化不明显,仅由0.87变为0.91,表明其沉降行为受影响较小。一阶动力学沉降模型结果表明,随着水环境HA浓度值由0提升至5 mg/L,g-C3N4的sv值降低,由最高0.0171下降至最低0.0161 cm/min,表明g-C3N4的沉降速率降低,分散稳定性增强。随着水环境HA浓度值由5提升至10 mg/L,g-C3N4的sv值变化不明显(表2),其变化趋势与试验结果一致(决定系数均大于0.97)。
随着水环境HA浓度的升高,g-C3N4的水动力学半径及表面ξ均出现先陡降后逐渐趋缓的下降趋势(表2)。研究表明,水体中的HA大分子能够吸附在微/纳米颗粒表面,并形成包裹层[18]。由于富含负电荷[17,27],包裹在g-C3N4表面的HA能够明显提高g-C3N4表面电负性,增强其颗粒间的静电排斥作用,降低g-C3N4颗粒的团聚及沉降,增强其分散稳定性。另一方面HA能够增强g-C3N4颗粒间的空间位阻效应,降低g-C3N4颗粒的碰撞,从而使g-C3N4颗粒的团聚及沉降程度减弱,分散稳定性增强[28-30]。另一方面,g-C3N4表面的HA包裹层厚度存在限值,一定程度后不再随HA浓度的增加而增厚,限值了其对g-C3N4的沉降和分散稳定性的影响。与本研究结果类似,Lyu等[31]研究表明,HA浓度对纳米CeO2在沙砾表面沉降行为的影响同样存在限值。
水环境中HA存在条件下,DLVO理论计算结果显示,g-C3N4颗粒间的Wtotal极高而第二极小势能值不明显(图3b),表明g-C3N4颗粒不容易在第一及第二势能处团聚,其沉降行为受到抑制,分散稳定性随之升高。
3 结论
本研究以广泛应用于农业有机污染物催化降解领域的石墨相氮化碳(Graphitic Carbon Nitride,g-C3N4)为研究对象,考察其在水体中的沉降和分散稳定性影响机制。研究结果表明,水环境离子强度(Ionic Strength,IS)、pH值和腐殖酸(Humic Acid,HA)均会对g-C3N4的沉降和分散稳定性产生影响,且影响程度各不相同。主要研究结论如下:
1)IS是影响g-C3N4沉降和分散稳定性的敏感因素。随着IS由0上升至50.0 mmol/L,360 min后g-C3N4悬液的终点标准化浓度(C/C0)由0.86变为0.58,表明g-C3N4的沉降随IS的升高而明显增强,分散稳定性降低。
2)水环境pH值变化对g-C3N4沉降和分散稳定性的影响较小。pH值接近等电点时(pH值为4)g-C3N4的沉降最明显,分散稳定性最强;随着pH值由4上升至10,360 min后g-C3N4悬液的终点C/C0由0.57变为0.78,表明pH值高于等电点时g-C3N4的沉降随pH值的升高而降低,分散稳定性逐渐增强。
3)水环境中HA的存在能明显抑制g-C3N4的沉降,提高其分散稳定性。随着HA浓度值由0提升至5 mg/L,360 min后g-C3N4悬液的终点C/C0由0.60变为0.87,表明g-C3N4的沉降一定程度上随HA浓度的升高而降低,其分散稳定性随之增强,且HA浓度对g-C3N4沉降和分散稳定性的影响存在阈值。
本文研究结果作为理论基础,能够为预测农业水环境中g-C3N4催化效率、评估g-C3N4的环境风险和生态安全提供科学依据,进而指导实际生产中g-C3N4的施用。目前,水环境中g-C3N4的沉降与分散稳定性研究正处于初期阶段,尚未形成完整综合的理论体系。在未来研究中,尤其值得关注农业污染水体的常见因素(如CO32-、SO42-、Ca2+、Mg2+等离子和重金属、农药、多环芳烃、抗生素等污染物)对g-C3N4沉降与分散稳定性的复合影响。
——《势能》

