红色荧光碳量子点用于肿瘤微酸环境诊断
黄靖 ,王丹阳 ,李淑花 ,范红 ,范楼珍 ,*
1北京师范大学化学学院,北京 100875
2首都医科大学附属北京朝阳医院,北京 100043
3山西省人民医院,太原 030012
1 引言
近年来,癌症已经成为危害人类身体健康的主要疾病1–3。肿瘤的早期诊断能显著提高癌症患者存活率或延长生存期4–6。目前,用于肿瘤诊断的荧光材料主要通过识别肿瘤细胞膜上特定的受体蛋白分子来实现,只能检测某一种或某一类肿瘤7–10。因此,利用肿瘤的独特性发展一种普适性荧光材料检测肿瘤非常重要11–13。
肿瘤的微环境指标,如低pH、低氧和高隙间压力是所有实体瘤的普遍特征14。低pH的主要原因是肿瘤细胞葡萄糖摄取率升高而氧化磷酸率降低,从而导致乳酸聚集15–17。肿瘤组织内的pH值为6.4–6.8,正常组织的pH值通常在7.0–7.4,因此在pH 6.8左右响应的荧光材料适合检测肿瘤18–20。传统pH响应的荧光材料多选用染料作为荧光剂,具有较大的毒性,响应范围比较宽,且容易受光漂白影响21–27。
碳量子点(CQDs)作为一种新型的零维碳纳米材料,由于低毒性、易于表面修饰、良好的水溶性、抗光漂白性以及优异的生物相容性等优点,被广泛应用于生物成像、药物传递等方面28–36。我们实验室已经报道了一种pH响应的荧光碳量子点(pRF-CQDs),当pH > 6.8时呈现蓝色荧光,而pH <6.8时呈现绿色荧光,但是蓝绿色短波荧光信号容易受生物体自身背景荧光干扰,因此需要设计一种红色的CQDs用于肿瘤微酸环境的诊断35。
我们以4-二甲氨基苯酚为前驱体,采用溶剂热法合成了一种红色荧光CQDs (R-CQDs),RCQDs荧光发射峰为640 nm,绝对荧光量子产率为12.8%,通过修饰单甲醚聚乙二醇衍生物(MeOPEG-PDPA),设计了pH响应红色荧光CQDs (pRFR-CQDs)37–43。当pH < 6.8时,pRF-R-CQDs的氨基质子化呈现红色荧光,而pH > 6.8时,pRF-R-CQDs的氨基去质子化导致红色荧光淬灭,因此能够利用荧光颜色差别区分出肿瘤组织和正常组织44–46。当肿瘤位置处没有形成明显肿块时,pRF-R-CQDs能够检测到微酸性肿瘤组织。因此,pRF-R-CQDs在临床肿瘤诊断方面具有潜在的实用价值。
2 实验部分
2.1 主要试剂及实验仪器
4‐二甲氨基苯酚(分析纯,阿法埃莎化学有限公司)、高碘酸钾(分析纯,上海阿拉丁生物科技有限公司)、单甲醚聚乙二醇2000 (分析纯,上海萨恩化学技术有限公司)。
荧光光谱仪(珀金埃尔默股份有限公司,Perkin Elmer-LS55)、紫外可见吸收光谱仪(岛津仪器有限公司,UV2450)、透射电子显微镜(日本电子株式会社,JEM2100),激光共聚焦荧光显微镜(徕卡仪器有限公司,LEICA STP)、流式细胞仪(美国BD公司,FACS Diva)、X射线光电子能谱(赛默飞世尔科技公司,Thermo Scientific)傅里叶变换红外光谱仪(赛默飞世尔科技公司,Nicolet)、小动物活体成像仪(珀金埃尔默仪器有限公司,IVIS Lumina Series)。
2.2 R-CQDs的制备
将20 mg的4-二甲氨基苯酚和60 mg的高碘酸钾溶解在10 ml的乙醇中,超声10 min,再将此溶液转移至25 mL的聚四氟乙烯的高压釜中,置于180 °C的烘箱中反应3 h。反应结束后,将此高压釜置于室温下冷却,在8000 r·min−1下离心10 min,除去不溶性杂质后将溶液烘干,在以CH3OH和CH2Cl2为洗脱剂(体积比1 : 25)的硅胶柱中分离后得到R-CQDs。
2.3 绝对量子产率的测量
采用配备120 mm积分球的FLR025光谱仪测量R-CQDs的量子产率。把FLR025光谱仪的测试光传送到积分球上,量子点的乙醇溶液放置在石英比色皿中,溶剂乙醇作为空白对照,测量R-CQDs的量子产率。
2.4 pRF-R-CQDs的制备
将10 g除水处理过的MeO-PEG-OH加入250 mL圆底烧瓶中,将圆底烧瓶浸入冰盐浴中不断搅拌,并滴加4.3 mL溴代异丁基酰溴,体系在室温下搅拌反应48 h。利用旋转蒸发仪除去THF,并将100 mL水加入剩余的有机相中,用二氯甲烷萃取有机相。对有机相依次进行洗涤、干燥、旋转蒸发,将得到的有机浓缩体系加入无水乙醚沉淀,减压抽滤得到大分子引发剂(MeO-PEG-Br)。在25 mL圆底烧瓶中加入0.56 g MeO-PEG-Br、14.4 mg催化剂CuBr、2.56 g甲基丙烯酸二异丙基氨基乙酯(DPAMA)和1.42 g R-CQDs。在瓶内保持氮气氛围下取配 体N,N,Nʹ,Nʺ,Nʺ- 五 甲 基 二 亚 乙 基 三 胺(PMDETA,99%)21 μL加入瓶中,将圆底烧瓶浸入60 °C油浴中反应48 h。通过中性A12O3柱除去催化剂和配体等杂质,得到嵌段共聚物(MeO-PEGPDPA)。将R-CQDs、MeO-PEG-PDPA和N-羟基琥珀酰亚胺混合后置于室温中于黑暗处剧烈搅拌并过夜反应,再将得到的溶液以CH3OH和CH2Cl2为洗脱剂(体积比1 : 20)在硅胶柱中分离,最终得到pRF-R-CQDs。
2.5 细胞活性检测
采用细胞计数法(CCK-8)检测细胞活性。将三种细胞悬液接种在96孔板中,培养板置于5% CO2、37 °C下预培养24 h。实验组向每孔加入10 μL不同浓度的pRF-R-CQDs缓冲溶液,空白对照组每孔加入10 μL生理盐水,再将培养板置于培养箱内孵育24 h。每孔加入10 μL CCK溶液,置于培养箱内孵育2 h,测定在450 nm处的吸光度值。
2.6 活体成像
活体成像实验所用动物为5–6周雌性裸鼠(15–20 g)。在裸鼠右腋下接种肿瘤细胞,至肿瘤体积达到约150 mm2进行活体成像实验。荷瘤裸鼠通过尾静脉注射100 μL pRF-R-CQDs缓冲溶液(剂量为5 mg∙kg−1)。注射后,在不同时间点采用活体成像仪收集荧光信号。此外,将注射12 h后的荷瘤裸鼠解剖得到肿瘤、肌肉、脑、肾、肠、脾、肺和心,在活体成像仪下观察肿瘤、肌肉和不同器官的成像。
2.7 组织成像
将肿瘤和腿部肌肉组织分别放平摆在组织支撑器中,滴入少许包埋剂,迅速置于冷冻台中。将冷冻的组织在冷冻切片机的机械承器上加紧,转动旋钮,将组织修复平整,制作冰冻组织切片(厚度:20 μm)。将切好的组织切片转移到载玻片上,在激光共聚焦荧光显微镜下观察,激发波长为561 nm。
3 结果与讨论
3.1 R-CQDs的荧光性质
图1a是R-CQDs水溶液在日光灯和365 nm紫外灯照射下的照片,R-CQDs水溶液发出明亮的红色荧光。图1b是R-CQDs的紫外可见吸收光谱图(UV-Vis)及荧光光谱(PL)。在波长为210 nm处存在明显的吸收峰,对应于sp2共轭结构的π–π*的跃迁吸收。在波长为285 nm附近存在一个较弱吸收峰,对应于C=O等结构的n–π*跃迁吸收,R-CQDs在545 nm处有特征吸收峰,对应的荧光发射峰位置为640 nm。图1c是不同pH下R-CQDs的荧光光谱,荧光强度在pH 6–8范围内无明显变化,表明RCQDs的荧光强度在pH 6–8范围内受pH影响较小。在30天的连续光照下,如图1d所示,R-CQDs的荧光强度没有明显变化,具有良好的稳定性。

图1 (a)日光灯(左)和紫外灯(右)照射下的R-CQDs水溶液,(b)R-CQDs的UV-Vis和PL光谱图,(c)R-CQDs在不同pH下的PL光谱(激发波长540 nm),(d)R-CQDs的荧光稳定性Fig. 1 (a)The photographs of R-CQDs aqueous solution under visible light and UV light, (b)UV-Vis absorption and PL spectra of R-CQDs, (c)PL spectra of R-CQDs at different pH, (d)Photostabilities of R-CQDs.
3.2 R-CQDs的形貌与结构表征
透射电子显微镜(TEM)结果表明R-CQDs的尺寸大小约为4 nm (图2a),高分辨透射电镜(右上插图)结果显示,R-CQDs的晶格间距为0.21 nm,对应于石墨烯(100)晶面的衍射。X射线光电子能谱(XPS)如图2b–d所示,R-CQDs主要由C、N、O三种元素组成,原子百分比分别为85.77%、4.32%、9.91%。R-CQDs的C 1s谱图中主要有284.8 eV一个比较强的峰,对应于石墨类sp2杂化C原子(C=C)的结合能。另外在285.8、286.4和287.8 eV处还有三个较弱的峰,分别对应于C―N、C―O和C=O的结合能。R-CQDs的N 1s峰位置分别位于399和400.6 eV,分别对应于氨基氮和石墨化氮。在傅里叶变换红外(FT-IR)光谱中(图2e),1065、1405、1640和3456 cm−1的峰分别对应于C―N、C=C、C=O和O―H的伸缩振动。拉曼(Raman)光谱图(图2f)中可以看到R-CQDs在1340和1585 cm−1处分别出现石墨烯特有的D峰和G峰,ID/IG值约为0.81,表明R-CQDs结晶性良好,缺陷较少。图2g是R-CQDs的X射线衍射(XRD)图,在23°左右出现一个弱而宽化的衍射峰,对应石墨(002)晶面间距。以上结构表征结果表明,R-CQDs表面含有大量的羰基和羟基,氮元素主要以石墨氮的形式存在,由此推断RCQDs的结构示意图(图2h)。
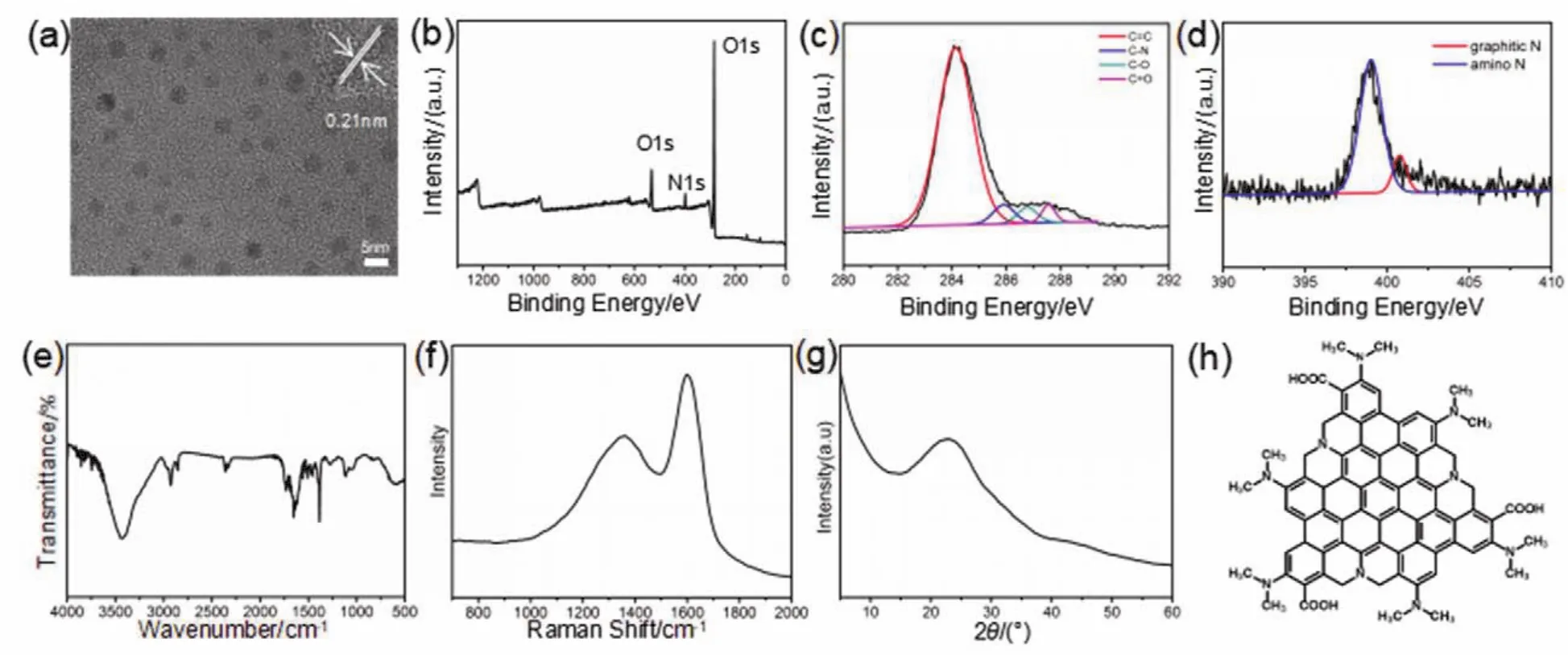
图2 R-CQDs的(a)TEM图,(b–d)XPS图,(e)FT-IR光谱图,(f)Raman光谱图,(g)XRD图谱,(h)结构示意图Fig. 2 (a)TEM images, (b–d)XPS analysis, (e)FT-IR spectra, (f)Raman spectrum, (g)XRD spectrum,(h)structure diagram of R-CQDs.
3.3 pRF-R-CQDs的荧光性质
图3a为pRF-R-CQDs的结构示意图。图3b是365 nm紫外灯激发下不同pH值的pRF-R-CQDs缓冲溶液外观图,当pH < 6.8时溶液呈现红色荧光,当pH > 6.8时溶液荧光淬灭。不同pH值下荧光光谱图(图3c)显示,pRF-R-CQDs溶液在pH > 6.8时荧光基本淬灭。当pH < 6.8时,且其荧光强度明显增高,pH 6.5时荧光最强。实验中通过酸碱滴定的方法确定了pRF-R-CQDs的pKa值,图3d是酸碱滴定曲线,计算了pRF-R-CQDs的pKa约等于6.76,非常接近于荧光突变点6.8。图3e是不同pH值下pRF-R-CQDs的TEM照片,当pH > 6.8时pRF-R-CQDs的氨基去质子化呈现胶束状,当pH < 6.8时pRF-R-CQDs的氨基质子化呈现胶束解离状。
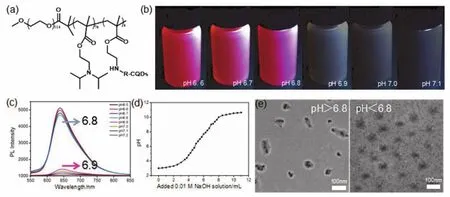
图3 (a)pRF-R-CQDs的分子结构,(b)不同pH条件下pRF-R-CQDs在紫外灯(365 nm)照射下的照片,(c)不同pH下pRF-R-CQDs的荧光光谱(激发波长540 nm),(d)pRF-R-CQDs的酸碱滴定曲线,(e)不同pH条件下pRF-R-CQDs的TEM图Fig. 3 (a)Structure diagram of pRF-R-CQDs. (b)Photographs showing fluorescence under UV light (excited at 365 nm)of the pRF-R-CQDs at different pH values. (c)Fluorescence spectra excited at 540 nm of pRF-R-CQDs at different pH values. (d)Potentiometric titration curves of pRF-R-CQDs. (e)TEM images of pRF-R-CQDs at different pH.
3.4 pRF-R-CQDs用于肿瘤组织检测
将pRF-R-CQDs分别皮下注射至四种荷瘤裸鼠(肿瘤类型分别为HepG2、PANC-1、HCT116和A549)的肿瘤和腿部肌肉处,12 h之后将肿瘤和腿部肌肉取出,冷冻切片后放置于激光共聚焦荧光显微镜下观察。如图4所示,四种肿瘤组织相对于正常组织即腿部肌肉组织密而细,并且发出明亮的红色荧光,而腿部肌肉组织未呈现荧光。结果表明pRF-R-CQDs可以避开生物自身荧光的干扰,利用肿瘤微酸性区分出正常组织和肿瘤组织。
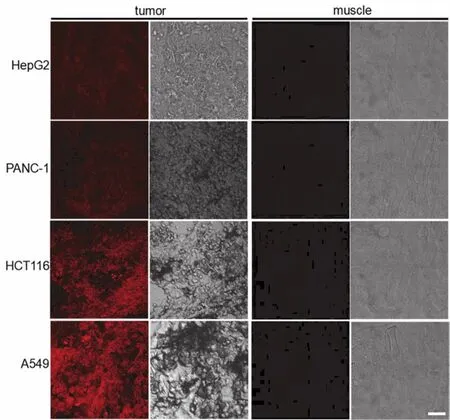
图4 pRF-R-CQDs分别皮下注射至HepG2、PANC-1、HCT116和A549荷瘤裸鼠的肿瘤和腿部肌肉处,12 h之后肿瘤组织冷冻切片(左二)和腿部肌肉组织冷冻切片(右二)的激光共聚焦荧光显微镜照片及相应的明场照片(标尺:24 μm)Fig. 4 Representative confocal microscopy images of indicated tumors in red fluorescence channel and white field(left two panels)and muscles in red fluorescence channel and white field (right two panels). Scale bars: 24 μm.
3.5 pRF-R-CQDs用于肿瘤诊断
将pRF-R-CQDs缓冲溶液通过尾静脉注射至HeLa荷瘤裸鼠体内,注射后选用活体成像仪收集荧光信号。图5a为pRF-R-CQDs注射后不同时间点的活体成像图。从图中可以观察到,注射2 h后,在肿瘤处观察到微弱的红色荧光信号,说明pRFR-CQDs在参与裸鼠血液循环中能够识别微酸性环境。由于肿瘤的被动靶向性,pRF-R-CQDs在肿瘤处聚集,其荧光信号随时间增强。24 h后裸鼠肿瘤处的荧光信号明显减弱,表明pRF-R-CQDs在裸鼠体内逐渐被代谢排出体外。解剖得到的主要器官荧光成像结果如图5b所示,由于失调的糖酵解引起肿瘤细胞间呈现微酸环境,所以pRF-R-CQDs在肿瘤处显示红色荧光,即pRF-R-CQDs可以应用于肿瘤的诊断。

图5 (a)荷瘤裸鼠通过尾静脉注射pRF-R-CQDs (5 mg∙kg-1)后不同时间的活体成像图,(b)12 h后解剖得到肿瘤、肌肉和各个器官的荧光成像图,(c)裸鼠接种肿瘤后,不同时间尾静脉注射pRF-R-CQDs后的活体成像图Fig. 5 (a)Representative images of a HeLa tumor-bearing mouse at the indicated time points after intravenous injection of pRF-R-CQDs (5 mg∙kg−1). (b)Imaging of tumor, muscle, major organs from a mouse treated with pRF-R-CQDs.(c)After tumor inoculation, mice were intravenously administered pRF-R-CQDs solution at a dose of 5 mg∙kg−1 every days. Twelve hours after each injection, mice were imaged.
将含1 × 106个细胞(0.1 mL)的HeLa细胞悬液皮下注射到裸鼠右侧腋窝。接种后每天将pRF-RCQDs缓冲溶液尾静脉注射到裸鼠体内,12 h后进行活体成像,重复观察10天。从图5c中可以看出,HeLa细胞植入裸鼠体内第3天时,可以观察到裸鼠的右腋出现微弱的荧光信号,而此时对应的灰度图中没有明显的肿块,第8天时该位置出现明显的凸起,有微小的肿块长成,荧光信号比较明显。随着HeLa细胞植入天数的逐渐增加,肿瘤继续增大,同时肿瘤的荧光信号也逐渐增强。实验结果表明,当肿瘤位置处产生微酸环境并没有形成明显的肿块时,pRF-R-CQDs可以显示荧光信号,有助于实现肿瘤的早期诊断。
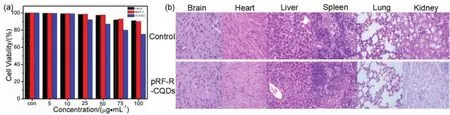
图6 (a)HeLa细胞、MCF-7细胞和HUVEC与不同浓度pRF-R-CQDs溶液作用后的细胞活性图,(b)主要器官苏木精-伊红染色切片(标尺:40 μm)Fig. 6 (a)Cytotoxicity of pRF-R-CQDs on indicated cells. (b)Representative images of indicated tissues with H&E staining, Scale bars: 40 μm.
3.6 pRF-R-CQDs的毒性测试
评估了pRF-R-CQDs对三组细胞的毒性,其中HeLa与MCF-7为肿瘤细胞,HUVEC (人脐静脉内皮细胞)来自正常组织。将一系列不同浓度pRF-RCQDs依次添加到细胞中,24 h后测定细胞活力。图6a表明pRF-R-CQDs在浓度高达100 μg∙mL−1时不表现出明显的毒性。进一步研究pRF-R-CQDs对活体动物的毒性。给健康小鼠每隔一天尾静脉注射pRF-R-CQDs,在第15天取出脑、心、肝、脾、肺、肾等主要器官,并切取后进行苏木精-伊红染色图6b,与对照组相比,pRF-R-CQDs处理过的小鼠的主要器官中均未出现明显的毒性。结果表明pRFR-CQDs在临床癌症诊断方面具有较大的潜能。
4 结论
合成了一种红色荧光碳量子点R-CQDs,并将MeO-PEG-PDPA修饰到其表面,制备了一种pH 6.8响应荧光碳量子点(pRF-R-CQDs)。当pH值小于6.8时呈现红色荧光,当pH值大于6.8时其荧光淬灭,能够实现肿瘤的诊断。由于pRF-R-CQDs能够区分肿瘤和正常组织,具有低毒性以及对肿瘤的高特异性和敏感性等特点,因此在肿瘤早期诊断方面有广泛的应用前景。此外,通过本研究中描述的方法可能合成近红外波长的荧光碳量子点用于肿瘤诊断。
- 物理化学学报的其它文章
- Photocrosslinking-Immobilized Polymer Vesicles for Lowering Temperature Triggered Drug Release
- Poly(ε-caprolactone)-Polypeptide Copolymer Micelles Enhance the Antibacterial Activities of Antibiotics
- ReaxFF MD局部区域反应追踪与物理性质可视化分析
- 稀土-天然皮革可穿戴X射线防护材料的合成及性能
- 石墨烯玻璃透明薄膜加热特性
- Single-Molecule Field-Effect Transistors with Graphene Electrodes and Covalent Pyrazine Linkers

