羟基磷灰石在脂肪干细胞相关骨组织工程中的应用热点研究*
申 杰,张司玺,曹志威,张春阳,赵志军
(1.内蒙古科技大学包头医学院,内蒙古 包头 014010;2.内蒙古科技大学包头医学院第一附属医院神经外科;3.内蒙古自治区骨组织再生与损伤修复工程技术中心)
脂肪干细胞(Adipose Derived Stem Cells,ADSCs)是近年来被广泛研究具有自我复制和多向分化潜能的间充质干细胞。具有明确的定向成骨分化能力、自身储存量巨大且易于提取与分离、体外培养能够稳定增殖传代,且较低的免疫原性可用于自体移植等优点,广泛应用于各类与骨组织相关的科学研究领域中[1-2]。随着材料制造技术的进步,重建天然细胞外基质(ECM)结构、诱导细胞成骨矿化、更好的骨力学性能成为羟基磷灰石(Hydroxyapatite,HA)及其相关材料新的发展方向。本文从HA及其多种新型材料的成分组成及结构特性以及对ADSCs增殖活性及成骨分化的不同影响入手,通过对近年来出现的多种新型HA支架材料进行总结,旨在为HA及ADSCs所构成的生物组织工程骨的基础研究与应用发展提供更多的借鉴和指导。
1 单纯HA及其纳米材料
ADSCs成骨特性主要受诱导环境及成骨诱导因子影响,HA具有良好的骨传导性及化学稳定性,且人工合成的HA与正常人体骨组织中无机成分高度相似,可塑的孔隙结构能够促进ADSCs成骨分化的特点使HA成为ADSCs在骨组织工程中最常应用的支架材料之一。程胜承等[3]将ADSCs与HA共培养时发现,HA的存在可以提升ADSCs成骨标志物—碱性磷酸酶(ALP)活性及相关成骨基因COL1A1、OPN、Runx2的表达水平,且梯度培养证明,浓度为20 mg/L的HA成骨诱导能力最佳,但随着HA浓度提升,反而会抑制ADSCs增殖。
随着纳米科技的发展,纳米羟基磷灰石(Nano-Hydroxyapatite,nHA)以其较小粒径,能够释放Ca2+和PO43-促进ADSCs成骨分化[4]。与ADSCs混合制成基质胶注射入骨髓腔中,治疗I型成骨不全[5]。通过电子显微镜观察发现,nHA纳米微环境拥有相互连通的孔隙类似于天然细胞外基质(ECM)结构,可提高相关分子的传输效率,并为ADSCs的附着提供充足接触面积,而这种特殊的纳米结构很可能与细胞黏着斑(Focaladhesion)之间存在一定的相互作用[6]。因此nHA可在缺乏成骨诱导环境的情况下促进ADSCs定向分化为成熟骨细胞。
2 共聚复合材料
尽管单纯HA具有良好的可塑性,但其如陶瓷般的脆性及较差的延展性等缺点,很大程度上限制其在骨组织工程中的应用前景。增加适度的柔韧性,提升其断裂伸长率并改善HA的力学性能,甚至通过重塑微环境结构使其更有利于ADSCs的贴附生长及成骨矿化,与其他生物材料进行共聚复合成为HA改性的重要方法。Wang等[7]将聚癸二酸甘油酯(PGS)中的氢氧根替换马来酸酐(gM)并与HA复合制成新型nHA/PGS-M复合支架,拥有良好回弹力的同时,150~300 μm大小的孔隙结构在接种ADSCs之后可以促进其成骨分化,Runx2、骨钙素、Col1A1等成骨相关因子表达也增高。
胶原蛋白(Collagen)及其水解产物明胶(Gelatin)均具有良好的生物活性及结构弹性,成为改善HA固有脆性的复合选择。Weiss-Bilka等[8]将HA与胶原蛋白复合,制成拥有较高孔隙率、适宜手术固定的圆孔结构、良好弹性及延展性的支架材料,这种新型的胶原蛋白/HA复合支架不仅能够促进ADSCs向成骨细胞分化,还能促进血管生成以及钙质沉积。Mazzoni等[9]也研发制备名为Coll/Pro Osteon 200的新型HA/胶原蛋白共聚支架,复合ADSCs用于治疗颌面部骨缺损病人并取得良好疗效,ALP、OGN和CLEC3B等基因的表达增高,临床评估显示该新型支架材料有促进ADSCs成骨分化及骨骼再生的作用。而在明胶与HA共聚应用方面,Sattary等[10]使用电纺丝技术成功制备聚己内酯/明胶/nHA/Vit D3新型复合支架,兼具柔韧性的同时nHA与Vit D3协同作用使ADSCs的成骨分化能力大大提升,ALP和Runx2的成骨表达期提前21 d。Wenz等[11]将甲基丙烯酰基修饰后的明胶与nHA复合而成三维支架,将ADSCs与人真皮微血管内皮细胞(HDMEC)共同封装进行培养14 d后,ADSCs成骨分化能力增强,同时微血管的稳定增殖也有利于ADSCs分化和增殖。Amjadian等[12]将左旋聚乳酸(PLLA)与明胶采用静电纺丝技术合成纳米纤维,再将nHA嵌入其中制成新型支架材料,将常用的成骨诱导成分—地塞米松渗入支架孔隙之中,用以诱导ADSCs的成骨分化并取得明确效果。ALP活性、钙盐沉积和相关成骨基因表达均增加,而这种新型支架优异的机械强度和拉伸性使其成为骨组织工程中支架材料的优秀选择。Lee等[13]也做过类似研究,其在PLLA/明胶/HA支架材料中,利用PLLA的药物控释特性将辛伐他丁(Simvastatin,SIM)包封其中,同时用β-环糊精(β-CD)作为连接剂稳定支架的力学性能(如图1),ALP及茜素红染色显示这种支架材料不仅能够促进ADSCs矿化,同时相较于无SIM的对照组,Runx2等成骨基因表达上调,说明SIM修饰的新型支架对ADSCs的成骨分化能力也具有促进作用。
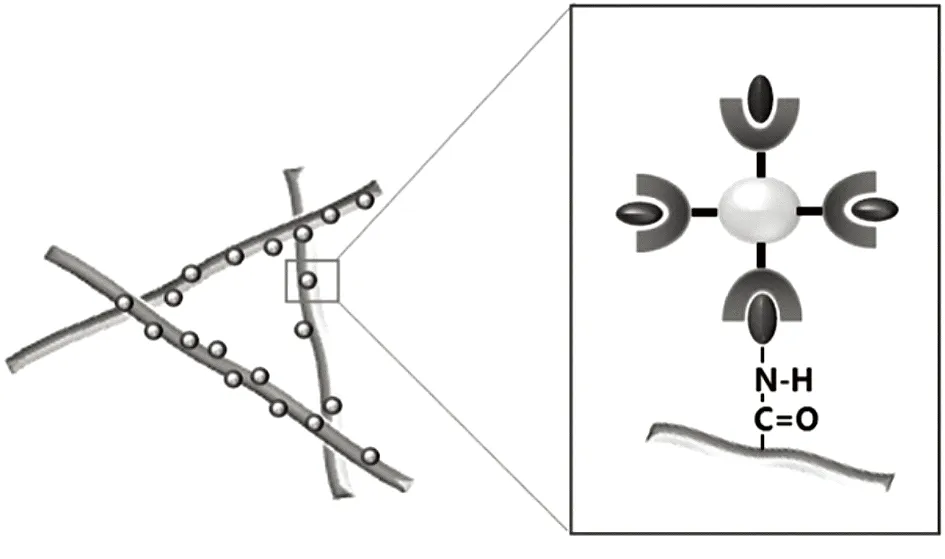
图1 β-环糊精修饰并控释辛伐他丁的PLLA/明胶/HA支架
丝素蛋白(Silk Fibroin,SF)是通过去除蚕丝中的丝胶,避免免疫排斥反应而获得的一种天然可降解的高分子纤维蛋白,具有良好的降解性、可塑性、生物相容性和力学性能等,优点使其在外科领域中有着广泛的应用历史。利用SF的优良韧性和可降解性,改变HA降解缓慢且脆性较高的缺点。施咏毅[14]将复合ADSCs的SF/HA支架植入兔股骨远端骨缺损取得了较好的修复效果。刘浩等[15]利用3 mL浓度为1 %的丝素蛋白与480 mg的nHA干粉混合干燥后,制备SF/HA支架,在接种ADSCs后通过MTT法和碱性磷酸酶分别检测其细胞活性和成骨能力后发现,相较于两种单纯材料,复合后的新型材料不仅在力学性能和结构强度上有更好的表现,其促成骨能力也更强。丁晓明等[16]采用相分离/沥滤技术制备的SF/HA多孔性支架拥有更好的结构性能,其均匀且相互连通的多孔结构更适宜ADSCs的贴附和生长,随着诱导时间的延长,相关成骨基因OPN及Osteonectin的表达量也随之增加。Eunkyung等[17]也利用静电纺丝技术,将HA颗粒混合于丝素蛋白纳米材料中,通过粘附性聚多巴胺(PDA)将另一部分HA颗粒固定于材料表面形成层功能化HA/SF纳米支架材料(如图2),不仅其力学性能得到改善,且能够为ADSCs提供更为优异的成骨矿化环境。通过质粒转染转录共激活因子(TAZ)对ADSCs进行基因修饰进一步增强其成骨能力,并在动物模型中实现较好的临界大、小颅骨缺损修复效果[17]。丁涛等[18]更是在SF/HA支架的基础上,复合经骨形态发生蛋白-14(BMP-14)转染的ADSCs修复大鼠尾椎缺损,这种支架材料不仅能够促进ADSCs的黏附和增殖,同时BMP-14促进ADSCs成骨分化并与SF/HA融合形成新骨,术后8周可见修复部位骨密度增高,并有大量骨痂形成。

图2 双层功能化HA/SF纳米支架结构示意图
β-磷酸三钙(β-Calcium Phosphate Tribasic,β-TCP)由钙和磷构成,是磷酸三钙的高温相,具有良好的生物相容性、能与骨组织直接融合、无炎症等不良反应的优点,使其成为骨组织工程领域的常用材料。其钙磷原子比为1.5,相比HA更易在体内降解吸收,同时与HA复合而成的HA/β-TCP支架,可根据其不同的表面构造、结晶构型决定其支架材料的强度和体内降解速率,适宜的孔隙大小能够更好的引导ADSCs迁移和增殖,促进ADSCs向成骨细胞分化。王腾飞等[19]利用成分比为6∶4的HA/β-TCP支架材料搭载ADSCs后修复兔腰椎缺损,修补区的新型材料基本降解吸收,实现材料与正常骨组织的骨性结合。Hashemibeni等[20]将ADSCs复合于HA/β-TCP后,用以修补犬胫骨圆柱形骨缺损后发现,相较于单纯使用HA/β-TCP在修补部位形成更加厚实的骨小梁和矿化基质,修复后的骨质硬度较好。吴洪亮[21]也利用HA/β-TCP作为人工骨支架载体,复合经低氧诱导因子-1α(Hypoxia Inducible Factor-1α,HIF-1α)转染的ADSCs后对兔股骨头坏死进行移植修复,利用HIF-1α的高表达促进血管生成以改善缺血现象,同时矿化的ADSCs复合HA/β-TCP实现较好的股骨头再生,这不仅为骨组织工程学应用于临床复杂结构的骨修复建立了实验基础,同时也为骨替代治疗中血管生成这一难题提供了新的思路和方向。
聚乳酸(Polylactic Acid,PLA)是一种可由淀粉原料提炼制成的新型生物可降解材料,其良好的可塑性,降解无毒及药物控释等特性在材料及药物领域被广泛研究。在上述HA与明胶共聚物的骨修复研究中,聚乳酸多次出现。Smieszek等[22]更是发现左旋聚乳酸(PLLA)与nHA最适配比,当nHA在聚合材料中占比10 %时ADSCs的黏附力及其增殖活性最好。与此同时,聚乳酸还有另外一种与HA合作的特别方式,Ma等[23]采用流动蒸发法在nHA的表面形成一层PLA纳米膜,其nHA侧可以有效促进ADSCs成骨分化,PLA膜的隔绝效果可以有效防止ADSCs与其他组织细胞共同黏附于HA材料表面造成的组织粘连,达到更好的骨缺损修复效果。
3 元素修饰材料
通过复合其他生物材料达到HA改性之外,一些元素的修饰和掺杂也可以发挥类似作用。锶元素(Sr)是一种类似钙生物学功能的人体所需微量元素之一,可以取代骨基质中HA的钙而提升骨质强度,因此临床中常用雷奈酸锶治疗骨质疏松。锶对ADSCs的成骨分化具有明确作用,因此陈龙[24]将锶修饰于HA支架,不仅能提升HA支架的力学性能和结构强度,还能有效提高ALP活性,加速ADSCs的矿化成骨。硼元素(P)也是人体所需微量元素之一,虽然还未阐明其在胚胎或人体发育中的具体机制,但硼对人体骨骼再生作用已经充分得到证实[25]。Akdere等[26]将硼元素添加至HA相关支架材料中,在不同的2D和3D培养环境中均较无硼材料更能促进ADSCs的黏附、增殖及成骨分化,骨传导性也更好。硅(Si)是自然界极为常见的一种元素,在骨组织工程中也得到广泛应用。Eatemad等[27]为改善HA降解速率慢的缺点,将硅元素加入到HA的支架材料中,复合ADSCs后发现硅元素的存在不会对ADSCs产生毒性作用,HA经硅修饰后形成的Si-HA微粒有较高的降解速率,能够释放出更多的离子并促进ADSCs成骨及基质矿化,这些元素的掺杂和修饰不仅能够在HA基础上对ADSCs的生物活性和成骨矿化起到一定的促进作用,同时也为相关特殊骨组织疾病的修复治疗提供更多的生物支架和涂层材料的个性化选择与应用。
4 结语与展望
HA作为最常用的骨替代材料被广泛应用,但随着骨组织工程学的不断发展,与其他学科诸如材料化学、临床医学的不断交融,单一材料的使用缺陷被逐渐放大,因此拥有更优性能的多种复合材料为HA相关材料在骨组织工程中的应用开辟了新道路。与此同时,HA对ADSCs成骨特性的改变也在HA相关材料的不断发展中得到更好表现,但制约其真正应用于临床还有许多问题有待解决。如调配HA相关骨组织工程材料内部各成分的比例,以适应修补缺损部位所需的结构强度和ADSCs生长﹑吸附的孔径大小;其降解控释速率如何匹配新骨生成而不至于过快导致支架塌陷或过慢限制骨细胞增殖;血管生成这一关键问题在HA相关材料临床应用中如何有效解决等。HA相关支架材料的不断研究与发展,提升ADSCs成骨和矿化能力,优化其结构与力学特性,实现更好的骨缺损修复效果,对骨组织工程的应用和前景有着十分重要的意义。

