内镜下食管静脉曲张套扎术治疗乙型肝炎肝硬化并发食管胃底静脉曲张破裂出血患者再出血风险观察*
叶 东,张俊霞,李 洁,刘 颖,张 丹,郭永泽
食管静脉曲张(esophageal varices,EV)是乙型肝炎肝硬化(liver cirrhosis,LC)患者病程发展过程中的重要并发症。EV破裂出血则是LC患者的重要死因[1]。近年来,随着内镜技术的进步,内镜下食管静脉曲张套扎术(endoscopic variceal ligation,EVL)被广泛应用于临床[2,3],止血效果得到显著的提高,患者病死率也显著降低。但超过30%患者在术后存在不同程度的再出血,既往报道多关注肝功能因素对术后出血的影响[4,5],而近来有研究显示并发肝性糖尿病患者术后再出血发生率更高[6]。本研究采用EVL治疗了LC并发EV患者,观察了术后出血情况,并建立预测模型分析了影响再出血的因素,现报道如下。
1 资料与方法
1.1 一般资料 2016年4月~2019年10月我院诊治的乙型肝炎肝硬化并发EV破裂出血患者178例,男性102例,女性76例;年龄为(54.9±10.3)岁。符合中华医学会发布的肝硬化诊断标准[7],参照中华医学会外科学分会发布的共识标准[8]诊断EV,其中Child-Pugh A级40例,B级64例,C级74例。并发肝性糖尿病86例。排除标准:①并发有严重的心肺基础疾病;②凝血功能障碍;③并发恶性肿瘤;④有原发性胃溃疡或糜烂性胃炎。本研究经河北工程大学附属医院医学伦理委员会审批同意(批号:2016-4),患者或家属签署知情同意书。
1.2 EVL治疗方法 术前动态监测心电图,完成血常规和凝血功能指标检测,排除有下列禁忌证患者,即食管曲张静脉直径>2 cm、肝肾功能严重不全、肝性脑病≥2期,不能配合治疗或存在食管狭窄者。在KPS评分≥70分、生命体征平稳、凝血功能指标正常后开始手术。手术时,患者取左侧卧位,使用奥林巴斯GIF-XQ140型胃镜行常规胃镜检查,明确食管曲张静脉的位置、程度,退镜。安装套扎器,再次进镜至贲门口上约5 cm处,用内镜的透明帽抵住曲张静脉,连续负压吸引后,旋转牵引钮,听到“咔”的声音后,注入少量气体,见曲张静脉呈深紫色,即表示套扎成功。再根据病变部位,由下而上选择下一个套扎点。每个套扎点间隔1.0~4.0 cm,使套扎点居于不同的水平面,查看无出血后退镜。
1.3 随访 在EVL术后即进入随访,行常规检测和检查,记录术后再出血情况。出血的诊断参照有关指南标准进行[9]:发生呕血、黑便或胃管内有血性液体,或外周血血红蛋白(Hb)下降>20 g/L,有出血表现者。
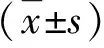
2 结果
2.1 一般情况 在178例患者中,12例(6.7%)患者在首次出血后,内科治疗失败,未行EVL治疗即死亡。166例接受EVL治疗,止血均获得成功。
2.2 随访情况 在接受EVL治疗的166例患者中,随访12~54个月,无失访病例,其中27例(16.3%)发生再出血。
2.3 再出血与未再出血患者血清指标比较 入院时,再出血组外周血Hb和血清白蛋白水平显著低于未再出血组(P<0.05),而空腹血糖(FPG)和糖化血红蛋白(HbA1c)水平显著高于未再出血组,差异均有统计学意义(P<0.05,表1)。

表1 再出血与未再出血患者血清指标比较
2.4 再出血与未再出血患者门脾静脉指标比较 入院止血后检查,发现再出血患者门静脉和脾静脉宽度显著大于未再出血组(P<0.05,表2)。

表2 再出血与未再出血患者门脾静脉指标比较
2.5 EVL后再出血的Cox风险模型分析情况 将可能影响EVL后再出血的因素纳入Cox风险回归模型,分析结果显示Child-Pugh分级、腹水、HbA1c、FPG和肝性糖尿病是术后再出血的独立影响因素(P<0.05,表3)。
表3 EVL后再出血的Cox风险模型分析
2.6 术后再出血预测模型的建立与应用 根据Cox风险回归模型分析结果,建立判断EVL后再出血的Nomogram预测模型,并绘制其校正曲线(图1),计算其C-index值为0.836。根据Nomogram列线图模型,以Nomogram得分为检验变量,以是否在EVL术后再出血为状态变量,绘制ROC(图2),结果显示Nomogram判断术后再出血的AUC为0.804(SE=0.053,95%CI=0.700~0.907,P=0.000),其敏感度为0.857,特异度为0.565。
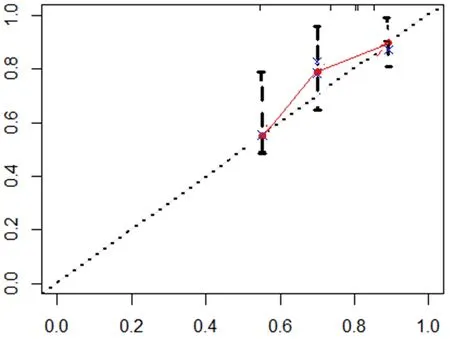
图1 Nomogram判断EVL术后再出血的校正曲线

图2 Nomogram判断术后再出血风险的ROC分析
3 讨论
EVL是LC并发EVB患者主要的治疗方法,其止血率超过90%[10]。Meta分析显示EVL止血效果显著优于内科治疗,并得以临床的公认[11]。近年来,研究显示EVL后再出血率超过20%,并认为LC并发EVB患者在术后再出血与曲张静脉数、Hb、Alb、腹水、糖尿病和门静脉血栓等因素有关[12,13]。在LC并发EVB患者,尽管紧急止血能取得一定的止血效果,但因肝性糖尿病的持续存在,往往发生再出血。在肝性糖尿病发生后,肝糖原合成障碍或储备减少[14,15],因而临床多见餐后血糖升高,而FPG未显著升高。随着肝功能的恶化,肝性糖尿病病情加重,肝糖原储备进一步减少,FPG水平降低,甚至出现空腹低血糖现象[16]。对于EVL术后患者,并发肝性糖尿病者术后糖代谢紊乱,血糖存在持续的波动状态,造成曲张静脉术后愈合时间延迟[17],成为术后出血的诱因。HbA1c能反映患者8~12周内血糖水平,已得到国家专业委员会和美国糖尿病协会的认可[18,19],能客观地反映糖代谢水平。
Child-Pugh评分与术后再出血率呈正相关性[20],EVL术后肝细胞代偿修复能力与术后再出血密切相关,肝脏是合成凝血因子的重要器官,术后肝脏受损和肝功能状态直接影响凝血因子的合成,进而引起术后再出血的发生。对于LC并发EVB患者,应严密监测肝功能状态,尽早消退腹水,以降低术后再出血的发生。另有报道,门静脉血栓的形成使门脉血流速度降低,不仅使EVL消除静脉曲张的时间延长,更可能进一步加重肝损伤,增加再出血的风险。
本研究随访观察了166例接受EVL治疗的LC并发EVB患者的再出血情况,结果显示EVL术后再出血发生率为16.3%,与有关报道相近。并发肝性糖尿病患者术后再出血发生率高。本研究根据Cox风险模型分析结果建立判断LC并发EVB患者术后再出血的Nomogram预测模型,并绘制校正曲线,其C-index值达0.836,而ROC分析结果发现该模型判断术后短期再出血风险的敏感度达0.857,说明该模型用于判断EVL术后再出血具有较高的实用性。

