促性腺激素释放激素类似物治疗对中枢性性早熟和快速进展型青春期患儿成年终身高改善的Meta分析
储昭乐 江辉 吴倩
(安徽省桐城市人民医院儿科,安徽桐城231400)
中枢性性早熟(central precocious puberty,CPP)是指由于下丘脑-垂体-性腺轴(hypothalamiepituitary-gonadal axis,HPGA)功能提前启动而导致女孩8岁前、男孩9岁前出现内外生殖器官快速发育及第二性征呈现的一种常见儿科内分泌疾病[1]。由于骨骼成熟较快,骨龄超过实际年龄,骨骺提前愈合,影响患儿的成年终身高(final adult height,FAH),另外由于第二性征过早发育及性成熟,可能会有相应的心理问题或社会行为异常。快速进展型青春期(early and fast puberty,EFP)为性早熟界定年龄后至正常青春发育年龄前,即女孩8~10岁、男孩9~11岁出现HPGA启动伴性征发育,但发育进程迅速,从一个发育分期进展到下一分期的时间较短(<6个月),生长速率增加、骨骼成熟迅速,短期内出现骨龄明显超过实际年龄,因骨骺早期愈合而影响FAH。
促性腺激素释放激素类似物(gonadotropinreleasing hormone analogue,GnRHa)的作用机制是与垂体前叶促性腺细胞的GnRH受体结合,开始可短暂促进黄体生成素(luteinizing hormone,LH)、卵泡刺激素(follicle-stimulating hormone,FSH)一过性释放增多(“点火效应”),继而使垂体靶细胞相应受体发生下降调节,抑制垂体-性腺轴,使LH、FSH和性腺激素分泌减少,从而控制性发育进程,延缓骨龄进展,从而保留骨生长板的生长潜能,实现身高追赶[1]。研究表明,6岁前患儿的GnRHa治疗明确能改善其FAH[2-4],但对于年龄大于6岁CPP/EFP患儿的GnRHa治疗对FAH的改 善仍然存在争议,一些研究报告了相互矛盾的结果,一些文章报道了GnRHa能改善CPP/EFP患儿FAH[5-11],而另外一些研究认为GnRHa不能改善FAH[12-14],为此,本研究检索GnRHa治疗青春期提前的相关文献,对年龄在6岁以后的患儿,集中在身高方面的数据进行定量综合,以期为临床治疗提供循证依据。
1 资料与方法
1.1 纳入和排除标准
(1)文献纳入标准:①随机对照研究和病例对照研究;②CPP和EFP患者,治疗年龄大于6岁;③对照组未接受治疗,GnRHa治疗组(以下简称试验组)采用GnRHa治疗;④观察指标:FAH、预测成年身高(predictive adult height,PAH)、遗传身高(target height,TH)、FAH的标准差分 值(FAH standard deviation score,FAHSDS)、身高获益(FAH-PAH);⑤文献语种为英文和中文。
(2)文献排除标准:①重复收录的文献;②合并其他疾病的患儿;③联合其他药物治疗的试验;④无需要的结局指标或未提供充分原始数据且索取无果,只有摘要而无全文;⑤综述和病例报告等类型。
1.2 检索策略
计 算 机 检 索PubMed、MEDLINE、Embase、The Cochrane Library、中国知网和万方数据库,收集相关文献。检索时限均从建库至2020年12月31日。英文检索词:“central precocious puberty”“early and fast puberty”“gonadotropin-releasing hor‐mone”“final adult height”。中文检索词:“中枢性性早熟”“快速进展型青春期”“促性腺激素释放激素类似物”“终身高”。检索策略英文以PubMed为例:用“(central precocious puberty)OR(early and fast puberty)OR CPP OR EFP”AND“(GnRH analogues)OR GnRHa OR GnRH-a OR(gonadotropin-releasing hormone analogue)OR(gonadotropin-releasing hormone analogs)”AND“height OR(final adult height)OR FAH”进行检索;中文以中国知网为例:用“GnRHa OR促性腺激素释放激素”AND“中枢性性早熟OR快速进展型早发育”AND“终身高OR成年身高”进行检索。
1.3 资料提取及文献质量评价
1.3.1 资料提取 参考Cochrane协作网推荐的方法编制资料提取表,由2名研究者独立提取资料,交叉核对,有不一致观点通过讨论进行解决。提取的资料包括:(1)文献的基本特征,包括文题、年份、出处、研究者姓名等;(2)纳入文献研究对象的基本特征、干预措施和结局指标。
1.3.2 文献质量评价 由采用Cochrane系统评价员手册5.1.0版[15]提供的标准进行评价,若≤2条评估标准为高风险,则该研究发生偏倚风险小、质量高;若>2条评估标准为高风险,则该研究发生偏倚的风险高、质量低。
1.4 统计学分析
采用Stata 12.0软件进行Meta分析。连续变量用加权均数差(weighted mean difference,WMD)及其95%可信区间(confidence interval,CI)表示临床疗效指标。判断异质性采用Q检验,I2≤50%时,表示各研究间无显著异质性,采用固定效应模型分析;I2≥50%认为研究间存在异质性,采用随机效应模型[16]。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果和纳入文献的基本情况
按制定的检索策略,共检出GnRHa治疗CPP/EFP的相关文献共455篇,其中英文360篇,中文95篇,经阅读标题、摘要或全文,最后筛选出符合纳入标准的有10篇,全为英文文献[5-14]。文献筛选流程见图1,纳入10篇文献相关信息见表1。所有文献均以使用GnRHa治疗为试验组,未治疗为对照组;10项研究共纳入了720例参与者,其中试验组475例,对照组245例,平均研究样本量72例(范围22~142例),其中结局指标包括:①FAH[5-14];②FAHSDS[5,8,11,14];③FAHPAH[10-12];④FAH-TH[8-11]。见表1。

图1 文献筛选流程和结果
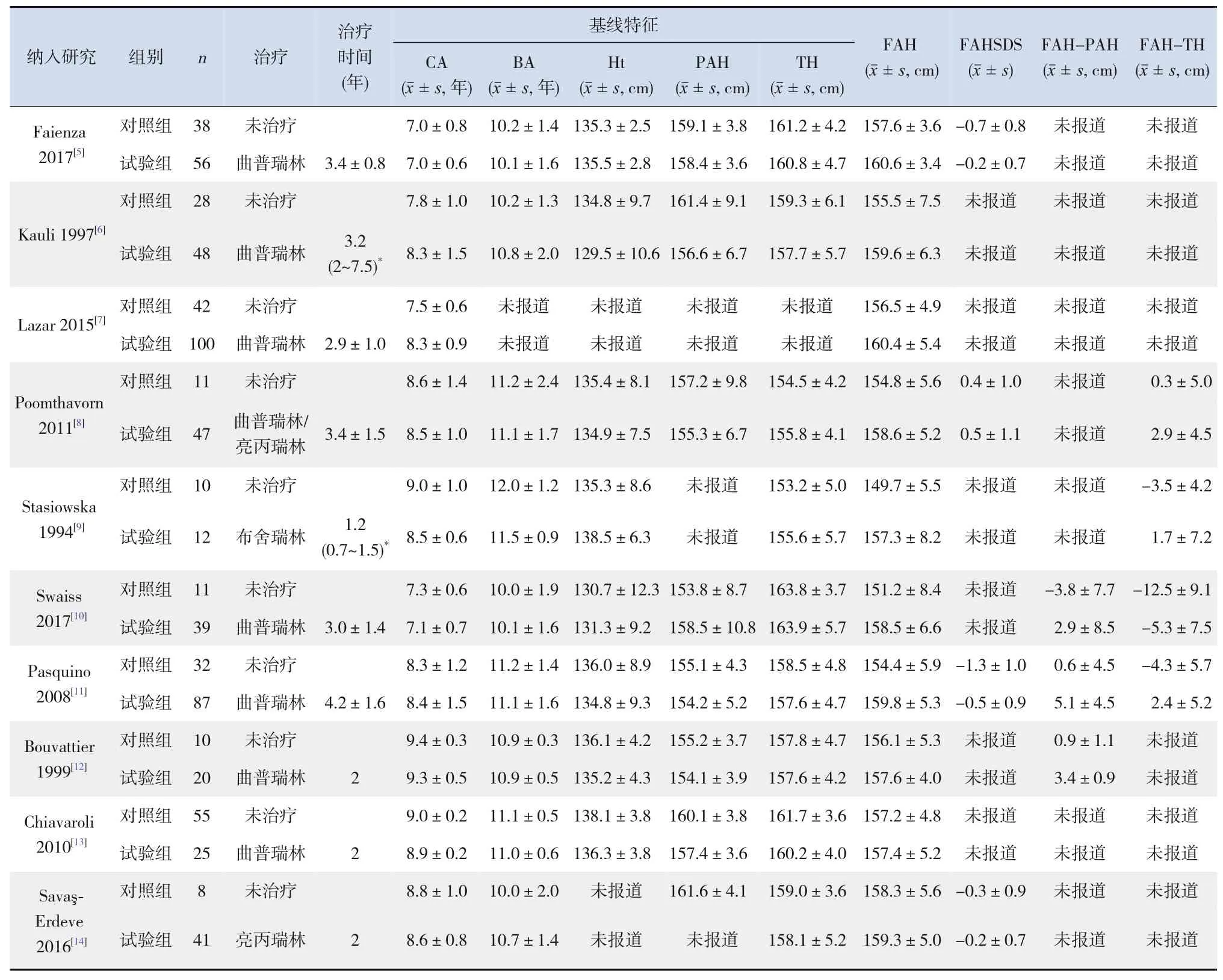
表1 纳入10篇文献的基本信息
2.2 文献质量评价
使用Review Manager 5.4软件中的评估工具评估所纳入的每个研究的偏倚风险,仅1篇文献为随机对照研究[12],其余均为病例对照研究[5-11,13-14],其中高质量文献4篇[10-13],低质量文献6篇[5-9,14]。见图2。

图2 研究偏倚风险评估 上图为每项纳入文献的质量评估结果;下图为每种偏倚风险评估结果的百分比。
2.3 Meta分析结果
2.3.1 FAH 10个研究[5-14]均涉及了FAH,共纳入720例患儿,其中试验组475例,对照组245例。各研究间异质性不大(I2=46.2%,P=0.053),故采用固定效应模型进行Meta分析。结果显示GnRHa能改善CPP/EFP患儿FAH,组间差异有统计学意义(WMD=3.30,95%CI:2.49~4.12,P<0.01)。为进一步降低异质性,我们按治疗时间进行亚组分析,结果显示治疗时间>2年组(WMD=3.88,95%CI:2.95~4.81,P<0.001)CPP/EFP患 儿 经GnRHa治疗后能改善FAH,治疗时间≤2年组(WMD=1.29,95%CI:-0.44~3.02,P=0.145)CPP/EFP患儿FAH无改善,提示治疗时间>2年组疗效优于治疗时间≤2年组。见图3。
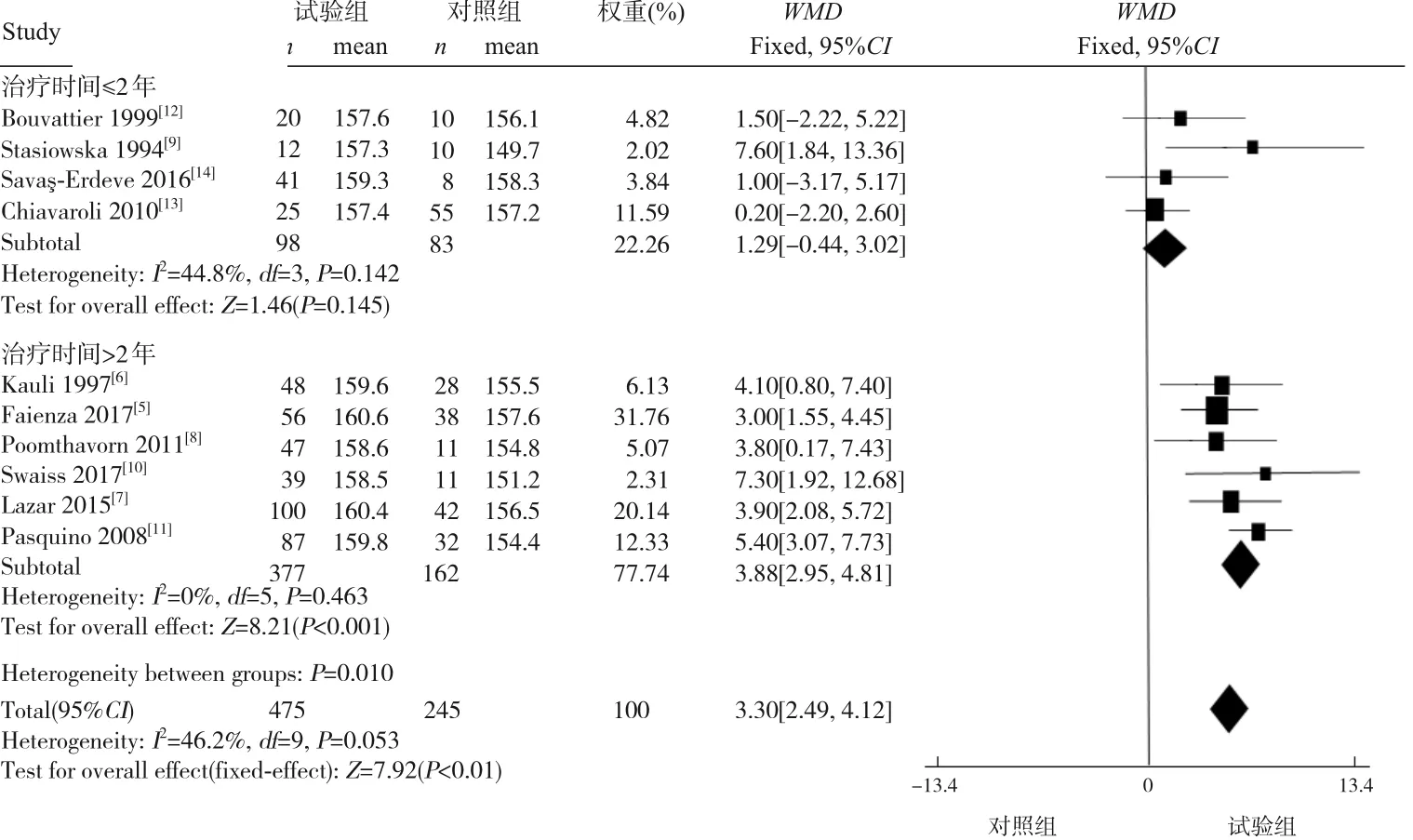
图3 GnRHa治疗CPP/EFP患儿FAH改变的森林图
2.3.2 FAHSDS 有4个研究[5,8,11,14]涉及该疗效指标,共纳入320例患儿,其中试验组231例,对照组89例。各研究间异质性不大(I2=33.1%,P=0.214),故采用固定效应模型进行Meta分析。结果显示GnRHa能改善患儿FAHSDS,组间差异有统计学意义(WMD=0.51,95%CI:0.29~0.73,P<0.01)。见图4。
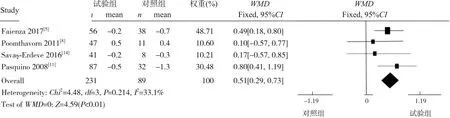
图4 GnRHa治疗CPP/EFP患儿FAHSDS改变的森林图
2.3.3 FAH-PAH 有3个研究[10-12]涉及该疗效指标,共纳入199例患儿,其中试验组146例,对照组53例。各研究间有异质性(I2=66.3%,P=0.051),故采用随机效应模型进行Meta分析。结果显示试验组终身高获益高于对照组,差异有统计学意义(WMD=2.89,95%CI:2.17~3.60,P<0.01)。见图5。
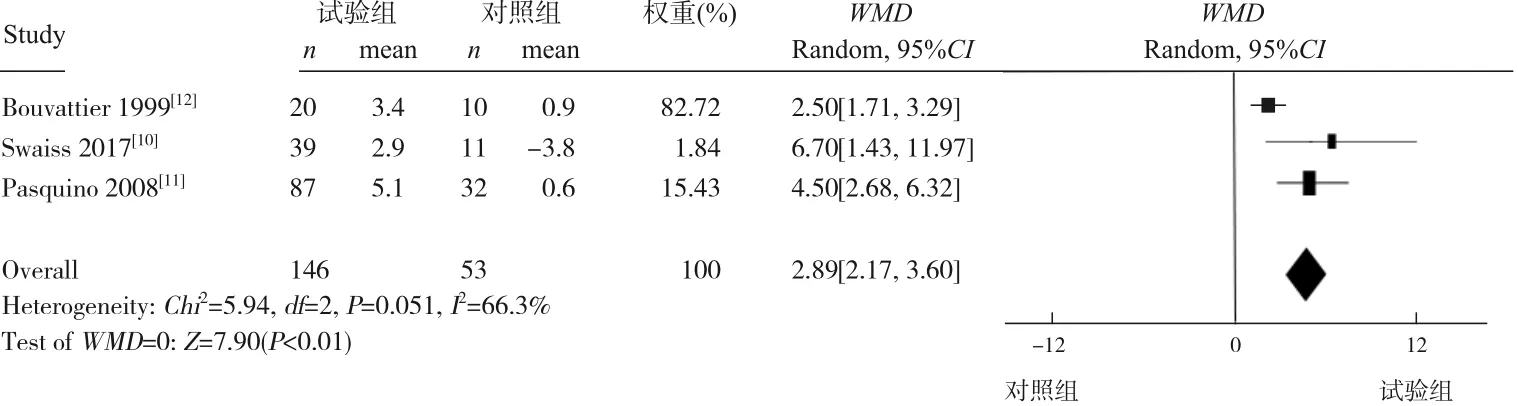
图5 GnRHa治疗CPP/EFP患儿FAH-PAH改变的森林图
2.3.4 FAH-TH 有4个研究[8-11]涉及该疗效指标,共纳入249例患儿,其中试验组185例,对照组64例。各研究间有异质性(I2=82.8%,P=0.001),故采用随机效应模型进行Meta分析。结果显示GnRHa不能改善FAH-TH,组间差异无统计学 意 义(WMD=4.26,95%CI:-0.23~8.74,P=0.063)。见图6。
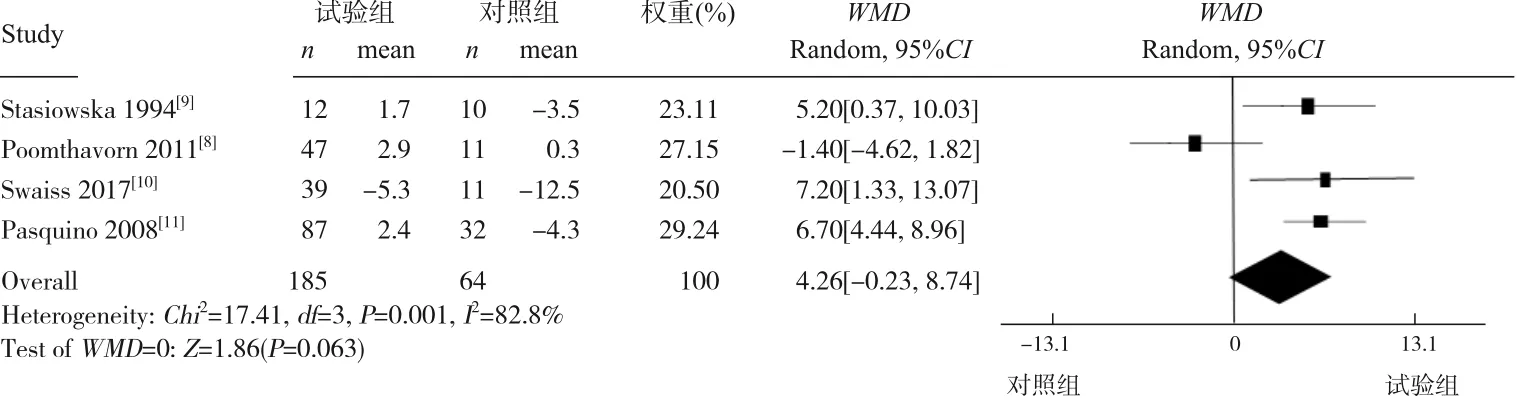
图6 GnRHa治疗CPP/EFP患儿FAH-TH改变的森林图
2.4 发表偏倚
对GnRHa治疗CPP/EFP患儿的疗效(FAH改善)行发表偏倚检验,Begg检验Z=0.18,P=0.858;Egger检 验t=0.60,P=0.567,且95%CI:-1.872~3.178。结果均提示无明显发表偏倚,见图7。

图7 GnRHa治疗CPP/EFP患儿FAH改变发表偏倚检验 Begg法和Egger法检验均提示无明显发表偏倚。
2.5 敏感性分析
剔除任一研究后,比较Meta分析合并值WMD及其95%CI变化不大,未改变Meta分析结果的方向,说明研究合并结果稳定性较好,结果基本可靠,见图8。

图8 GnRHa治疗CPP/EFP患儿FAH改变敏感性分析 合并值WMD及其95%CI变化不大,说明纳入Meta分析的各研究合并结果基本稳定。
2.6 不良反应
所有的研究均无严重不良反应报道。
3 讨论
随着环境风险因素暴露增加,CPP/EFP的发病率逐年升高[17],其治疗也愈发受到儿科医生的重视。CPP/EFP致FAH受损源于雌激素提前暴露导致骨龄加速,损害了患儿的生长潜能,使患儿的生长潜能和时间窗缩短。改善FAH是GnRHa治疗CPP/EFP的主要目标。GnRHa治疗实现患儿FAH改善的机制是经GnRH受体调节而抑制垂体促性腺激素的释放,进而抑制性激素的分泌,延缓骨龄进展,从而保留骨生长板的生长潜能,实现身高追赶。这一过程并非靠生长加速而是延长可继续生长的时间。
关于GnRHa改善CPP/EFP患儿FAH的有效性,国外共识认为GnRHa治疗对<6岁CPP女童身高获益明显,对6~8岁CPP女童身高获益不详[18-19]。已有发表的系统综述评估GnRHa治疗儿童CPP的长期疗效和安全性。该研究从3 515篇文献中筛选出98项研究,涉及105篇参考文献,共收集了5 475名CPP患儿(98.5%为女孩)的数据,这些数据包括接受GnRHa(任何给药方案)或GnRHa联合生长激素长期治疗(≥6个月)的CPP患儿,分析结果表明GnRHa治疗改善女孩的FAH超过2.32 cm,而且接受GnRHa治疗的女孩平均FAH高于她们的TH或与之接近[20]。该系统综述仅评估了CPP患儿,且纳入的研究包括单一观察无对照组的研究,没有对纳入的研究进行偏倚风险评估。另一系统综述[21]评估了GnRHa在改善7~10岁青春期启动的女孩FAH方面的有效性,纳入6项研究,共332名女生,平均治疗时间为2年,分析结果显示组间差异无统计学意义(WMD=0.50,P=0.42),与本研究结果相反,但他们纳入病例数少,平均治疗时间较短,且未按治疗时间进行亚组分析。
本研究对10篇文献进行Meta分析,包括720名受试者,其中试验组475例,对照组245例,探讨GnRHa改善CPP/EFP患儿FAH的疗效。Meta分析结果显示GnRHa能改善CPP/EFP患儿FAH。按治疗时间进行亚组分析,结果显示治疗时间>2年组经GnRHa治疗后能改善患儿FAH,治疗时间≤2年组经GnRHa治疗后患儿FAH无改善,说明治疗时间>2年组疗效优于治疗时间≤2年组。GnRHa能改善患儿FAHSDS,且使患儿终身高获益;但不能改善FAH-TH。
一项评价GnRHa联用重组人生长激素治疗CPP/EFP患儿并改善其FAH的多中心回顾性研究[22],涉及CPP/EFP患者448名,年龄均在8岁以上,并对所有患者进行随访,直至达到FAH,结果显示在身高获益(FAH-PAH)方面,联合治疗组[(9.51±0.53)cm]、单用GnRHa治疗组[(8.07±0.37)cm]、对照组[(6.44±0.91)cm]间差异有统计学意义,联合治疗组身高获益更明显,这与一项Meta分析结果一致[23]。
青春期早熟因为第二性征过早发育及性成熟,会带来一定的心理和社会问题,会困扰父母,甚至影响治疗[19];证据表明,GnRHa治疗不仅能改善患儿认知功能,也会减少一些儿童心理和社会问题[24-25];同时研究证明GnRHa治疗不增加超重/肥胖的风险、不增加多囊卵巢综合征发生率,且GnRHa治疗未增加糖尿病、高脂血症等代谢性疾病的风险[20]。
本研究的发表偏倚结果显示,所纳入文献存在发表偏倚的可能性小;同时考虑到治疗时间、试验类型、最大样本量可能会对结果产生影响,进行了敏感度分析,结果均较为稳定,表明纳入的文献中FAH指标合并效应结果较为可靠;然而纳入FAH-TH指标合并效应存在一定的异质性,可能与每次试验纳入标准不一致有关。本研究的不足之处和局限性:(1)随机对照研究仅1篇,其余均非随机对照试验,通常对照组由拒绝干预的患者组成;(2)文献质量差异较大,文献总体质量较低,总样本量较小;(3)使用的GnRHa种类、剂量差异较大,疗程不一。
综上所述,GnRHa治疗能改善CPP/EFP患儿FAH,尤其治疗时间>2年的患儿身高获益更明显,对于预测FAH严重受损者建议联用重组人生长激素;此外,GnRHa治疗过程中未见明显严重不良反应。但结论的可靠性,尚需更多的大样本、高质量的前瞻性随机对照研究进一步验证。

