莲蓬壳活性炭对水中苯胺的吸附性能
杨晓冉,李凌凌,王 逸,高连芬
(1.安徽省生态环境监测中心,安徽 合肥 230071;2.武汉科技大学 化学与化工学院,湖北 武汉 430081)
1 引言
苯胺是一级芳香胺的典型代表物质,作为重要的有机化工原料、精细化工中间体和制造业中不可或缺的溶剂[1],广泛地应用于农药、医药、军工、染料、香料和橡胶硫化等行业,有着无法替代的关键作用[2]。苯胺具有长期残留性、生物蓄积性、致癌性等特点[3],一旦进入水体和土壤中,将对生态环境、人畜身心健康造成很大的影响[4]。因此,被美国EPA列为优先控制的污染物之一,也被我国列入14类环境优先控制污染物黑名单[3, 5]。
活性炭具有发达的孔隙结构,广泛地应用于水净化处理。且其化学性质稳定,无臭无味,亦可用于食品、医药和化工等行业的脱色工艺中,比普通吸附剂的吸附效果更好。本实验采用废弃的莲蓬壳制作的活性炭,研究其对水中苯胺有良好的吸附能力。
2 实验部分
2.1 试剂和仪器
主要试剂和原料:莲蓬壳活性炭来自实验室自制。苯胺标准品,环保部标准样品研究所;硫酸氢钾、氨基磺酸铵、盐酸萘乙二胺,均为分析纯,国药集团。
主要仪器:MicrometicsASAP-2020比表面积测定仪,上海麦克仪器;UV2700可见-紫外分光光度计,日本岛津公司。
2.2 实验方法
2.2.1 莲蓬壳活性炭孔隙结构分析
采用全自动比表面积及孔隙分析仪测定莲蓬壳活性炭的比表面积和孔隙结构。
2.2.2 莲蓬壳活性炭对苯胺的吸附实验
参照GB11889-89对苯胺浓度进行测定,使用紫外分光光度计于波长221 nm处测定苯胺溶液的吸光值,根据公式(1)计算苯胺的平衡吸附量。
Qe=(C0-Ce)×V/m
(1)
式(1)中:C0为吸附质的初始浓度,mg/L;Ce为吸附后吸附质的浓度,mg/L;V为溶液的体积,L;m为吸附剂的用量,g。
3 结果与讨论
3.1 莲蓬壳活性炭的表征
吸附剂的吸附性能主要由孔容量、比表面积决定。对莲蓬壳活性炭孔隙结构进行测定,结果显示其BET比表面积为663 m2/g,大于工业用水处理活性炭一级标准(500 m2/g)[6]。总孔容积为0.402 cm3/g,其中孔径在2.0nm以下的微孔容积为0.224 cm3/g,占总孔容积的56%,剩余的孔容积由中孔提供,按照国际理论与应用化学协会(IUPAC)的分类标准, 莲蓬壳活性炭属于微孔炭[7]。
3.2 初始pH值对苯胺去除率的影响
配制5份初始浓度为20 mg/L的苯胺溶液,于每升溶液中投加1 g莲蓬壳活性炭,分别调节pH值为2.0、4.0、6.0、8.0、10.0,振荡反应120 min,过滤后测定水溶液中剩余的苯胺浓度,并计算苯胺的去除率。如图1所示,莲蓬壳活性炭对苯胺的去除率随着溶液pH值的增加而增加,当pH值为8.0时,去除率达到最高点。因此,碱性条件下更有利于活性炭对苯胺的吸收。原因是由于溶液pH值影响了苯胺在水溶液中的存在形式。苯胺在水溶液中的解离常数为4.64。当溶液pH值较低时莲蓬壳活性炭和苯胺的表面均携带正电荷,两者之间的静电排斥较强导致吸附效率较低。当pH值大于苯胺的解离常数,苯胺的表面逐步呈现电中性状态,与莲蓬壳活性炭之间的静电排斥作用减少,吸附效率大大提高[8]。在pH值为8.0时吸附容量达到最大并保持稳定。因此,本实验选择8.0为最佳pH值。
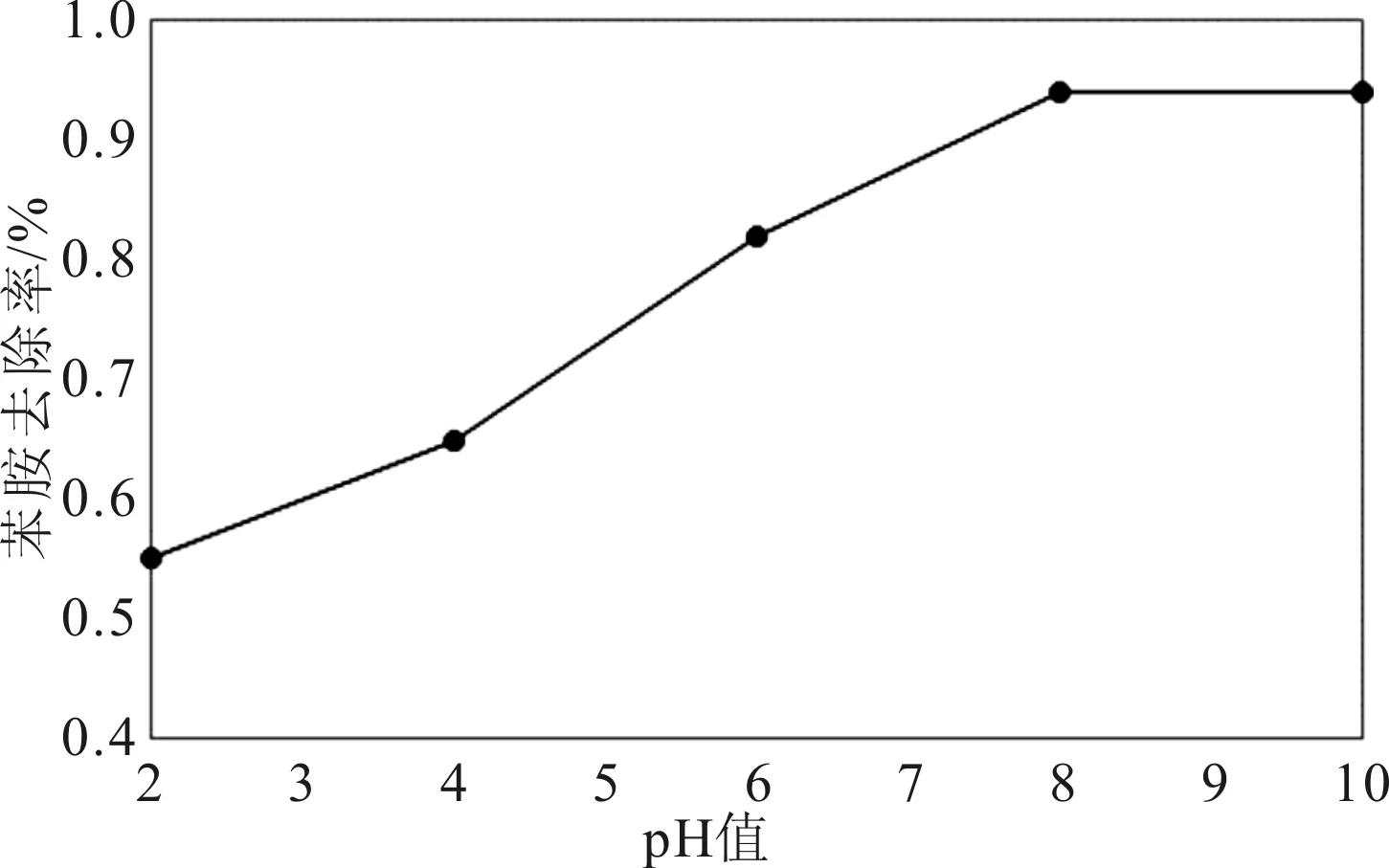
图1 pH值对莲蓬壳活性炭吸附苯胺的影响
3.3 初始浓度对莲蓬壳活性炭吸附苯胺的影响及其等温吸附线
配制5份初始浓度分别为5、10、20、30、40 mg/L的苯胺溶液,每升溶液中投加1 g莲蓬壳活性炭,调节pH值为8.0,在293K、303K、313K 3个不同温度条件下振荡反应180 min,过滤后测定水溶液中剩余的苯胺浓度,并计算吸附反应的热力学参数。
等温吸附线描述的是体系达到平衡时吸附质在吸附剂和溶液中浓度的关系。由图2可见,随着苯胺溶液初始浓度的增加以及反应温度的升高,平衡吸附量Qe显著增大。当苯胺初始浓度达到30 mg/L以上时,平衡吸附量Qe的增加值变缓。反应温度为313K时的最大吸附量为22.2 mg/g。这主要是由于随着苯胺初始浓度的增加推动了其从液相中扩散莲蓬壳活性炭的表面;温度的升高加快了苯胺在液相中的扩散速度,从而导致平衡吸附量增加,因此该吸附过程为吸热反应。

图2 苯胺溶液初始浓度对吸附性能的影响
采用Langmuir和Freundlich两种等温吸附方程对实验数据进行拟合。方程表达式如下:

(2)

(3)
式(2)、(3)中:Qe为平衡吸附量,mg/g;Qm为使用Langmuir方程计算得出的理论饱和吸附量,mg/g;KL为Langmuir方程常量,L/mg;b为吸附平衡常数;KF、n为Freundlich方程常数,其中当n>1时,表示吸附过程属于优先吸附。
拟合后的相关参数如表1所示。Langmuir等温吸附方程计算得出的理论饱和吸附量Qm与实验中得到的实际平衡吸附量比较接近,且相关系数R2大于0.99,优于Freundlich等温吸附方程拟合的相关系数。因此,Langmuir等温吸附模型能更好地描述苯胺浓度在5~40 mg/L范围内时莲蓬壳活性炭对苯胺的吸附行为。这说明莲蓬壳活性炭表面的吸附位点分布较均匀,与苯胺之间形成了单分子层吸附。而Freundlich等温吸附方程拟合的结果n>1,说明苯胺在莲蓬壳活性炭上的吸附属于优先吸附[9,10]。

表1 等温吸附方程拟合参数
3.4 吸附时间对莲蓬壳活性炭吸附苯胺的影响
配制初始浓度分别为15 mg/L和30 mg/L的苯胺溶液,每升溶液中投加莲蓬壳活性炭1 g,调节pH值为8.0,在313K温度下振荡反应,每隔一定时间取样过滤后分析苯胺的浓度。
如图3所示,在吸附过程的前30 min,吸附量随时间快速上升,30 min后吸附量增长缓慢并逐渐接近平衡。主要原因是吸附初期苯胺浓度较高,并且莲蓬壳活性炭内部的孔隙率也较高,溶质的浓度差会生成较高的传质推动力,有利于吸附。而随着莲蓬壳活性炭内部的孔隙被占据,吸附速率减慢并逐渐达到了饱和状态[11],在180 min左右接近平衡。另外,苯胺的初始浓度越高,吸附达到平衡时活性炭的单位吸附量越大。
采用准一级和准二级两种动力学模型拟合活性炭吸附苯胺的动力学过程。
准一级动力学模型方程如下式:
In(Qe-Qt)=InQe-K1t
(4)

(5)
式(4)、(5)中,Qt为某时刻活性炭单位质量吸附量,mg/g;t为吸附时间,min;K1为准一级吸附速率常数,min-1;K2为准二级吸附速率常数,g/(mg·min)。
拟合后的参数见表2。当苯胺初始浓度为15 mg/L和30 mg/L时,准二级动力学方程对初始浓度为15 mg/L和30 mg/L吸附体系计算得出的理论平衡吸附量(Qe,cal)分别为12.56 mg/g和21.98 mg/g,与实验值(Qe,exp)12.10 mg/g和21.44 mg/g很接近,相关系数R2大于0.99,优于准一级动力学方程的相关系数。这主要是由于,准一级动力学方程是描述吸附速率与吸附剂表面未被吸附的量成比例,是对吸附初始阶段动力学进行的描述,局限性较大[12]。而准二级速率方程是建立在化学反应或通过电子共享得失的化学吸附基础上,包含了吸附的所有过程,更真实全面地反映吸附的动力学机制[13, 14]。此外,对于需要较长的时间才能达到体系平衡的吸附反应体系,准二级动力学方程的优势在于无需等到反应平衡,即可通过方程计算出与实验值接近的平衡吸附量,可以更好地描述吸附反应的整个过程。
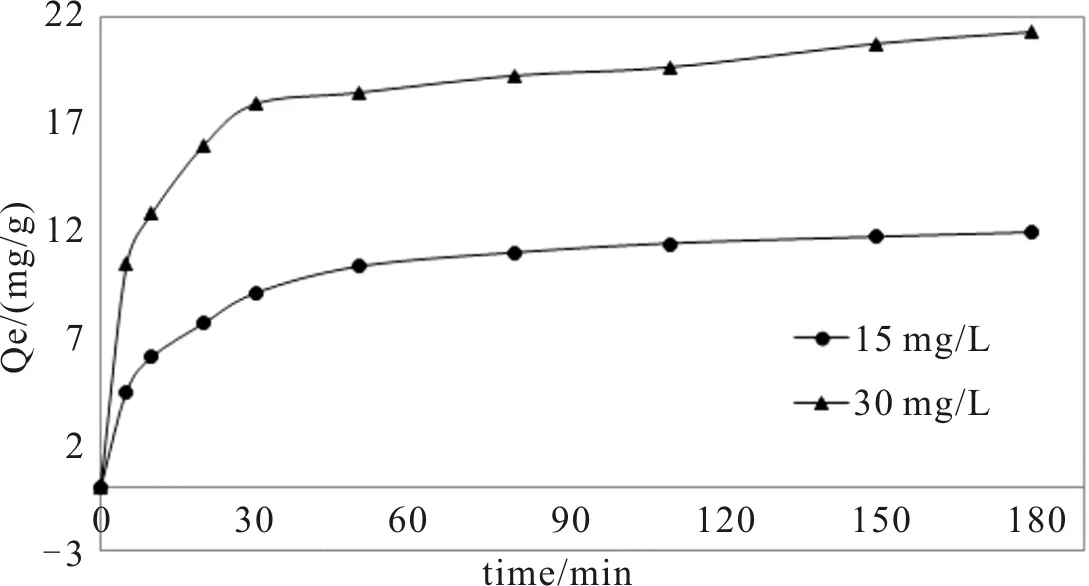
图3 吸附动力学实验
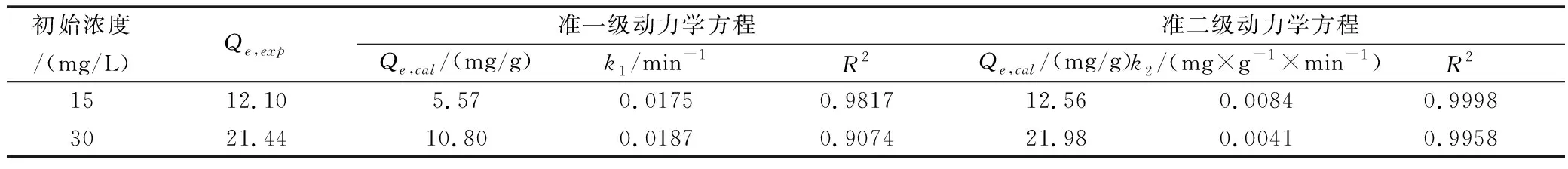
表2 动力学方程拟合参数
3.5 吸附机理
苯胺分子从液相中被吸附到固相中的过程可以分为以下步骤,活性炭表面液膜的膜扩散、苯胺分子向活性炭内表面的扩散、活性炭的表面吸附。其中过程最慢的阶段为吸附反应的控速步骤[15]。一般而言,表面吸附反应是快速步骤,因此吸附反应的总速率由膜扩散、内扩散或由两者共同控制[16]。
利用Weber和Morris颗粒内扩散模型对实验数据进行分析[10],计算公式如下:
Qt=Kpt0.5+C
(6)
式(6)中:Kp为颗粒扩散速率参数,μg/(g·min0.5);截距表示边界层效应的程度。
以莲蓬壳活性炭在某时刻的吸附量Q对t0.5作图,从图4可以看出,初始浓度为15和30 mg/L的苯胺溶液,吸附反应的平均速率参数Kp分别为5.67和11.14 μg/(g·t0.5),Kp随着苯胺初始浓度增加而增大。这是因为较高的初始浓度,可以提供更大的推动力[10],加快了吸附反应的速度。此外,每个浓度的反应曲线,Qt对t0.5拟合后的图形都呈现两个线性部分,反应开始的前30 min拟合的直线基本通过原点,说明控速因素为颗粒内扩散;30 min以后直线不通过原点且有较大的截距,说明反应由膜扩散和颗粒内扩散两个因素共同控制[7,17,18]。
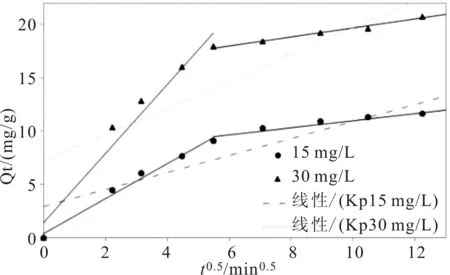
图4 不同初始苯胺浓度的Weber-Morris 曲线
4 结论
(1)莲蓬壳活性炭与苯胺溶液的吸附反应中,溶液的pH值对吸附的影响很大,当pH值为8.0时苯胺的去除率最大。
(2)莲蓬壳活性炭对苯胺的平衡吸附量与苯胺的初始浓度和反应体系的温度呈正相关性。在313K时,最大吸附量达22.4 mg/g。
(3)当苯胺浓度在5~40 mg/L范围内时,吸附平衡参数符合Langmuir等温吸附模型。莲蓬壳活性炭对苯胺的吸附动力学行为符合准二级动力学方程。
(4)Weber和Morris颗粒内扩散模型研究莲蓬壳活性炭对苯胺的吸附机理,前30 min由颗粒内扩散控制,后期由颗粒内扩散控制与膜扩散共同控制。颗粒扩散速率随苯胺初始浓度增加而增大。

