柴胡疏肝散煎剂治疗功能性腹痛综合征患者的近期随访研究
赵彦
(河南省三门峡市陕州区疾病预防控制中心传染科 三门峡 472000)
功能性腹痛综合征(Functional Abdominal Pain Syndrome,FAPS)是指病程≥6个月的持续或频繁发作的下腹部疼痛,其病理机制尚未完全明确,相关研究认为,内脏敏感性升高在其发生、发展中起着重要作用[1~3]。而P物质(SP)、降钙素基因相关肽(CGRP)、5-羟色胺(5-HT)作为疼痛介质,可能参与内脏敏感性升高进程。目前临床针对FAPS患者主要采用抗抑郁药、内脏感觉调节剂、抗惊厥药等西医疗法,但部分患者病情易反复发作。近年来,中医通过整体理念、多靶点施治在FAPS治疗中得到临床广泛关注,认为FAPS归属于“腹痛”范畴,情志不舒、肝失调达、气机阻滞、不通则痛是其主要病机,治疗宜疏肝解郁、理气止痛。柴胡疏肝散煎剂具有行气解郁、调肝止痛之效,但关于其对FAPS患者疼痛相关物质的影响有待进一步论证。基于此,本研究尝试探讨柴胡疏肝散煎剂口服治疗FAPS效果及对疼痛相关物质的影响。现报道如下:
1 资料与方法
1.1 一般资料 选取2019年7月~2020年9月我院FAPS患者97例,采用奇偶分组法分为西医组(48例)与联合组(49例)。联合组女23例,男26例;年龄25~59岁,平均(37.65±1.83)岁;病程7~35个月,平均(16.72±3.05)个月。西医组女19例,男29例;年龄28~57岁,平均(36.69±2.92)岁;病程8~33个月,平均(17.15±2.44)个月。两组年龄、性别、病程等基线资料均衡可比(P>0.05)。
1.2 诊断标准 (1)西医诊断标准:持续或近乎持续腹痛;疼痛与进食、排便或月经等生理行为无关;部分日常生活能力丧失;疼痛未伪装;排除其他可引起腹痛的功能性胃肠病。(2)中医诊断标准属肝郁气滞型,主症:腹痛腹胀累及两胁,痛无定处,痛引少腹;次症:食欲不振,时有嗳气,失眠多梦;舌淡红,苔白,脉弦。
1.3 选取标准(1)纳入标准:符合上述西医FAPS诊断标准及中医证型诊断标准;病程≥6个月;患者均知情同意。(2)排除标准:近28 d内有抗抑郁药、质子泵抑制剂等药物服用史者;处于妊娠期、哺乳期等特殊时期者;合并肝肾等其他重要脏器功能严重障碍者;严重失聪、言语功能障碍或精神紊乱者。
1.4 治疗方法 西医组实施常规西医治疗,口服氟哌噻吨美利曲辛胶囊(国药准字H20150043),1粒/次,早晨及中午各1粒,注意治疗期间忌食辛辣生冷等刺激类食物。联合组在西医组基础上加用柴胡疏肝散煎剂,组方:柴胡10 g,香附10 g,白芍15 g,枳壳10 g,陈皮6 g,紫苏梗10 g,川芎10 g,郁金10 g,甘草9 g。水煎取汁400 ml,分早晚各服用1次。两组均连续治疗28 d。
1.5 观察指标(1)治疗效果。(2)中医证候积分、疼痛程度。治疗前、治疗28 d后主症(腹痛、两肋胀痛)按照无症状、症状不明显、症状明显、症状严重分别计为0、3、6、9分;次症(食欲不振、嗳气、失眠多梦)按照无症状、症状不明显、症状明显、症状严重分别计为0、1、2、3分。疼痛程度采用视觉模拟评分法(VAS)评分进行测评,总分范围0~10分,分值越高,疼痛程度越剧烈。(3)疼痛相关物质,分别于治疗前、治疗28 d后空腹取外周静脉血5 ml,常规离心处理(1 000×g离心10 min,离心半径6 cm),取上清液,-20℃低温保存待检。按照上海恒远生物科技有限公司提供的酶联免疫吸附试验试剂盒说明书操作流程测定血清SP、CGRP、5-HT水平。(4)治疗结束后随访1个月统计复发率,复发标准:痊愈、显著进步、缓解患者再次出现FAPS。
1.6疗效判定标准 主症及次症基本消退,中医证候积分下降95.0%及以上为痊愈;主症及次症显著缓解,中医证候积分下降70.0%及以上但不足95.0%为显著进步;主症及次症有所控制,中医证候积分下降30.0%及以上但不足70.0%为缓解;治疗28 d后,主症及次症均未出现明显缓解,或病情恶化,中医证候积分下降30.0%以下为无效。将痊愈、显著进步、缓解纳入总有效。
1.7 统计学方法 通过统计学软件SPSS22.0处理数据,计量资料采取Bartlett方差齐性检验与夏皮罗-威尔克正态性检验,均确认具备方差齐性且近似服从正态分布,以(±s)描述,组内比较采用配对t检验,组间比较采用独立样本t检验;计数资料用%表示,采用χ2检验。P<0.05示差异有统计学意义。
2 结果
2.1 两组治疗效果比较 治疗28 d后,联合组11例痊愈,19例显著进步,15例缓解,4例无效;西医组2例痊愈,10例显著进步,24例缓解,12例无效。联合组总有效率91.84%(45/49)高于西医组75.00%(36/48)(χ2=4.990,P=0.026)。
2.2 两组中医证候积分、VAS评分比较 配对t检验,两组治疗28 d后中医证候积分、VAS评分较治疗前下降(P<0.05);独立样本t检验,两组治疗前中医证候积分、VAS评分比较无显著差异(P>0.05);联合组治疗28 d后中医证候积分、VAS评分均较西医组低(P<0.05)。见表1。
表1 两组中医证候积分、VAS评分比较(分,±s)
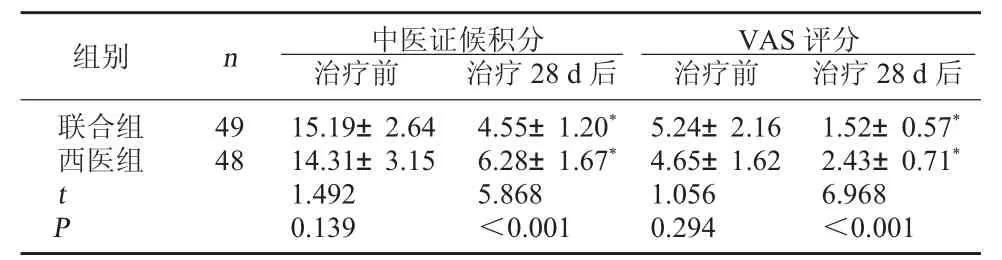
表1 两组中医证候积分、VAS评分比较(分,±s)
注:与同组治疗前比较,*P<0.05。
VAS评分治疗前 治疗28 d后联合组西医组组别 n 中医证候积分治疗前 治疗28 d后49 48 tP 15.19±2.64 14.31±3.15 1.492 0.139 4.55±1.20*6.28±1.67*5.868<0.001 5.24±2.16 4.65±1.62 1.056 0.294 1.52±0.57*2.43±0.71*6.968<0.001
2.3 两组疼痛相关物质比较 配对t检验,两组治疗28 d后血清SP、CGRP、5-HT水平较治疗前下降(P<0.05);独立样本t检验,两组治疗前血清SP、CGRP、5-HT水平比较无显著差异(P>0.05);联合组治疗28 d后血清SP、CGRP、5-HT水平均较西医组低(P<0.05)。见表2。
表2 两组疼痛相关物质比较(±s)
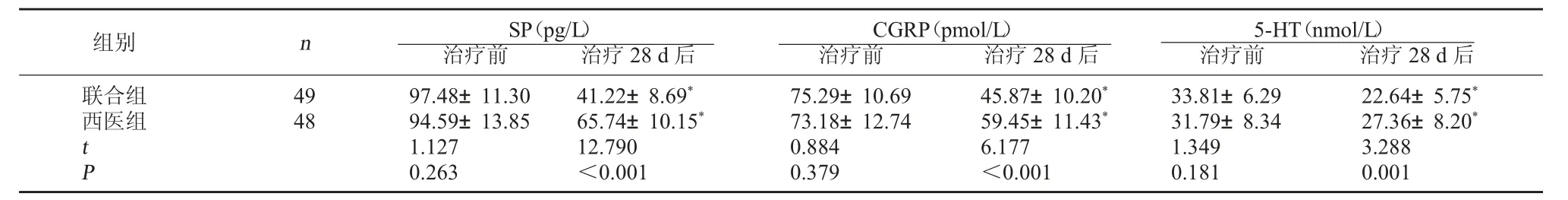
表2 两组疼痛相关物质比较(±s)
注:与同组治疗前比较,*P<0.05。
5-HT(nmol/L)治疗前 治疗28 d后联合组西医组组别 n SP(pg/L)治疗前 治疗28 d后CGRP(pmol/L)治疗前 治疗28 d后49 48 tP 97.48±11.30 94.59±13.85 1.127 0.263 41.22±8.69*65.74±10.15*12.790<0.001 75.29±10.69 73.18±12.74 0.884 0.379 45.87±10.20*59.45±11.43*6.177<0.001 33.81±6.29 31.79±8.34 1.349 0.181 22.64±5.75*27.36±8.20*3.288 0.001
2.4 两组复发情况比较 随访1个月,联合组复发2例,西医组复发3例。联合组复发率4.44%(2/45)与西医组8.33%(3/36)比较无显著差异(χ2=0.067,P=0.796)。
3 讨论
中医认为,FAPS主要病理机制在于情志不遂,木失调达,则肝郁血滞,经气不利,不通则痛,导致腹痛时作,攻窜不定,嗳气频作,纳寐欠安,甚则痛及少腹。故治疗重点在于疏肝解郁、理气调中。柴胡疏肝散煎剂中柴胡为君药,味苦、辛,性微寒,归肝、胆经,可解表退热,疏肝解郁,升举阳气。香附为臣药,味辛、微味苦、微甘,性平,归肝、脾、三焦经,能疏肝解郁,调经止痛,理气调中。白芍、枳壳、陈皮共为佐药,其中白芍味苦、酸,性微寒,归肝、脾经,可柔肝止痛、平抑肝阳;枳壳味苦、辛、酸,性微寒,归脾、胃经,可行气宽中、消胀除满;陈皮味辛、苦,性温,归脾、肺经,可理气健脾,燥湿化痰。甘草为使药,性平,味甘,入心经、脾经、肺经、胃经,可调和诸药。诸药共行疏肝解郁、行气止痛之功。王安琪等[4]研究显示,在黛力新治疗的同时配合加味柴胡疏肝散,有助于缓解FAPS患者腹痛症状,且临床总有效率为86.7%。本研究结果表明,柴胡疏肝散煎剂口服有助于减轻FAPS患者腹痛程度,缓解临床症状,总有效率为91.84%,考虑机制可能在于,柴胡疏肝散煎剂中富含柴胡、川芎、枳壳、紫苏梗等中药的有效成分,不仅可产生良好抗抑郁作用,有效调节患者脑-肠轴互动异常,还能降低胃肠平滑肌张力,进一步减弱内脏植物神经高敏感性。
另有学者指出,内源性疼痛调节系统改变可能是FAPS发生的重要因素[5]。FAPS发生时,外周及中枢神经可释放促肾上腺皮质激素释放因子,激活5-HT表达,刺激脑干蓝斑,进而增强内脏敏感性,削弱内脏疼痛阈值,引起疼痛[6]。SP作为一种信号传导分子,可连接中枢系统与免疫系统,活化血小板,促进5-HT大量释放,从而参与痛觉传导[7~8]。CGRP对内脏疼痛具有一定调控作用。本研究创新性分析FAPS患者疼痛相关物质改善情况,结果显示,联合组治疗28 d后血清SP、CGRP、5-HT水平均较西医组低,提示柴胡疏肝散煎剂口服治疗有助于改善FAPS患者疼痛相关物质水平,这可能归因于柴胡疏肝散煎剂中富含α-香附酮、白芍提取物、柴胡皂苷等化学成分,可产生良好镇静、镇痛效果。随访1个月,两组复发率比较无明显差异。进一步分析可知,柴胡疏肝散煎剂口服不会增加FAPS患者复发率,具有一定安全性。综上可知,柴胡疏肝散煎剂口服有助于增强治疗效果,调控FAPS患者疼痛相关物质水平,改善中医证候,缓解疼痛程度,且具有一定安全性。

