芎芪醒脑方对轻、中度阿尔茨海默病患者临床疗效及血清炎症因子的影响❋
杨淑荃, 范德辉, 卢桂梅, 袁智先, 苏美意, 张振宁, 林 颖, 唐 明
(1.广州中医药大学研究生院,广州 510405; 2.广东省第二中医院,广州 510095)
阿尔茨海默病(alzheimer’s disease, AD)约占老年痴呆的50%~75%,主要表现为认知功能减退、精神行为异常及生活自理能力受限[1]。1项国际研究预测,截至2050年受AD影响的人数将达1.14亿[2]。目前AD的治疗药物应用最广泛的是胆碱酯酶抑制剂,如多奈哌齐能减少乙酰胆碱分解,增强神经冲动传递,但不良反应较多,且5 mg/d的剂量只对AD早中期有效,不能阻止AD病情进展。同时AD新药研发时间长、成本高,且血脑屏障的保护作用一般药物分子难以进入颅内[3]。中药复方因安全有效、多环节、多途径的治疗特点,对于防治AD具有独特优势[4]。卢桂梅教授是第四批全国名老中医药学术经验传承工作指导老师,其辨证精准、用药灵活,自拟芎芪醒脑方用于治疗AD取得良好疗效。有研究表明,炎症反应在AD早期阶段至关重要[5]。笔者结合自身临床实践及AD病理机制,观察芎芪醒脑方对轻、中度AD患者的临床疗效及血清炎症因子的影响,现报道如下。本研究经广东省第二中医院医学伦理委员会批准并监督,粤二中医(2017)伦审第023号。
1 资料与方法
1.1 一般资料
选取广东省第二中医院2018年9月至2019年12月康复科门诊及住院部收治的70例轻、中度AD患者为研究对象。患者首次就诊时按随机数字表法将患者分为观察组36例和对照组34例。经过培训的专业人员不参与研究过程的随机分组和临床治疗,只负责病例资料的记录评估、数据分析等。观察组男21例,女15例;年龄58~79岁,平均年龄(68.37±15.20)岁;病程6个月~4年,平均病程(2.71±0.84)年;AD轻度19例,中度17例;文盲5例,小学13例,中学及以上18例;临床痴呆评定量表(clinical dementia rating, CDR)评分(1.87±0.95)分。对照组男20例,女14例;年龄56~80岁,平均年龄(67.02±16.13)岁;病程8个月~5年,平均病程(2.84±0.79)年;AD轻度18例,中度16例;文盲3例,小学12例,中学及以上19例;CDR评分(1.92±0.86)分。2组基线特征比较差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准
西医诊断标准参照2011年美国衰老研究所和阿尔茨海默病学会(NIA-AA)[6]、2018年中国医师协会神经内科医师分会认知障碍疾病专业委员会制定的《中国痴呆与认知障碍诊治指南》(简称2018指南)[7]中AD的相关标准制定。中医诊断标准(肾虚髓减、气虚血瘀型)参照2002年《中药新药临床研究指导原则》[8]制定。主症:智能减退,腰膝酸软,倦怠思卧。次症:表情呆板、思维迟钝,善惊易恐,脑转,耳鸣或有幻听,面颊潮红,小便失禁,大便自遗,舌红、少苔,脉细数。主症具备2项(智能减退必备),次症至少具备2项以上。
1.3 纳入标准
符合上述中西医诊断标准;病程≥6个月,年龄55~80岁;简易精神状态检查量表评分(mini-mental state examination, MMSE)10~26分,<17分(文盲)、20分(小学)、24分(中学及以上)[10];CDR=1.0, 2.0;日常生活能力量表(activity of daily living scale, ADL)>22分[11];Hachinski缺血指数量表≤4分;Hamilton抑郁量表≤17分;患者有能够进行测试的视力和听力;患者及家属知情同意。
1.4 排除标准
重度AD或其他理化因素诱发AD;有明确的脑血管疾病;老年精神分裂症;有严重内科疾病,如恶性肿瘤、出血性疾病;合并严重胃、十二指肠疾病影响药物吸收者;过敏体质且对本试验药物过敏或难以耐受者;依从性差,不遵守本研究相关规定;近期使用过对本研究有干扰作用的药物;无可靠陪护。
1.5 治疗方法
基础治疗:2组调控血压、血糖、血脂、同型半胱氨酸水平等对症处理。结合必要的康复措施,如记忆力、语言训练等,每次60 min,每日1次,连续6 d为1个疗程,间隔休息1 d,治疗8周。
对照组:基础治疗+多奈哌齐片口服(卫材(中国)药业有限公司,批准文号5 mg国药准字H20050978,10 mg国药准字H20070181),前4周每日5 mg,后4周每日10 mg,20∶00服用。
观察组:基础治疗+芎芪醒脑方颗粒冲服。药物组成:黄芪、丹参、党参各30 g,熟地、女贞子各20 g,川芎10 g,赤芍、地龙各15 g,僵蚕12 g,田三七、全蝎各6 g,蜈蚣2条并随症加减用药[11],中药统一采用广东一方制药有限公司出产的配方颗粒。嘱患者将配好的中药颗粒热水冲服400 ml,于9∶00和20∶00分2次服用,每日1剂,连服8周。
1.6 观察指标
①智能变化:1)MMSE,包括定向力、即刻记忆、注意力及计算力、回忆能力、语言功能等,正常、轻度、中度、重度分别为27~30、21~26、10~20、<10分[9];2)AD认知评定量表(alzheimer's disease assessment scale-cognitive subscale, ADAS-Cog),包括词语回忆、执行指令、定向力、语言表达、注意力等项目共75分,大于15.5分为异常[12]。
②日常生活能力:ADL,14项56分,完全正常、不同程度的功能下降、明显的功能障碍,依次为<16分、16~22分、>22分[10]。
③精神行为变化:神经精神症状问卷(neuropsychiatric inventory questionnaire, NPI),12个亚项,每项附3个问题,由轻到重依次为0~3分、0~2分、0~5分共120分[13]。
④血清炎症因子:采用酶联免疫吸附法检测血清肿瘤坏死因子α(TNF-α)、白细胞介素-4、6、10(IL-4、IL-6、IL-10)含量。试剂盒购于广州欣博盛生物科技有限公司,严格按照说明书操作。
⑤不良反应:治疗前后患者行血常规、尿常规、肝肾功能及心电图检查,临床医生判定患者服药后反应。
1.7 疗效标准
临床疗效评定以MMSE改善率进行疗效分级。MMSE改善率=(治疗后评分-治疗前评分)/治疗后评分×100%[14],显效、有效、无效,改善率依次为>20%、10%~20%、<10%,总有效率=显效率+有效率。
1.8 统计学方法
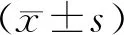
2 结果
2.1 2组临床疗效比较
表1示,2组总有效率比较差异有统计学意义(P<0.05),观察组优于对照组。

表1 2组临床疗效比较[例(%)]
2.2 2组各量表评分比较
表2示,与治疗前比较,观察组治疗4周后和治疗8周后、对照组治疗8周后的MMSE升高(P<0.05),ADAS-Cog、ADL、NPI降低(P<0.05)。与对照组比较,观察组治疗4周后和治疗8周后的MMSE升高(P<0.05)。

表2 2组各量表评分比较分)
2.3 2组血清炎症因子比较
表3示,与治疗前比较,2组治疗4周后和治疗8周后TNF-α、IL-6降低(P<0.05),IL-4、IL-10升高(P<0.05)。与对照组比较,观察组治疗4周后和治疗8周后 TNF-α、IL-6降低(P<0.05),IL-4、IL-10升高(P<0.05)。
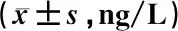
表3 2组炎症因子数比较
2.4 不良反应比较
观察组出现头晕1例,恶心1例,食欲下降1例,总不良反应率8.33%(3/36)。对照组出现头晕2例,恶心2例,乏力1例,失眠1例,食欲下降2例,总不良反应率23.53%(8/34),2组比较差异有统计学意义(P<0.05),观察组明显低于对照组。
3 讨论
2018指南[7]A级推荐AD患者选用胆碱酯酶抑制剂治疗。目前多奈哌齐片最常用,并取得较理想的疗效[15]。本研究中,5 mg/d的多奈哌齐治疗4周后,MMSE、ADAS-Cog、ADL、NPI无明显变化,而继续以10 mg/d的多奈哌齐治疗4周后,MMSE升高,ADAS-Cog、ADL、NPI降低,可能与其加量有关。其药品说明书2018年7月24日修订指出,根据多奈哌齐抑制乙酰胆碱水解的作用机制推测,随着病程进展,功能完整的胆碱神经元逐渐减少,多奈哌齐的作用可能减弱;持续24周的临床试验也显示,10 mg/d的治疗剂量(以往大多为5 mg/d)可有效改善中重度AD患者的认知功能。西医治疗AD局限于单一的病理过程,并不能阻止AD病情进展且不良反应较多。中药具有多靶点、多系统的治疗优势,开发出高效低毒的AD中药复方有较大的发展空间[16]。
AD属于中医学“痴呆”“善忘”“癫证”等范畴,大多本虚标实。肾虚为本,精髓不足,脑海空虚,清窍失养;肾气不足,血行缓慢,气虚血瘀,干扰清窍。芎芪醒脑方补气益肾、活血祛瘀。方中黄芪、党参补气以生血、益气以行血,熟地、女贞子滋肾阴、填肾精,丹参、赤芍、川芎、田三七活血祛瘀,地龙、僵蚕、全蝎、蜈蚣走窜通络。本方攻补兼施,补而不滞,补中有通。近年来AD的炎症机制备受重视[17],也有研究表明中药复方可以调节AD炎症因子数[18]。TNF-α、IL-6是常见的促炎细胞因子,IL-4、IL-10是常见的抗炎细胞因子[19]。动物实验发现,黄芪甲苷对脑缺血再灌注大鼠具有抗炎抗衰老的生物活性,可减少TNF-α、IL-6数量[20];富硒女贞子粗多糖可提高小鼠IL-4生成水平,从而增强免疫功能[21];赤芍能下调糖尿病肾病大鼠肾脏TNF-α的表达[22];川芎挥发油显著抑制脂多糖致血管认知障碍小鼠TNF-α的表达[23];丹参茎叶酚酸组分能降低溃疡性结肠炎模型小鼠IL-6数量[24]。本研究中,观察组ADAS-Cog、ADL、NPI治疗后较治疗前明显降低,且治疗4周和8周后的MMSE较对照组明显升高,表明芎芪醒脑方对轻、中度AD患者有较好的临床疗效,能改善AD患者的认知功能、日常生活自理能力及精神行为状态。与对照组比较,观察组治疗4周后和8周后的IL-4、IL-10升高,TNF-α、IL-6降低,表明芎芪醒脑方的作用机制可能与调节血清炎症因子有关。
临床上,西医往往待AD完全诊断明确后给予药物治疗,但2018指南[8]指出,AD起病隐匿、病程缓慢、进行性加重,若早期干预能体现中医治未病思想[25],能否减少AD发病率、阻止病情恶化,需要中医药研究者进一步发掘中医药预防优势。本研究只纳入轻、中度AD患者,其远期疗效如何有待完善。

