非顺应性球囊修饰技术对球囊通过性的影响
张卫锋,贾海燕,王艳飞,贾辛未,曹雪滨,朱烨然
经皮冠状动脉(冠脉)介入治疗(PCI),尤其是冠脉支架植入治疗是目前急性冠脉综合症(ACS),尤其是急性心肌梗死(AMI)血运重建的重要治疗手段[1,2];而支架植入后通过非顺应性球囊实现的后扩张技术可优化支架的膨胀[1,3],降低远期心血管不良事件发生率[3,4]。因此植入支架后的后扩张是支架治疗中的重要部分,但支架植入后有时因弥漫性病变、钙化病变导致支架贴壁不良[5-7]或选用大直径的非顺应性球囊等情况,导致非顺应性球囊不能通过已植入的支架,进而无法对支架充分扩张。可采取双导丝技术、分支或同向锚定[2],甚至需子母导管增加支撑力[8-10]等技术解决,但均增加手术操作复杂性、延长手术时间、增加手术并发症及风险并增加患者经济负担。非顺应性球囊修饰技术是对非顺应性球囊尖端进行J型折弯(1~2 mm,100~120°),同时对于球囊体部分数等份轻折(60~120°)进而改善非顺应性球囊通过性的技术。本研究宗旨在通过自身前后对照比较未经修饰球囊组及修饰球囊通过率的差别,明确球囊修饰技术是否增加球囊通过性。
1 资料与方法
1.1 研究对象与分组2019年10月至2020年5月共841例患者于河北大学附属医院心血管内科接受了冠脉支架植入治疗,其中52例在支架植入后拟行支架后扩张时,应用未经修饰的非顺应性球囊到位失败,不能通过已经释放的支架,定义为修饰前组。应用球囊修饰技术后,再次尝试通过已植入的支架,定义为修饰后组。收集患者临床资料、冠脉病变特征及实验数据。该研究方案通过我院伦理委员会审核;入组患者均签署知情同意书。入选标准:年龄28~85岁,男性或非妊娠期女性;自愿签署知情同意书;符合2018版中国急性冠脉综合征指南且需行PCI的患者;支架植入后非顺应性球囊通过支架失败。排除标准:有PCI禁忌;接受过冠脉旁路移植术;合并心源性休克或室颤或急性心力衰竭的患者。
1.2 方法
1.2.1 治疗所有接受PCI的患者,术前1 d均予以阿司匹林300 mg和硫酸氢氯吡格雷300 mg治疗,术中应用普通肝素抗凝,术中活化部分凝血活酮时间(APTT)保持在正常参考范围的2~3倍,所有患者植入均为药物洗脱支架;术后予以终生的阿司匹林肠溶片(100 mg 1/d)联合1年以上的硫酸氢氯吡格雷(75 mg 1/d)或替格瑞洛(90 mg 2/d)等治疗。
所有患者均接受了经桡动脉入径的冠脉介入治疗;同一例手术由同一术者完成,术者根据冠脉解剖特点,选取6F不同类型的指引导管及导丝,根据冠脉病变的参考血管直径,选择药物涂层支架,应用半顺应性球囊预扩张,支架到位后以10~12 atm 10 s释放支架;根据支架直径,按1:1选择相应直径的非顺应性球囊进行后扩张,非顺应性球囊在不能到位时,在保证指引导管同轴的情况下,尝试加大推送力度,当指引导管被推离冠脉开口后1 cm,如球囊仍不能到位时,定义为修饰前组,撤出球囊导管,以左拇指指甲平面作为支撑,右拇指指甲尖端对球囊尖端进行J型折弯(1~2 mm,100~120°),同时对球囊体部分数等份轻折(60~120°),经修饰塑形后定义为修饰后组,再次尝试能否到位,到位后对已植入的支架进行后扩张。
1.2.2 研究终点
1.2.2.1 研究终点主要终点事件为经修饰后的非顺应性球囊通过支架成功,或应用传统的其他方法到位成功(如指引导管深插、双导丝技术、球囊锚定技术等),同时冠脉造影提示冠脉病变残余狭窄≤20%,冠脉血流3级。次要终点事件为非顺应性球囊不能回抱、非顺应性球囊破裂。术后1个以电话随访或门诊复查的形式记录患者情况,记录是否有主要心血管不良事件(MACE事件)发生(包括心源性死亡、急性心肌梗死、再次同一血管的血运重建)。
1.2.2.2 非顺应球囊修饰方法对非顺应性球囊尖端进行J型折弯(1~2 mm,100~120°),同时对于球囊体部分数等份轻折(60~120°),图1。
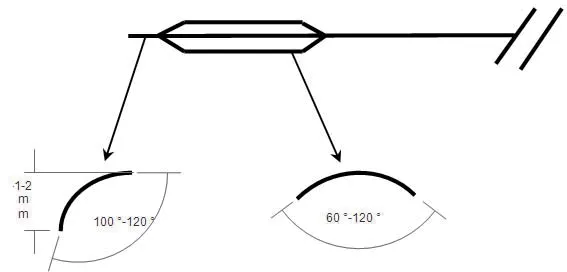
图1 非顺应性球囊修饰技术示意图
1.2.2.3 非顺应性球囊通过或到位失败在指引导管同轴良好的情况下,非顺应性球囊远端金属标记点不能达到支架末端。
1.2.2.4 球囊通过总阻力同轴状态下,给予非顺应性球囊推送力引起的指引导管被推离冠脉开口的距离。
1.2.2.5 球囊导丝摩擦阻力球囊沿导丝前进时的阻力,10分定义为完全不能前进,0分定义为完全没有阻力,同一术者根据个人手感,对同一病例进行判断评分。
1.3 统计学分析所有数据均采用SPSS 23.0统计学软件分析。计量资料采用均数±标准差(±s)表示,两组间均数的比较采用配对t检验,计数资料采用例数(构成比)表示,组间比较采用χ2检验或Fisher精确检验,球囊修饰后的通过成功率应用McNemar法统计分析。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料本实验采用自身前后对照设计,因此修饰前组及修饰后组的临床资料完全相同(表1)。52例非顺应性球囊通过支架失败病例中,直径≥3.0 mm的非顺应性球囊占73.1%,6F JL3.5指引导管占65.4%,迂曲病变或病变长度>30 mm的占65.4%,钙化病变占44.1%;支架植入冠脉中段占67.3%,但局限于本实验中入组人群均为球囊通过支架失败的病例,因此上述因素是否为非顺行性球囊通过支架失败的危险因素尚需进一步实验证实。

表1 入组患者的临床及手术资料
2.2 主要终点事件方面对首次通过支架失败的非顺应性球囊修饰后,球囊通过支架成功率为80.8%(P<0.05),修饰后组10例(18.2%)通过支架失败,其中8例采取双导丝技术通过,2例采用双导丝技术结合球囊修饰技术后通过。此外,球囊修饰后组的球囊前进总阻力小于修饰前组[(0.24±0.10)cm vs. (0.93±0.10)cm,P<0.05],但导丝摩擦阻力修饰后组高于修饰前组[(3.06±0.80) vs. (1.63±0.71),P<0.05];实验中记录到不同厂家的非顺应性球囊经修饰后通过成功率无统计学差异(P=0.236),且未出现球囊回抱不良、破裂等并发症,术后1月随访后无MACE事件发生,表2~3。

表2 患者手术相关资料
3 讨论
冠心病发病人数逐年上升,给社会造成了很大负担[11-13],而冠心病的治疗,尤其是AMI治疗,越来越依靠PCI[14],冠脉支架植入后通过非顺应性球囊实现的后扩张明显降低患者的远期支架内再狭窄及急性支架内血栓事件发生率[4,15]。非顺应性球囊,又称为后扩张球囊,多用于冠脉支架植入后的支架充分扩张,也可用于支架植入前钙化病变的预扩张及支架内再狭窄的治疗[3,4,7,16-18],其与半顺行性球囊在PCI中具有重要地位,但相较于同一厂家及直径的半顺应性集及顺应性球囊,非顺应性球囊拥有更厚的球囊材料,在未充气扩张状态下,非顺应性球囊导管的球囊附着部位直径更大。此外,由于同样的原因,同一厂家不同直径的非顺应性球囊导管,直径越大的导管,其球囊附着部分直径也越大[20],手感上球囊也越硬,因此非顺应性球囊导管的通过性相对较低。

表3 非顺应性球囊修饰后组不同后扩球囊种类通过情况b
实验中,我们通过对到位失败的后扩张球囊进行修饰后,提高了球囊到位成功率,提示球囊修饰技术通过改变非顺应性球囊的物理形态,可增加球囊通过性。非顺应性球囊通过支架过程中,是通过总阻力及术者的推进力两者共同作用;通过总阻力主要包括指引导丝对球囊的摩擦阻力和支架或冠脉病变对于球囊的阻力,其可表现于在球囊在冠脉内前进过程中,同轴状态下指引导管被推离冠脉口的距离。在相同患者、指引导管、体位、放大倍数和操作者的情况下,球囊修饰前与球囊修饰后的距离的差值可作为判断阻力改变的间接指标。为方便计算,定义未被推离冠脉口的总阻力为1 cm。修饰后组,其球囊通过总阻力较修饰前组降低,因此修饰后组的通过率得以提升。非顺应性球囊修饰技术降低了球囊通过的总阻力,但由于其没有改变球囊的涂层及亲水特性,并且增加了球囊内部与导丝之间的摩擦阻力。因此其降低球囊通过总阻力的原因在于降低了支架或冠脉病变对于球囊的外在阻力。本实验中非顺应性球囊的应用是在支架成功到位并释放之后,非顺应性球囊前进阻力的主要来源于支架的相互作用,可避免球囊导致的支架变形、损伤。据我们所知,这是目前唯一通过降低球囊前进总阻力的方法来解决支架植入后非顺应性球囊通过失败的方法。相较于双导丝技术、延长导管技术、球囊锚定或指引导管深插技术[19,21-25],其减小了冠脉开口撕裂、冠脉夹层、导丝坎顿或断裂、血管损伤、血栓及空气栓塞的风险,同时简化了手术操作,因此理论上可缩短手术时间、降低射线暴露量、同时降低了手术器材用量,降低手术费用。此外,直径≥3.0 mm的非顺应性球囊、指引导管JL3.5 、迂曲或成角病变、长病变、支架位于冠脉中段,在球囊通过失败病例中占据了50%以上,提示其可能为球囊到位失败的危险因素,但因入选的均为球囊通过失败的病例,其预测作用仍需进一步实验证实。
此外,由于后扩球囊修饰技术改变了球囊的物理形态,但对于球囊结构,尤其是外部材料、直径及充气囊内部结构并未产生影响,而非顺应性球囊对与支架的扩张效果主要取决球囊内部压力。因此,非顺应性球囊修饰技术从理论上不影响球囊对支架的后扩张效果,但需进一步实验用血管内超声成像(IVUS)证实。需指出,虽然该技术增加了导丝与球囊内部的摩擦阻力,但并未出现球囊不能回抱等并发症,且术后1个月随访无主要心血管不良事件发生提示该技术安全。
本研究的局限性在于:①球囊修饰技术仍需与双导丝技术,甚至是球囊锚定技术进行完全随机对照实验证实其有效性;②本研究为小样本单中心研究,需大样本、多中心实验证实后扩球囊修饰技术的有效性。
综上所述,非顺应性球囊修饰技术可安全有效的提高通过支架失败的球囊的通过成功率,缩短手术时间、降低手术复杂性、减轻患者经济负担,且操作简单,应用前景广阔。

