肺表面活性物质联合布地奈德治疗重症呼吸窘迫综合征早产儿的效果
孟昭慧
济南市莱芜人民医院药剂科,山东济南 271100
新生儿呼吸窘迫综合征(newborn respiratory distress syndrome,NRDS)较为常见,其多发于早产儿群体,出生4~12 h 内新生儿可发生呼吸困难等症状并逐渐加重,促使机体严重缺氧,若不及时治疗,可危及生命[1-2]。目前,临床治疗本病多于通气支持基础上加用肺表面活性物质(pulmonary surfactant,PS)治疗,可有效补充内源性PS 不足,加快肺泡表面细胞发育成熟,以提高肺泡细胞稳定性,纠正患儿气体交换障碍,改善通气功能,从而缓解机体缺氧症状[3-4]。但PS 经气管滴入不易于肺泡均匀分布,且滴入过程中会造成不同程度肺损伤,导致患儿恢复较慢。布地奈德属于糖皮质激素,其具有较高脂溶性和水溶性,且对肺泡Ⅱ型细胞受体亲和力高,进入患儿肺组织后可加快肺泡Ⅱ型细胞合成,促进PS 分泌,以增强肺功能。此外,布地奈德具有强效抗炎作用,可阻止肺泡间渗出液生成,减轻肺水肿,降低肺损伤。相关研究显示[5],激素联合PS 可降低NRDS 患儿病死率和并发症风险。鉴于此,本研究选取济南市莱芜人民医院收治的98 例重症NRDS 早产儿作为研究对象,旨在分析PS 联合布地奈德治疗重症NRDS 的临床效果。
1 资料与方法
1.1 一般资料
选取2019年7月—2020年7月济南市莱芜人民医院收治的98 例重症NRDS 早产儿作为研究对象,按随机数字表法将其分为两组,每组各49 例。对照组中,男25 例,女24 例;胎龄27~34 周,平均(30.15±1.24)周;出生体重1205~1484 g,平均(1328.56±104.39)g;身长36~42 cm,平均(39.52±1.53)cm;NRDS 分级:Ⅲ级34 例,Ⅳ级15 例。观察组中,男27例,女22 例;胎龄27~35 周,平均(30.18±1.26)周;出生体重1212~1488 g,平均(1328.63±105.12)g;身长37~42 cm,平均身长(39.57±1.56)cm;NRDS 分级:Ⅲ级33 例,Ⅳ级16 例。两组患儿的一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经济南市莱芜人民医院医学伦理委员会审核及同意,患儿家属均知晓本研究情况并签署知情同意书。
1.2 纳入及排除标准
纳入标准:患儿均符合《儿科学》[6]中NRDS 相关诊断;患儿的NRDS 分级为Ⅲ~Ⅳ级;患儿的出生体重低于1500 g;患儿的胎龄<37 周;患儿均于分娩8 h 内进行治疗。
排除标准:呼吸道存在先天畸形的患儿;伴有吸入性肺炎的患儿;神经系统严重异常的患儿;对本研究用药过敏的患儿。
1.3 方法
两组患儿均接受保暖、通气支持、抗感染、清除气道分泌物等对症治疗。
对照组患儿加用PS(华润双鹤药业股份有限公司,国药准字H20052128,生产批号:20190528)治疗,于分娩8 h 内给药,先对PS 进行预热,待温度达37℃后,将150 mg/kg 的PS 抽取至注射器内,插入气管导管内,抬高患儿上身30°,仰卧位将药液缓慢滴入支气管内,完毕后加压给氧5 min,便于药物肺内均匀分布,若病情无明显改善,8~12 h 后可再次予以PS。
观察组患儿于对照组基础上予以布地奈德(As traZeneca Pty Ltd,国药准字H20140475,生产批号:20190615)治疗,将0.25 mg/kg 与预热的PS 混匀后采用上述方法滴入支气管内,PS 剂量同对照组,若无明显改善,可于8~12 h 后再次予以PS,但不加用布地奈德。
两组均用药至吸入氧浓度低于40%或拔管。
1.4 观察指标及评价标准
①动脉血气状况。治疗前和治疗24 h 后,以GEM3500 型血气分析仪(南京汉誉医疗科技有限公司)检测两组患儿的动脉血氧分压(partial pressure of oxygen in artery,PaO2)、二氧化碳分压(partial pressure of carbon dioxide,PaCO2)和氧合指数(oxygenation index,OI)变化,其中OI=PaO2/吸入氧浓度。②呼吸机相关参数。治疗前和治疗24 h 后,比较两组患儿的吸气峰压(peak inspiratory pressure,PIP)、吸入氧浓度(frac tion of inspire O2,FiO2)和呼吸频率(respiratory rate,RR)变化。③通气相关指标。比较两组患儿的有创通气时间、撤机时间和住院时间。④不良反应。包括发热、心率减慢。
1.5 统计学方法
采用SPSS 22.0 统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,两组间比较采用独立样本t检验,组内比较采用配对样本t检验;计数资料采用率表示,组间比较采用χ2检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患儿治疗前后动脉血气状况的比较
两组患儿治疗前的动脉血气指标比较,差异无统计学意义(P>0.05);两组患儿治疗后的PaO2、OI 均高于治疗前,PaCO2均低于治疗前,且观察组患儿治疗后的PaO2、OI 高于对照组,PaCO2低于对照组,差异有统计学意义(P<0.05)(表1)。
表1 两组患儿治疗前后动脉血气状况的比较(mmHg,±s)

表1 两组患儿治疗前后动脉血气状况的比较(mmHg,±s)
与本组治疗前比较,aP<0.05;1 mmHg=0.133 kPa
组别PaO2治疗前治疗后PaCO2治疗前治疗后OI治疗前治疗后观察组(n=49)对照组(n=49)t 值P 值44.15±5.03 44.18±5.05 0.030 0.977 81.79±6.79a 76.68±6.34a 3.851 0.000 60.35±5.71 60.42±5.74 0.061 0.952 40.52±4.58a 45.31±4.62a 5.154 0.000 203.96±12.52 205.48±12.75 0.595 0.553 283.69±19.13a 264.41±17.76a 5.170 0.000
2.2 两组患儿治疗前后呼吸机相关参数的比较
两组患儿治疗前的呼吸机相关参数比较,差异无统计学意义(P>0.05);两组患儿治疗后的PIP、FiO2、RR 均低于治疗前,且观察组患儿治疗后的PIP、FiO2、RR 低于对照组,差异有统计学意义(P<0.05)(表2)。
表2 两组患儿治疗前后呼吸机相关参数的比较(±s)

表2 两组患儿治疗前后呼吸机相关参数的比较(±s)
与本组治疗前比较,aP<0.05
组别PIP(cmH2O)治疗前治疗后FiO2(%)治疗前治疗后RR(次/min)治疗前治疗后观察组(n=49)对照组(n=49)t 值P 值23.16±3.12 23.21±3.16 0.079 0.937 17.89±1.86a 19.65±2.02a 4.487 0.000 51.42±5.39 51.45±5.42 0.028 0.978 29.68±4.05a 33.71±4.27a 4.793 0.000 45.63±4.85 45.71±4.91 0.081 0.936 35.42±4.31a 40.28±4.65a 5.366 0.000
2.3 两组患儿通气相关指标的比较
观察组患儿的有创通气、撤机和住院时间短于对照组,差异有统计学意义(P<0.05)(表3)。
表3 两组患儿通气相关指标的比较(d,±s)

表3 两组患儿通气相关指标的比较(d,±s)
组别有创通气时间撤机时间住院时间观察组(n=49)对照组(n=49)t 值P 值3.25±0.42 4.51±0.86 4.25 0.00 27.69±3.65 31.14±3.85 3.92 0.00 40.13±5.62 46.85±5.79 2.08 0.02
2.4 两组患儿不良反应发生情况的比较
两组患儿的不良反应总发生率比较,差异无统计学意义(P>0.05)(表4)。两组患儿均未发生严重不良反应,经过对症处理后未影响治疗。
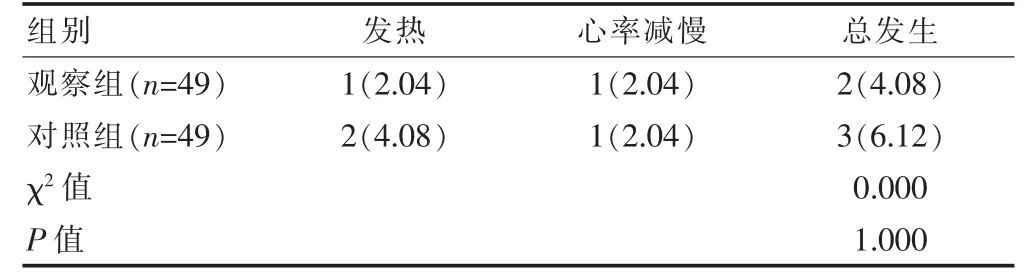
表4 两组患儿不良反应发生情况的比较[n(%)]
3 讨论
NRDS 多由PS 不足所致,患儿肺泡因PS 缺乏会逐渐萎缩,引起进行肺不张,从而导致气体交换障碍,诱发呼吸困难等症状,造成机体缺氧、酸中毒[7-8]。而PS 于孕18~20 周开始分泌,35~36 周时肺部方可发育至成熟状态,故本病多发于早产儿群体,且越早出生发病风险越高。目前,临床治疗本病多于早期予以辅助通气治疗,以快速纠正机体缺氧状态,阻止病情继续恶化,缓解呼吸困难等症状,但常规通气治疗效果有限,无法从根本上解决PS 分泌不足问题[9]。
PS 是由肺泡Ⅱ型细胞分泌的脂蛋白,经支气管滴入后,可快速到达肺组织,增加肺部PS 含量,并于肺泡液层表面呈单分子层形式排列,以降低肺表面张力,增强肺泡容量稳定性,促使肺泡复张,从而建立良好气体交换平台,提高肺通气能力[10-11]。PS 还可提高肺顺应性,减低呼吸阻力,减少肺泡间黏液生成,以降低肺部出血和肺水肿风险[12-13]。但NRDS 病情危急,单药疗效有限,不利于患儿病情快速好转,且PS 对肺部炎性损伤改善效果欠佳。本研究结果显示,两组患儿治疗前的动脉血气状况比较,差异无统计学意义(P>0.05);两组患儿治疗后的PaO2、OI 均升高,PaCO2均降低,且观察组患儿治疗后的PaO2、OI 高于对照组,PaCO2低于对照组,差异有统计学意义(P<0.05);两组患儿治疗前的呼吸机相关参数比较,差异无统计学意义(P>0.05);两组患儿治疗后的PIP、FiO2、RR 均降低,且观察组患儿治疗后的PIP、FiO2、RR 低于对照组,差异有统计学意义(P<0.05);观察组患儿的有创通气、撤机和住院时间短于对照组,差异有统计学意义(P<0.05);两组患儿的不良反应总发生率比较,差异无统计学意义(P>0.05)。提示PS 联合布地奈德治疗重症NRDS 效果显著,可改善动脉血气状况,促进肺组织成熟,缩短有创通气时间,且不良反应少。周栩平等[14]研究显示,布地奈德联合PS 治疗重症NRDS 效果显著,可改善患儿血氧指标,缩短有创通气时间、撤机时间,加快患儿病情好转,与本研究结果相类似。布地奈德属于非卤化激素,将其混合PS 一起滴入支气管,可尽早到达肺内,提高肥大细胞膜稳定性,降低免疫反应和透明质酸酶活性,减少炎症介质释放,从而减轻肺部炎性损伤,促进肺组织修复,以加快肺通气功能恢复。布地奈德还可提高肺泡纤毛摆动功能,减少肺泡萎陷,增强肺顺应性,且该药与肺泡Ⅱ型细胞亲和力高,可加快内源性PS 合成,加速肺发育成熟,增强肺功能[15]。与PS 联用后可协同增效,利于尽早控制肺部炎症反应,减轻肺损伤,减少PS 消耗,并能拮抗肺实质过度异常修复,避免支气管肺发育不良,进而帮助患儿恢复肺正常功能,提高自主呼吸能力,缩短呼吸机支持时间。但本研究仍存在一定局限性,研究所收集样本量有限,可能存在一定误差,且观察指标较少,未能进一步分析两药联合对减少重症NRDS 患儿支气管肺发育不良等并发症的影响,后续仍需扩大样本量,增加观察指标,进一步明确布地奈德联合PS 的治疗制剂,以论证本研究观点。
综上所述,PS 联合布地奈德可提高重症NRDS患儿PaO2,纠正机体缺氧状态,促进PIP、FiO2、RR 降低,以缩短撤机时间,减轻肺损伤,且安全性高。

