一种MOFs材料2,5-吡啶羧酸锂盐的电化学性能研究
郝丽敏,甘 露
(重庆航天职业技术学院 重庆 400021)
1 引言
金属有机骨架化合物MOFs是Metal Organic Frameworks的英文简称,它是指由无机金属中心(金属离子或金属簇)与桥连的有机配体通过自组装作用相互连接,形成的一类具有周期性网络结构的晶态多孔材料。MOFs材料是一种既不同于无机多孔材料,也不同于一般有机配合物的杂化材料,通常也称其为有机-无机配位聚合物,兼具无机材料的刚性和有机材料的柔性。MOFs材料由于其独特的性能特征,在现代材料研究、生物、化学等多个领域方面呈现出巨大的发展潜力,具有重要的研究价值。
吡啶羧酸类配体是一类含有N和羧基配体的多功能典型性配体,能够充分结合并体现出含N和羧基配体二者的优点,因此,在配位能力和配位形式上具有了丰富且突出的特点。由吡啶羧酸类配体通过与金属离子组装配合而成的一类MOFs材料称为吡啶羧酸盐类材料[1]。根据羧基在含N吡啶环上所处位置的不同,吡啶二甲羧酸有2,5-吡啶二甲酸、3,5-吡啶二甲酸、2,6-吡啶二甲酸和3,4-吡啶二甲酸等多种异构体。因此,吡啶羧酸类MOFs材料具有了不对称性,且其能通过配位与N、O形成不同功能的原子,金属离子在与其发生配位取代时可以具有不同的选择性,能够以多种方式与金属离子结合。此外,吡啶羧酸类MOFs材料还能通过发生一系列自组装反应,从而形成具有次级单元和多核结构的聚合物。近年来,某课题组成员选用2,5-吡啶二甲酸(C7H5NO4)与氢氧化钠(NaOH)反应,得到了吡啶羧酸类MOFs材料2,5-吡啶二甲酸钠,通过电化学性能测试,该含氮环吡啶二甲酸钠盐的可逆容量达到了190 mAh/g[2]。
本文通过溶液法制备2,5-吡啶羧酸锂盐,对该邻位取代羧酸锂盐的电化学性能进行分析研究,讨论探索吡啶羧酸盐类材料用作锂离子电池负极材料的可能性。
2 材料制备
采用溶液法制备2,5-吡啶羧酸锂盐,首先称取LiOH·H2O 0.084 g溶于20 mL无水乙醇(EtOH)并充分溶解;另称取2,5-吡啶二甲酸(C7H5NO4)0.167 g溶于20 mL无水乙醇(EtOH)中,待充分溶解后,将以上两种溶液混合并充分搅拌2 h,完全混合均匀后过滤,将过滤后的溶液在80 ℃真空环境中干燥直至所用溶剂完全蒸发,得到反应成品白色粉末。
根据基本的化学反应原理:酸碱相遇后会发生中和反应,两种原料分别属于酸类和碱类,因此,预测该反应的生成物可能为吡啶羧酸锂盐,图1为该锂盐的化学结构制备示意图。
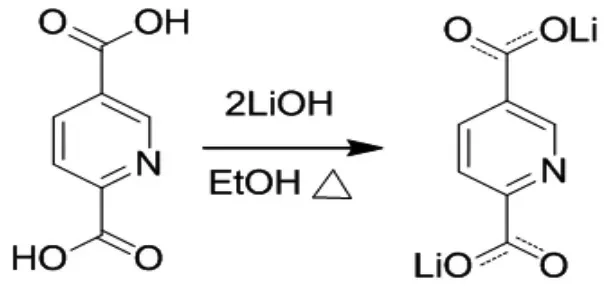
图1 实验制备2,5-吡啶羧酸锂盐的化学结构示意图
3 测试结果研究
3.1 XRD (X-射线衍射分析X-ray Diffraction)图谱分析
图2为本实验所制备的2,5-吡啶羧酸锂盐的XRD图谱,以及反应原料2,5-吡啶二甲酸的XRD图谱对比。由图可见,两者的衍射峰出现在不同角度,2,5-吡啶羧酸锂盐的物相分析中未出现原料2,5-吡啶二甲酸的晶相图谱,这说明反应原料2,5-吡啶二甲酸与LiOH·H2O发生化学反应生成了新物相2,5-吡啶羧酸锂盐,该锂盐与反应所取原料2,5-吡啶二甲酸完全不同[3]。但目前暂时未对反应所生成的2,5-吡啶羧酸锂盐进行单晶结构分析,所以无法准确表述2,5-吡啶羧酸锂盐的具体物相和结构类型。

图2 2,5-吡啶羧酸锂盐与2,5-吡啶二甲酸的标准PDF卡对比
3.2 红外图谱分析(FTIR)
图3为本实验所制备的2,5-吡啶羧酸锂盐及其对应的反应原料2,5-吡啶二甲酸配体的红外图谱。由图可见,在1 700 cm-1时,反应原料2,5-吡啶二甲酸会有一个较强的吸收峰,这主要归结为其所带羰基的特征峰。当反应原料2,5-吡啶二甲酸与锂离子发生化学反应后,在1 700 cm-1时,实验制备的2,5-吡啶羧酸锂盐基本没有出现吸收峰,且在低波数700 cm-1和1 500 cm-1时出现了羧基的对称反对称伸缩振动峰,这充分说明了原料2,5-吡啶二甲酸中羰基上的质子已脱掉完全[4],并与锂离子结合形成了2,5-吡啶羧酸锂盐。

图3 2,5-吡啶二甲酸及其对应产物2,5-吡啶羧酸锂盐的红外图谱
结合图2中的XRD图谱分析结果,可以完全确认,反应物2,5-吡啶二甲酸已经与LiOH·H2O两种原料已经发生化学反应,生成了新物质2,5-吡啶羧酸锂盐。
3.3 SEM扫描电镜测试(Scanning Electron Microscope)图谱分析
图4为本实验所制备的2,5-吡啶羧酸锂盐的SEM图谱。从该图谱中可分析反应生成物2,5-吡啶羧酸锂盐的形貌。由图可知,2,5-吡啶羧酸锂盐团聚现象较为严重,呈现为层状结构的一次粒子,粒子大小约为4 μm。此外,图中能观察到的散落在2,5-吡啶羧酸锂盐旁边的更细小的不明微粒,可能是反应生成的中间产物,这是由于所测样品本身的导电性能较差,且形成该中间产物与样品制备时的工艺、溶剂及蒸发温度等多种因素均有关。

图4 反应生成物2,5-吡啶羧酸锂的SEM图谱
3.4 恒电流充放电(Galvanostatic Charge/Discharge Measurement)测试和循环伏安(Cyclic Voltammetry,CV)性能分析
图5为本实验所制备的2,5-吡啶羧酸锂盐的充放电曲线及其循环稳定性曲线。将实验制备的2,5-吡啶羧酸锂盐电极活性材料充分研磨后,将质量比为7:2:1的电极材料、super P与PVDF均匀混合,同时加入N-甲基吡咯烷酮少许,充分搅拌,得到黏稠的黑色浆料。该浆料即为待测活动性材料,将其均匀涂抹在铜片(直径约为16 mm)上,真空条件下,100 ℃干燥,10 h后可得到实验所需的负极材料电极片。将该电极片与金属锂片、隔膜、正极壳、负极壳和适量电解液在充满高纯度Ar气的手套箱内组装成2025型扣式电池,用于测试材料的电化学性能。

图5 实验制备2,5-吡啶羧酸锂盐电化学性能分析图
实验所用测试电压:0.2~3 V,电流密度:50 mA/g,CV曲线的扫描速率:0.3 mV/s。
由图a可知,2,5-吡啶羧酸锂首次放电比容量达到380.6 mAh/g,在1.5 V左右时出现了放电平台,其首次充电比容量约为220.7 mAh/g,由此可得出2,5-吡啶羧酸锂盐在首次充放电循环中出现的不可逆容量为159.9 mAh/g,这可能是由于2,5-吡啶羧酸锂盐在首次充放电过程中的结构尚不稳定,且在充放电时材料表面形成了钝化层SEI膜[2],该膜会消耗一定量的锂离子活性,产生较大的不可逆比容量。由图b可知,2,5-吡啶羧酸锂盐的循环稳定性总体比较稳定,在循环过程中其比容量略有衰减,循环60次后,其充电比容量为195.0 mAh/g,放电比容量为201.2 mAh/g。由此得出,2,5-吡啶羧酸锂盐在循环过程中的比容量较高,循环性能也较为稳定。
经实验测试,反应原料2,5-吡啶二甲酸和LiOH·H2O的充放电比容量极低,而反应产物2,5-吡啶羧酸锂盐具有不同于原料的充放电性能,这同时也从另一方面进一步证明了2,5-吡啶二甲酸和LiOH·H2O两种原料确实已经发生了化学反应,形成了新物质2,5-吡啶羧酸锂盐。
4 小结
本文以2,5-吡啶二甲酸和LiOH·H2O为反应原料,用溶液法制备形成了层状2,5-吡啶羧酸锂盐,该材料的具体结构暂时未知,对2,5-吡啶羧酸锂盐这种有机羧酸锂盐材料进行了充放电性能测试分析,初步分析研究了2,5-吡啶羧酸锂盐的电化学性能。结果表明,当电流密度为50 mA/g,电压范围为0.2~3 V进行充放电时,2,5-吡啶羧酸锂盐的充放电性能较好,循环性能较为稳定。
目前,将吡啶羧酸锂盐类MOFs材料用作锂离子电池电极材料的研究仍处于起步阶段,今后的研究方向将继续锁定在该吡啶羧酸锂盐的单晶结构的确定、多种异构体吡啶羧酸锂盐的电化学性能比较、缩小吡啶羧酸锂盐的颗粒尺寸所需反应条件以及提高吡啶羧酸锂盐材料的电化学性能等方向。

