超声造影在腹主动脉瘤腔内修复术后内漏检测中的应用
李先涛,叶小剑,林奕辰,郭平凡
腹主动脉瘤腔内修复术(endovascular aortic repair, EVAR)术后内漏发生率相当高,需要终身随访以早期发现内漏和预防动脉瘤破裂[1]。EVAR术后影像学随访方式包括X光、CT血管造影(CT angiography, CTA)、MR血管造影(MR angiography, MRA)、常规动脉造影和彩色多普勒超声等检查,各种检查方式在发现内漏的准确性方面各有优势[2],其中CTA因可精确评估瘤体的形态学特征、瘤腔直径、移植物锚定性能和结构变化,目前仍作为EVAR术后的主要随访方式,但其弊端也很明显,如造影剂肾病、辐射相关的癌症风险以及高昂的费用。理想的随访工具应具备以下优点:经济、精确、安全、辐射小、重复性高、可广泛使用。彩超具有无创、经济、易携带、无辐射、无肾毒性、可明确血流方向等特点,新一代超声造影剂的出现使得超声造影(contrast-enhanced ultrasound, CEUS)技术得以进一步发展,在发现内漏方面的性价比也相当高。本研究通过与传统的CTA比较,探讨以CEUS为基础的随访模式在EVAR术后随访中的应用价值。
1 对象与方法
1.1 对象 收集2019年7月1日-2020年11月1日收治并成功实施EVAR术的肾下型腹主动脉瘤患者62例,男性50例,女性12例;年龄(68.17±6.23)岁(58~83岁),其中>80岁10例;体质量指数(body mass index,BMI)为(22.09±2.79)kg/m2。合并高血压病46例,合并糖尿病6例,合并冠状动脉粥样硬化性心脏病(冠心病)8例,合并心力衰竭3例,合并肾功能不全19例,术中同期施行瘤腔弹簧圈栓塞术14例。在术后1个月内,分别行CTA及CEUS检查,两种检查相隔时间<1周。纳入标准:成功实施EVAR术的肾下型腹主动脉瘤患者,对随访的依从性强。排除马凡综合征、炎性动脉瘤、破裂腹主动脉瘤、术中使用平行支架移植物或开窗开槽技术及开放或复合手术患者。本研究经医院伦理委员会审批同意,患者均知情同意。
1.2 方法
1.2.1 影像学工具和造影剂 CEUS采用彩色多普勒超声(IU22,荷兰飞利浦公司),探头C5-1,频率1~5 MHz,超声造影剂为声诺维(六氟化硫微泡)(瑞士Bracco Imaging B.V.公司);CTA采用320排 CT机(德国西门子公司),造影剂为碘海醇注射液(泰州扬子江药业集团)。检查前充分告知患者两种随访工具的利弊。
1.2.2 CEUS操作流程 整个腹主动脉从膈肌水平扫描至髂外动脉,注意瘤体内有无血流信号充填。取横断面上最宽处前后径和左右径的平均值为瘤体直径。超声造影剂采用团注法,首剂1 mL,随后推注0.9%的生理盐水5 mL。探头先扫描横断面,从支架的头端至尾端连续动态扫描,注意支架近远端锚定区、支架组件连接部位,观察是否有造影剂微泡渗透至瘤体内或瘤体外血管,是否逆行灌注瘤腔。一旦探及微泡进入瘤腔,应确认位置,待血管内造影剂完全清除后,再追加1 mL造影剂,聚焦于可疑内漏位置。记录内漏出现时间、微泡渗出位置、反流侧支的尺寸及瘤腔内微泡弥散的范围。诊断困难时,可重复上述步骤1次。所有动态图像储存于移动硬盘便于后续分析。CEUS由一位具有15 a以上工作经验的超声医师使用同一台超声机独立完成操作并出具报告,对CTA结果不知晓。
1.2.3 CTA操作流程 采用双筒高压注射器以4 mL/s的流率经肘正中静脉注射90 mL造影剂及30 mL生理盐水。应用对比剂监测法,ROI设于膈肌水平降主动脉层面,监测CT值达到阈值250 Hu自动触发动脉期扫描,静脉期扫描延迟1 min,扫描厚度1 mm,使用1和7 mm层厚行三维重建,管电压及管电流均采用自动调节技术。由具有15 a以上工作经验的血管外科及放射科医师独立判断CTA诊断结果,有争议时双方共同讨论并得出最终结论。
1.2.4 内漏的定义和分型 内漏是动脉瘤腔内、支架移植物外持续的血流灌注,分为5型[3]:1型来源于支架近端(1a)或远端锚定区(1b);2型来源于侧支血管,如肠系膜下动脉、腰动脉、副肾动脉;3型来源于支架组件的连接处;4型来源于支架移植物的孔隙;5型为瘤腔内高压,但无明确来源。
2 结 果
2.1 一般情况 62例中,19例(30.64%)患者合并肾功能不全,其中14例合并内漏高危因素,即瘤体外至少3对腰动脉是通畅的或肠系膜下动脉直径>3 mm,均施行瘤腔内弹簧圈栓塞术以预防内漏。
2.2 CTA和CEUS诊断EVAR术后内漏情况 CTA和CEUS发现内漏的类型和数量详见表1和图1。CTA判断总的内漏发生率为22.58%(14/62),CEUS为25.81%(16/62),二者对1型和3型内漏的判断基本一致,1型2例,3型1例;而对2型内漏,CTA诊断了11例(17.74%),CEUS诊断了13例(20.97%)。CEUS多发现的2例均为EVAR术中使用瘤腔弹簧圈栓塞的患者(图2),但二者差别无统计学意义。CTA测量瘤体的直径为(54.2±9.2)mm,CEUS为(53.4±11.1)mm,二者差别无统计学意义。CTA检查时长较CEUS明显缩短(P<0.05)。

表1 CTA和CEUS诊断EVAR术后内漏情况
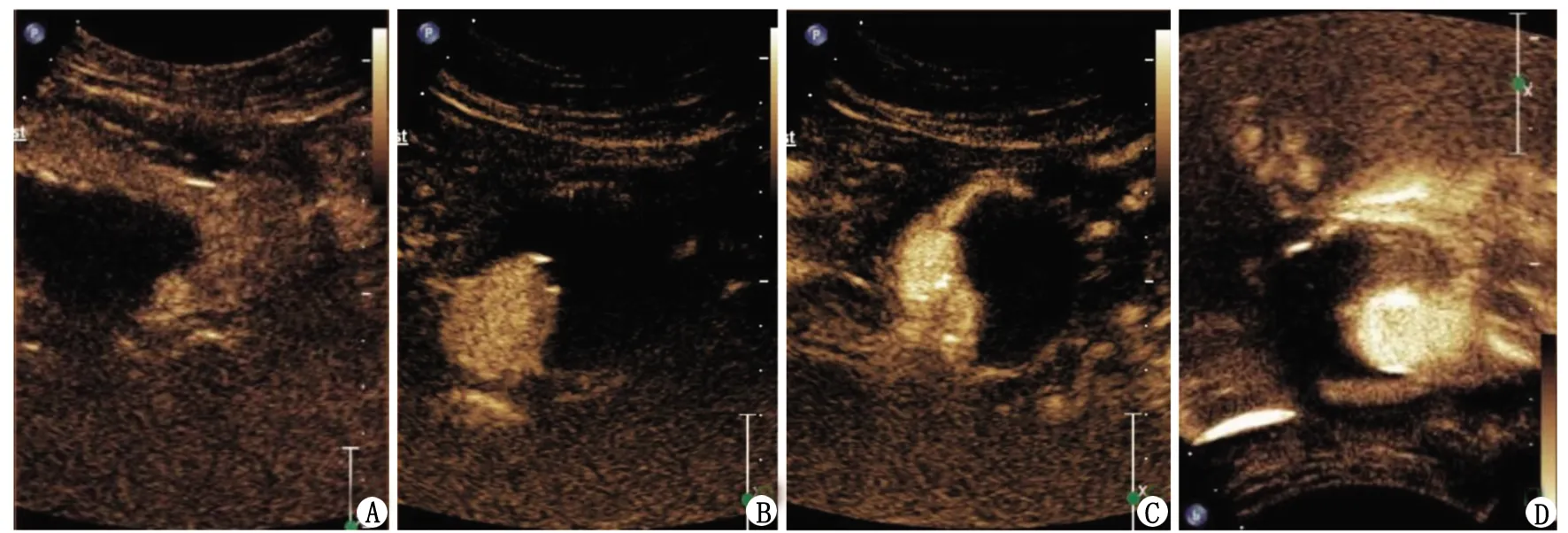
A:瘤体远端来源的1b型内漏;B:肠系膜下动脉来源的2型内漏,在造影剂推注18 s时尚未显影;C:肠系膜下动脉来源的2型内漏,在造影剂推注30 s后清晰可鉴;D:发生于主髂动脉支架连接处的3型内漏。
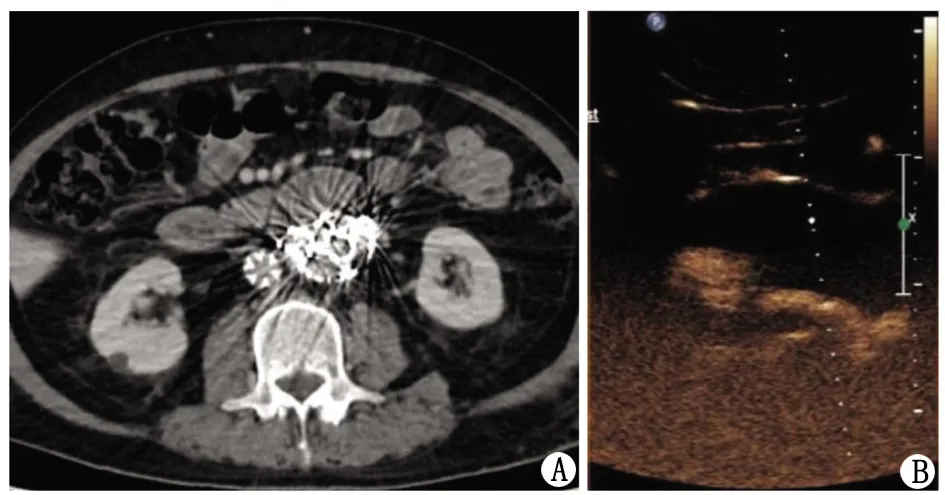
A:CTA检查显示瘤腔内金属弹簧圈造成的伪影;B:超声造影显示2型内漏来源于右侧腰动脉。
3 讨 论
EVAR是当前处理腹主动脉瘤切实可行的方案,但其术后并发症发生率较高,以内漏最受关注,其中2型内漏最常见[2]。本研究显示,以CTA和CEUS为诊断标准时,内漏总发生率分别为22.58%和25.81%,均以2型内漏为主。但两种随访工具对1型和3型内漏的判断一致。大多2型内漏为良性内漏,可进一步观察,无需紧急处理。本研究中,CEUS比CTA多发现2例2型内漏,均为EVAR术中使用瘤腔弹簧圈栓塞的患者。CTA漏诊考虑与金属伪影的影响有关,而CEUS不会受此干扰,仍可准确判断内漏的来源及血流方向。对于瘤体直径的判断,CEUS和CTA有一定差异,但未达到统计学意义。超声的特点是具有操作者依赖性,由同一位超声医师使用同一台机器进行CEUS可最大程度避免操作者偏倚。
Brown等[3]发现,大多数EVAR后动脉瘤破裂发生在术后3 a内,死亡率60%,破裂前仅有35%的患者在随访过程中监测到内漏。CTA和CEUS在检测内漏时,结果不一致的主要是2型内漏。本研究结果与之相似,CEUS似乎能发现更多的2型内漏,这与其动态观察、可重复性高、不受金属伪影干扰有关,而2型内漏的干预指征是瘤体直径增加,故对瘤体直径的动态测量极其重要。本研究中,CEUS对瘤体直径的判断与CTA无显著差别。近年来,国内使用的超声造影剂多为第2代造影剂,具有绝佳的敏感性,且严重过敏反应的发生率仅0.001%,而第1代造影剂在注射初期易出现伪影,导致假阳性[4]。另外,注射方式也可影响诊断灵敏度,连续注射能使检查时间延长,从而发现缓慢型内漏。CEUS能动态监测缓慢出现的内漏,而CTA则有可能错过扫描期,也是造成以CTA为金标准时CEUS出现假阳性的原因。Chung等[5]的综述系统分析了8篇对比CEUS和CTA的临床研究,发现CEUS诊断内漏的灵敏度为0.914(95% CI:0.866~0.949),特异度为0.782(95%CI:0.741~0.820)。Harky等[7]筛选了18篇文章共计1 773例患者,结果发现1型内漏发生率4.3%,两种工具的检出率无差异;2型内漏检出率,CEUS为22%,CTA为23%;3型内漏检出率,CEUS为1.8%,CTA为2%;CEUS诊断内漏的灵敏度高于CTA,特异度无明显差异。Kapetani等[6]发现,CEUS总的灵敏度和特异度分别为94%和93%,诊断1型和3型内漏的灵敏度和特异度分别为97%和100%。Yang等[7]发现,CEUS能发现CTA不能发现的内漏,CEUS和常规彩色多普勒超声均能监测到内漏时,CEUS可提供更多的内漏信息,如微泡的弥散模式和流动的时间窗,从而有利于分型并判断严重程度。该团队的研究证实,当CTA出现可疑假阴性结果时,CEUS的确能提供更多的阳性内漏信息。Bredahl等[8]报道了10例CTA诊断为2型内漏但CEUS却未发现的内漏病例,随访过程(615~1 476 d)不需要再干预;另外,所有需要再干预的内漏,CEUS和CTA均可发现,而CTA发现但CEUS忽略的内漏,要么自行消失,要么还不足以造成瘤腔增大。因此,EVAR术后第1年的随访,CEUS完全可以取代CTA。而对于CTA或CEUS均未发现内漏的患者,可以普通多普勒超声作为随访工具,监测瘤腔直径变化,当无定论或考虑再次干预的病例才采用CTA检查。
部分研究认为,MRA比CTA更易检出内漏[9],但此观点忽略了金属血管移植物产生的伪影,而且由于强有力的磁场,支架移植物有移位的风险。另有学者建议,以彩色多普勒超声替代CTA,虽然可准确测量直径,但其诊断内漏的灵敏度不足[10]。Lowe等[4]报道,三维CEUS相对于CTA具有显著的优势,诊断内漏更准确、更灵敏,但限于技术条件,目前在该团队暂无法执行。
CEUS的不足之处是操作者依赖性,连续扫描时只能在动脉瘤一个特定的层面进行分析,如果扫描时内漏未出现,则需要追加一剂造影剂再次扫描,且对于内漏来源的判断需要丰富的经验。CEUS无法发现支架断裂、打折、移位或组件分离,但可提供间接征象,如支架打折后引起的血管狭窄,在PW模式中表现为支架内流速增加。
本研究的不足之处为单中心研究,样本量小,随访期短。CEUS用于EVAR术后随访安全、有效、经济、可重复性好、患者满意度高,尤其适用于术中瘤腔弹簧圈栓塞的患者,但不能完全替代CTA,尤其对于1型或3型内漏以及瘤体直径增加的2型内漏,仍需采用CTA进行充分评估以计划再次介入干预。

