RNA病毒感染性疾病的皮肤表现
刘力豪,宗文凯,崔盘根,陈 敏
RNA病毒,根据巴尔的摩病毒分类系统可分为正义单链RNA病毒、反义单链RNA病毒、双链RNA病毒及单链逆转录病毒。RNA病毒所致的传染病在引起机体不同器官系统损害的同时,也可引起皮肤黏膜损害,且皮损种类多,表现复杂。部分RNA病毒所致传染病早期可能仅有皮肤黏膜表现,易发生误诊、漏诊以致延误有效的治疗,最终导致疾病的播散。本文就以RNA病毒感染所致传染病伴随的皮肤黏膜表现或其典型皮肤表现及其可能的相关机制进行综述。
1 正义单链RNA病毒
1.1 冠状病毒(coronavirus)
严重急性呼吸综合征冠状病毒(severe acute respiratory syndrome-associated coronavirus,SARSCoV)和SARS-CoV-2可产生严重的下呼吸道感染,且可引起大规模爆发[1]。严重急性呼吸综合征(severe acute respiratory syndrome,SARS)是由SARS-CoV引起的一种以发热及呼吸道症状为主的急性传染病。有报道2例SARS患者在发病后5 d出现玫瑰红色丘疹,直径2~3 mm,外有红晕,压之不褪色,分布于双上肢及面颈部,无疼痛及瘙痒等不适。随后褪至暗紫色,并逐渐缩小,红晕扩大。持续到第3周仍未完全消退。结合患者病史,考虑与SARS感染相关[2]。2019冠状病毒病(coronavirus disease 2019,COVID-19)是由SARS-CoV-2感染所致的以发热、干咳等症状为主,严重时可出现多器官衰竭甚至死亡的疾病。COVID-19相关的皮肤黏膜表现包括斑丘疹、荨麻疹样、水痘样水疱、网状青斑及紫癜样皮损。皮损一般见于病情活动期,可在数日内消退,多伴有瘙痒症状[3]。另有报道COVID-19患者出现手足末端水肿性红斑、水疱、血疱、黑痂,伴有疼痛不适,被称为冻疮样皮损(chilblain-like lesions,CLL)。一般是在病程晚期出现,平均持续12.7 d,皮损可自行好转,多见于儿童及青少年[4]。皮损相关机制目前尚未明确,有学者提出可能与异常补体激活及在微血管中沉积导致血管损伤相关[5]。有COVID-19患儿在病程第2~4周出现川崎病样表现,也被称为儿童多系统炎症综合征,此类表现考虑可能与延迟免疫激活导致细胞因子风暴相关[6]。目前就皮肤黏膜损害与COVID-19病情严重程度的相关性尚未有定论[3]。
1.2 寨卡病毒
寨卡病毒(zika virus,ZIKV)感染者会出现低热、皮损、关节疼痛和结膜炎等症状。ZIKV感染相关皮损通常为红色斑疹、丘疹、斑丘疹,呈圆形至椭圆形或网状分布,压之褪色,伴有剧烈瘙痒。常先出现躯干部,后扩散至面部、四肢,随后可泛发全身。皮损多在首发症状出现后1~2 d内出现,随后2~3 d后逐渐缓解,平均持续6 d。皮损消退伴细小脱屑,消退后无瘢痕形成或色素改变。瘙痒症状一般在皮损消退后3~5 d缓解[7,8]。不典型皮损包括风团、口腔黏膜溃疡、因ZIKV免疫介导的血小板减少引起皮肤黏膜出血表现。相关皮损可能与ZIKV在真皮巨噬细胞及皮肤成纤维细胞内复制而触发初始免疫反应,或ZIKV在角质形成细胞内复制躲避宿主免疫应答相关[8]。有ZIKV感染患者在痊愈后可出现点滴型银屑病或泛发性脓疱型银屑病,这些患者无银屑病既往史或家族史,考虑可能与角质形成细胞源性炎症递质的刺激作用及在皮肤中的多功能T淋巴细胞介导的免疫反应相关[9]。
1.3 登革病毒
登革热是由登革病毒(dengue virus)引起的急性传染病,临床表现多为高热、寒战、头痛、肌肉疼痛。于发热后 3~7 d在颜面、四肢出现充血性皮损或点状出血疹,典型皮损为四肢的针尖样出血点,或融合成片的红斑疹,疹间可见散在片状正常皮肤,称为“皮岛”,亦可出现不同程度的皮肤或黏膜出血现象。有推测是特异 CD8+T 淋巴细胞高度活化增殖,同时皮肤淋巴细胞相关抗原通过病毒特异性CD4+及CD5+T淋巴细胞相关性循环转移到皮肤上进行表达[10]。也有推测皮损出现的机制为病毒复制增殖引起的两次病毒血症,导致的炎性递质释放,使皮肤血管通透性增加、组织水肿、毛细血管破裂而引起相关皮损[11]。
1.4 丙型肝炎病毒
慢性丙型病毒性肝炎是由丙型肝炎病毒(hepatitis virus C,HCV)所致,可伴随皮肤损害,包括混合性冷球蛋白血症(mixed cryoglobulinemia,MC)、迟发性皮肤卟啉病(porphyria cutanea tarda,PCT)等。MC表现为下肢皮肤痛性可触及性紫癜、瘀斑及溃疡,考虑可能HCV-IgG抗体与HCV-脂蛋白复合物刺激形成免疫复合物所致。PCT表现包括皮肤脆性增加、光敏性皮损、色素沉着,曝光部位可有水疱或大疱形成,可能病因包括HCV感染影响肝脏功能受损、肝细胞损伤导致尿卟啉原脱羧酶活性降低、肝脏自身免疫反应增强等[12]。也有报道,HCV感染也与扁平苔藓、多形红斑、过敏性紫癜、白塞病、结节性痒疹、皮肤瘙痒症、荨麻疹及坏疽性脓皮病等疾病有关,但目前相关发病机制尚不清楚[13]。
1.5 肠道病毒
肠道病毒(enterovirus)可引起手足口病(hand,foot and mouth disease,HFMD),主 要 表 现 为 发热、乏力及皮损等症状,其中以柯萨奇病毒A-16(coxsackievirus-A16,CV-A16)与肠道病毒71型最常见。HFMD平均潜伏期3~5 d,一般1周内痊愈。典型皮损为掌跖、口腔黏膜、臀部等部位出现红色至暗红色斑丘疹、疱疹,疱内少量浑浊液体,米粒至豆粒大小,周围有红晕,不痛不痒,皮损消退后无结痂或色素改变。肠道病毒感染人体后,与咽部、肠道上皮细胞表面病毒受体相结合,随后病毒复制并释放入血,播散到皮肤及黏膜而引起皮损[14]。而CV-A6、CV-A10血清型所引起的HFMD皮损不典型,皮损广泛且严重,可累及躯干、口周及四肢,可为紫癜、瘀斑,甚至是大疱或指甲脱落,伴有明显瘙痒,消退期可出现脱屑、色素沉着等。然而目前针对脱甲的机制尚不明确,可能与大量病毒复制导致甲基质的破坏有关[15]。肠道病毒导致HFMD时可合并多形红斑,考虑可能是肠道病毒感染后机体出现免疫复合物介导的血管炎性反应,导致血管壁的通透性增高,引起相应症状[16]。
2 反义单链RNA病毒
2.1 甲型流感病毒
甲型流感病毒(influenza A)可导致甲型流行性感冒(甲流),主要表现为发热、头痛、肌痛及全身不适。但皮损并非甲流的常见临床表现,仅见于2%的甲流患者,且通常为儿童。相关皮损常表现为粉红至暗红色斑疹、斑丘疹及紫癜,可局限于躯干部位或泛发全身,可伴或不伴痒感,痊愈后皮损可完全消退[17]。有报道甲流与过敏性紫癜及川崎病相关,其中血管炎症表现考虑与淋巴细胞亚群异常或病毒感染导致细胞因子失衡相关,特别是Th1及Th17细胞及其细胞因子[18,19]。也有报道甲流与伴发嗜酸粒细胞增多及系统症状的药疹综合征(drug rash with eosinophilia and systemic symptoms,DRESS)、Gianotti-Crosti综合征(Gianotti-Crosti syndrome,GCS)等相关,但相关机制尚不清楚[20,21]。
2.2 埃博拉病毒
埃博拉病毒(ebola virus)可导致埃博拉出血热,患者常在发热后第4~6 d出现特征性麻疹样皮损、斑丘疹,呈暗红色,主要分布在双侧上肢的近端屈侧以及双侧大腿处或头部,随后全身泛发,局部融合成片。皮损在数天至 2 周内消退并脱屑,且以掌跖部位为主,部分患者的皮损可长期遗留色素沉着。其他皮肤表现包括紫癜、瘀斑和眼睛、口咽部的黏膜病变[22]。重症患者可见皮肤瘀斑、皮下血肿及结膜出血等出血表现。皮损相关机制可能是病毒在局部淋巴结及全身淋巴系统增殖、刺激机体产生及释放大量细胞因子及趋化因子,从而导致血管内皮通透性增加,最后引起弥散性血管内凝血[10]。但皮损改变可能是非特征性皮肤变化,不可作为疾病诊断标准及临床判断病情及治疗效果的依据[23]。
2.3 麻疹病毒
麻疹病毒(measles virus)可引起麻疹,主要表现为发热、呼吸道症状、眼结合膜炎及典型皮肤黏膜损害,可伴发肺炎、亚急性硬化性全脑炎等并发症[24]。麻疹黏膜斑(Koplik斑)是麻疹早期特征性表现,多在发疹前1~2 d出现,位于第二磨牙对面的颊黏膜上,直径为0.5~1 mm的灰白色小点,周围有红晕,可增多后融合成片,在发疹后第2天消退。发热2~4 d开始出现典型皮损,先出现于耳后、发际、面部,随后蔓延至躯干和四肢。为玫瑰色斑丘疹,压之褪色,可相互融合,疹间皮肤正常。出疹后3~5 d内皮损按出疹顺序逐渐消退,消退后留有褐色色素沉着及细小糠样脱屑。皮肤黏膜损害与毛细血管内病毒抗原堆积及细胞介导的抗病毒免疫反应相关,因此细胞免疫受损的患者可能不会出现或延迟出现特征性皮损[25]。
3 双链RNA病毒
3.1 轮状病毒
轮状病毒(rotavirus)可引起轮状病毒肠炎,常见症状为腹泻、呕吐及发热,也可引起心、肝、脑、肾等肠道外多系统功能损害,严重可致死[26]。有报道婴儿出现轮状病毒肠炎合并Sweet综合征,考虑与轮状病毒感染后诱导机体产生促炎因子,特别是白细胞介素-1、粒细胞集落刺激因子、粒细胞-巨噬细胞集落刺激因子及α干扰素进而介导和调节免疫有关[27]。轮状病毒可引起过敏性紫癜,与轮状病毒作为抗原引起的变态反应相关[28]。成人轮状病毒感染后出现泛发斑丘疹,消退后伴头皮糠样脱屑,手足部出现手、袜套样脱屑;也有报道轮状病毒与GCS、婴儿急性出血性水肿等相关,但相关机制尚未明确[26]。
4 单链逆转录病毒
4.1 人免疫缺陷病毒
人免疫缺陷病毒(human immunodeficiency virus,HIV)急性期感染是指体内存在HIV病毒但抗体尚未阳转的阶段。急性期患者一般在感染后1~4周内出现症状,持续2~3周。常见症状包括发热、乏力、肌肉和关节疼痛、中枢神经系统异常及皮肤黏膜损害等[29]。急性期患者多在发热后2~3 d出现皮损,为数量不等的直径5~10 mm椭圆形或圆形粉红色至暗红色斑疹、斑丘疹,边界清晰,无瘙痒。主要分布在上胸部,尤其是领圈部位,也可见于头面部,四肢少见。一般持续5~8 d后逐渐好转。部分患者可在口腔黏膜、外阴等部位出现红斑、溃疡[30]。有研究推测急性期皮损与CD8+T淋巴细胞在局部皮损浸润或急性期患者的淋巴组织中的CD1a+树突状细胞产生增加并分泌炎性因子相关。此外,HIV病毒感染相关皮肤病还包括炎症性皮肤病、继发性感染性皮肤病及肿瘤等(表1)[31]。
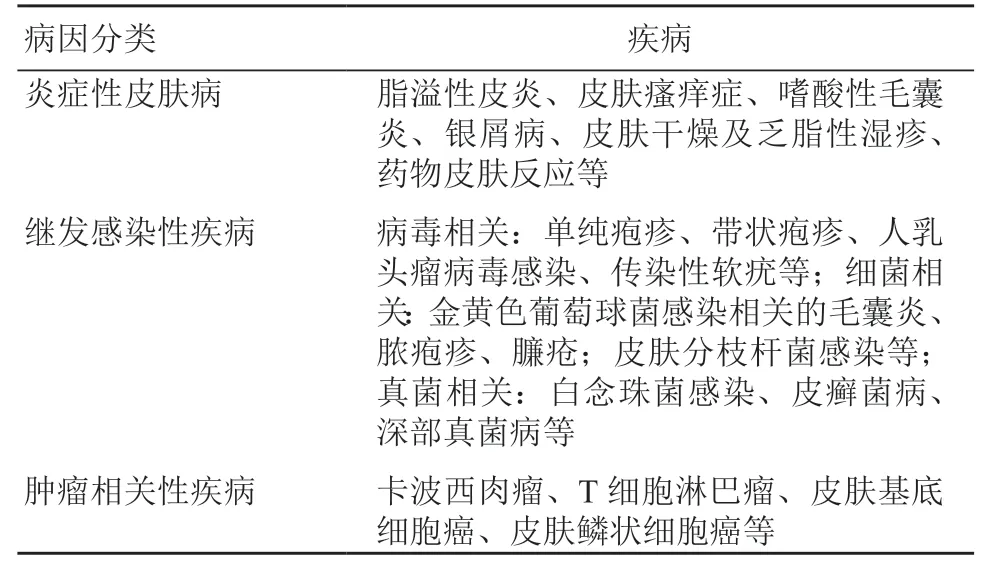
表1 HIV感染相关皮肤病
5 小结
综上所述,RNA病毒所致传染病相关皮肤黏膜损害表现多样,可伴有发热、瘙痒症状,需要与不同病原体所致的感染性疾病及非感染性疾病进行鉴别[4,11,17](表2)。如今大部分皮损形成机制未明确,多数发疹样皮肤表现与机体对病毒的高度敏感性相关[17],尚有待进一步研究。部分RNA病毒感染后首发的临床表现可仅有皮肤黏膜损害,对早期识别、诊断有较大的临床意义,可阻止疾病进展和限制疾病进一步传播。因此在临床工作中,需要皮肤科医生提高警惕性,拓展诊疗思路,需要详细询问现病史及体格检查,特别是流行病学史、药物使用史及皮损的表现及变化等,进一步提高对疾病的诊断和鉴别能力,避免误诊、误治。

表2 根据皮损表现的鉴别诊断

