外泌体miR-155通过调节SOCS1影响重症急性胰腺炎肺损伤
缪宝洲,汪敬恒,钟俊峰,潘恩,林秀丽
福建中医药大学附属福鼎市医院重症医学科,福建福鼎355200
急性胰腺炎(acute pancreatitis,AP)是ICU常见疾病,随着生活方式的改变,发病日趋年轻化[1-2]。重症急性胰腺炎(severe acute pancreatitis,SAP)患者伴有或者不伴有多脏器功能衰竭(mutiple organ failure,MOF),决定了其严重程度,尤其是急性肺损伤(acute lung injure,ALI)[3]和急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)[4]。外泌体排出细胞外并携带核酸传递信息,可穿透血管壁,同时可穿透细胞外基质[5],其中MicroRNA即为外面运输核酸之一,从而影响下游基因表达[6-7]。SAP-ALI的内皮细胞通透性发生改变,可能导致外泌体的分泌增多,携带MicroRNA增多[8]。
AP发生发展过程中,胰液的释放会导致胰腺自我消化[9],从而产生IL-17的CD4+T辅助细胞(Th17)的积聚[10]。文献中已经证实SOCS1调节STAT5,STAT5是Treg细胞的统计调节器[11]。Wang等[12]人研究发现,miR-155可以抑制SOCS1,从而影响AP的发生发展过程。设想miR-155通过外泌体包裹转运可以通过SOCS1影响SAP-ALI的过程。因此该文方便选取福建中医药大学附属福鼎医院重症医学科(ICU)2019年1—12月收治入院的128例急性胰腺炎患者血浆进行了相关研究,现报道如下。
1 材料与方法
1.1 材料
方便选取福建中医药大学附属福鼎医院重症医学科(ICU)收治入院的128例急性胰腺炎患者血浆,其中急性胰腺炎伴肺损伤(AP with ALI,AWA)35例,急性胰腺炎不伴肺损伤(AP without ALI,AOA)93例,采集8名非患者志愿者血浆,年龄39~53岁。根据伴有或者不伴有ALI将患者分成两组,AWA组35例,男女比例为17例∶18例,平均年龄为(48.6±16.1)岁;AOA组93例,男女比例为44例∶49例,平均年龄(45.6±16.5)岁。采集8名非患者志愿者血浆,平均年龄(46.3±4.17)岁。签署知情同意书后,经过福建中医药大学附属福鼎医院伦理委员会论证通过,伦理委员会批准文号:鼎医综〔2020〕124号。外泌体大体试剂盒:德国QIAGEN公司。
1.2 方法
1.2.1 标本采集因胰腺炎急诊入院的患者外周血3~5 mL,抗凝,至实验室离心,低速1 000 g,10 min。取上层血浆至1.5 m LEP管,分装做好标记,-80℃保存备用。
1.2.2 提取外泌体将标本从储存管中取出,用200 mL XBP缓冲液与血浆等体积混合,收集混合液体,注入exoEasy滤柱中离心。使用PexoEasy滤柱加入缓冲液后离心。在滤网膜上,室温孵育1 min。离心,5 000 g,5 min,备用。
1.2.3 提取RNA加入400 μl酸化酚氯仿,通过震荡方式进行混匀,时间30~60 s。混匀后加入20 μl外部参照cel-miR-39(5 pmol/L)。纯乙醇萃取离心结束。洗涤,离心条件为室温9 500 g,空转1 min后弃去收集管,用新的收集管将洗脱液预热至95℃。预热好洗脱液后加入滤膜中,根据上述条件再离心30 s,回收收集管内滤液。检测收集到的溶液。
1.2.4 进行miR-155的荧光定量检测 以U6为内参基因,U6及miR-155特 异 引 序 列 为,miR-155:Forward primer:5'-GCGAAAGCATTTGCCAAGAA-3',Reverse primer:5'-CATCACAGACCTGTTATTGC-3';内 参U6:Forward primer:5'-AGCGGGAAATCGTGCGTGACA-3',Reverse primer:5'-GTGGACTTGGGAGAGGACTGG-3'。
1.3 统计方法
采用SPSS 22.0统计学软件处理数据,PCR以celmiR-39作为外源性参照,miR-155相对表达量计算公式45-Ct=45-(CtmiR-155-CtmiR-39)。miR-155结果中,每个样本设置3个重复,取算术平均值。计量资料以(±s)表示,组间差异比较采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 外泌体鉴定
Western blot结果提示,β-actin未在外泌体检测出,外泌体未被污染;外泌体组,TSG101和CD81特异性标志物表达升高,外泌体分离成功,见图1A。用细胞摄取动态光散射分析,发现外泌体平均直径为(80.69±18.11)nm,同时证实外泌体具有膜结构呈囊泡状,见图1B。

图1 外泌体鉴定:A.western blot结果显示TSG101和CD81表达;B.外泌体的形态
2.2 3组血浆外泌体miR-155水平比较
AWA患者血浆外泌体miR-155的相对表达量为(15.11±2.18),AOA患者血浆外泌体miR-155的相对表达量为(10.64±1.65),非患者志愿者(NC)血浆外泌体miR-155的相对表达量为(5.19±0.44)。AOA组血浆外泌体miR-155水平显著高于健康志愿者(P<0.01);AWA组血浆外泌体miR-155水平显著高于AOA组,差异有统计学意义(P<0.01),见图2。
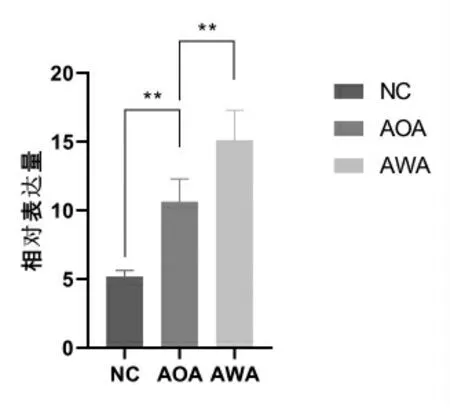
图2 外泌体miR-155在AWA患者血浆中的表达情况
2.3 miR-155直接靶点SOCS1的确定
为了研究miR-155的潜在靶基因,利用targetscan软件进行了生物信息学分析。使用这种方法,在3’-UTR的SOCS1 mRNA中预测miR-155结合位点,见图3A。为了检测miR-155对SOCS1的调节作用,对CD4+T细胞进行了双荧光素酶报告试验。细胞共转染了野生型(WT)或突变型(MUT)SOCS13’-UTR质粒和miR-155或对照miR转染。MiR-155显著抑制WT的荧光素酶报告活性,与对照组相比,差异有统计学意义(P<0.01),但不抑制MUT-SOCS13’-UTR,表明SOCS1是MiR-155的直接靶点(图3B)。RT-PCR分析miR-155转染细胞中的SOCS1,证实miRNA下调了CD4+T细胞中SOCS1的表达,差异有统计学意义(P<0.01),见图3,用miR-155抑制剂处理细胞可逆转这种作用,差异有统计学意义(P<0.01),见图3C。

图3 miR-155直接靶点SOCS1的确定。A.miR-155和SOCS1 mRNA的序列匹配;B.WT或MUT SOCS1 3’-UTR与miR-155或对照miR共转染的荧光素酶检测报告;C.转染后3天CD4+T细胞SOCS1的Rt-PCR分析
2.4 3组血浆CD4+T细胞中SOCS1表达情况比较
为探讨miR-155对AP和ALI的作用机制,进一步研究了不同分组中CD4+T细胞的SOCS1的表达情况。研究结果发现,AWA组较AOA组,SOCS1在蛋白和mRNA水平均明显降低,差异有统计学意义(P<0.05)。AOA组较正常组,SOCS1在蛋白和mRNA水平也均明显降低,差异有统计学意义(P<0.05)。见图4。

图4 western blot实验和实时定量PCR实验
3 讨论
目前AP的诊断包括两个方面,临床表现和实验室检查,但尚无准确预测AP严重程度的标志物,此标志物需要时间准确性,即必须在早期发现并准确预测。miR-155参与了多种疾病的发生发展[13],在某些胰腺疾病中,如星状细胞通过相关机制转化时,miR-155表达下调[14]。该课题依据以上调查基础,采集AP患者血浆并分离纯化鉴定血浆外泌体,研究发现外泌体miR-155在AWA患者血浆中显著高表达,AWA患者相对表达量为(15.11±2.18),AOA患者相对表达量为(10.64±1.65),NC组相对表达量为(5.19±0.44)。AWA组血浆外泌体miR-155水平是AOA组的1.5倍,是NC组的3倍,这从侧面提示miR-155可能以外泌体形式存在于血浆中,并与AP的病情发展有一定的关系。Jiménez等[15]人发现,AP能够产生2个不同的外泌体群,它们在细胞分布、蛋白质和miRNA含量上存在相应的差异,并且可以产生不同的生理效应。其中一个即miR-155明显升高为特点,且miR-21和miR-122降低,其中AP组外泌体miR-155是对照组的4倍,而该文结果中AWA是NC组的3倍,结果相近,与该研究结果相符。说明外泌体miRNA的异常表达,会对疾病产生较大影响,结果显示,miR-155在AWA患者血浆外泌体中高表达。
那么外泌体miR-155通过什么途径对AP的严重程度发挥作用?有研究显示,miR-155可通过靶向结合SOCS1发挥抗肿瘤作用,Zhang等[16]发现,miR-155通过直接靶向SOCS1促进间变性甲状腺癌的进展,其研究结果表明,荧光素酶实验验证了miR-155和SOCS1的靶向结合作用,同时能够抑制甲状腺癌细胞中SOCS1的表达,降低其表达后从而造成肿瘤进展。该研究进一步研究了miR-155与SOCS1的关系,利用targetscan软件进行了生物信息学分析。使用这种方法,在3’-UTR的SOCS1 mRNA中预测miR-155结合位点(图3A)。为了检测miR-155对SOCS1的调节作用,对CD4+T细胞进行了双荧光素酶报告试验,结果发现miR-155通过抑制性结合SOCS1 mRNA达到抑制其表达(图3C),对照组明显高于miR-155组,约为3倍,得到了与Zhang等人的研究类似的结果。同时进行不同分组之间SOCS1的表达情况分析,结果发现,AWA组较AOA组,SOCS1在蛋白和mRNA水平均明显降低(P<0.05),如图4所示。AOA组较NC组,SOCS1在蛋白和mRNA水平也均明显降低(P<0.05),与外泌体miR-155的表达呈负相关。通过以上结果,推论可以发现,SOCS1参与了AP的发生发展过程,外泌体miR-155通过抑制性结合SOCS1的3’TUR来抑制其表达,影响AP的病程进展。在Wang等[12]的研究中,在胰腺炎中已经证实miR-155可以靶向结合SOCS1并通过这一调节轴对Th17/Treg比率进行调节,SOCS1的表达情况与胰腺炎的严重程度相关,与该研究结果一致。综上所述,外泌体miR-155可以作为预测AP病程进展的标志物,值得进一步深入研究。
外泌体miRNA在近些年研究中呈现明显的应用优势,尤其在重症疾病中,包括胰腺炎、肿瘤、肾纤维化等方面。该研究确定了SOCS1是miR-155的直接靶向结合目标,外泌体源性miR-155在AWA患者血浆中高表达,其可通过调节SOCS1的表达影响重症急性胰腺炎肺损伤,为外泌体在重症胰腺炎方面的研究打下基础。但对其机制仍所知甚少,如外泌体源性miR-155如何发生上调,如何发生下调,是否可以确定界定值范围,来判断疾病进展情况,需要继续深入研究。
综上所述,外泌体源性miR-155的表达水平与重症胰腺炎患者的发病情况息息相关,使得它对于疾病的预后判断十分重要,有望成为诊断和提示预后的生物标志物。因此可进一步对miR-200c的发展潜力进行挖掘,从而更好的为临床服务。

