左心室辅助装置的临床应用现状和展望
张帅综述,侯剑峰审校
在慢性收缩性心力衰竭的治疗上,尽管目前取得了长足进展,但仍然需要更先进的方法来治疗和管理终末期心力衰竭。2009~2016年,我国28 家心脏移植中心共上报2 149例心脏移植数据[1],这仅仅是我国等待心脏移植的终末期心力衰竭患者中的很少一部分。另外,有相关研究表明,我国心力衰竭患者的总体疾病认知程度较差[2]。左心室辅助装置(LVAD)的应用为这些短期死亡率高又不能及时进行心脏移植的患者带来了福音。但是,目前LVAD还不能作为心脏移植的替代治疗。未来LVAD 的研发应该提高其生物相容性,以减少植入后不良事件的发生[3]。
1 左心室辅助装置的原理和发展
LVAD 的基本原理是通过左心室心尖插管将血液引出,在LVAD 血泵提供的动力下,将血液通过主动脉插管输送至主动脉,通过以上的辅助循环来减轻左心室负荷。LVAD 发展至今,已有三代产品应用于临床。
第一代LVAD 即搏动式隔膜泵,它的核心结构是一个柔韧性材料的囊腔,囊腔的一侧是隔膜,囊腔两端连接进、出导管,并在两接口处分别放置单向阀门,以保证血液单向流动;驱动装置通过气体或液体对隔膜施加外力以产生搏动,造成腔内压力的顺序性变化,完成泵血功能;其结构复杂,体积大,不能完全植入体内,经皮肤进出身体的导线管道易发生感染;其单向阀门易损耗,并且易在此处形成血栓,耐久性差,现已很少应用于成人心室辅助。目前仍然应用于临床的搏动泵例如,Berlin EXCOR(Berlin Heart,德国)主要适用于儿科患者等待心脏移植的过渡期。
第二代LVAD 即恒流泵,为连续流叶轮血泵,此类血泵的叶片通过机械轴承安装在血泵转子上,转子带动叶片旋转,从而推动血液沿螺旋线方向前向运动。恒流泵进一步可分为轴流泵和离心泵。目前在临床上应用的主要是HeartMate Ⅱ(Abbott,美国)、MicroMed DeBakey VAD(MicroMed Cardiovascular,美国)等轴流泵。轴流泵由于自身体积小,叶轮需以7 000~12 000 转/min 的速度旋转才能产生足够的推力,由此带来的剪切力是造成溶血和血管性血友病因子断裂的主要原因[4]。尽管如此,轴流泵具有体积小、结构相对简单、与血液的接触面积小等优点,目前正成为心脏移植前过渡支持治疗和终生治疗的主流心室辅助装置类型。
第三代LVAD 以悬浮技术为特点,因此凡采用磁悬浮和(或)液力悬浮技术研发的LVAD 均可称为第三代LVAD,其一般具有悬浮和驱动两个系统,以离心泵为主,由于不存在轴承,降低了传统上轴承的磨损、发热以及轴承密封处血栓的发生率。其中,HeartWare HVAD(Medtronic,美国)是以磁悬浮和液力悬浮为设计特点的离心泵,是第一个可完全放置在心包腔内而不需要腹膜外泵袋的LVAD。HeartMate Ⅲ(Abbott,美国)是以全磁悬浮为设计特点的新型第三代LVAD,具有更好的生物相容性,植入后不良事件的发生率更小[5]。迄今为止,鲜有HeartMate Ⅲ发生泵内血栓的病例报道。
2 左心室辅助装置的临床应用及植入后收益
不同类别的LVAD 具有不同的植入适应证、内部结构以及泵血方式,对于非住院患者的长期机械循环辅助,有以下两个指征[6]:(1)作为药物治疗不能控制的终末期心力衰竭患者进行心脏移植前的过渡治疗,直至获得供体器官;(2)作为因并发症或年龄过大而不能进行心脏移植的终末期收缩性心力衰竭患者的终生治疗。
由于病情会随时发生恶化或者好转,因此LVAD 作为过渡治疗还是终生治疗,要依据病情变化以及植入后的情况而定。LVAD 植入后往往短时间内即可改善患者的血流动力学,包括增加心输出量、降低心室充盈压、降低肺动脉压以及肺血管阻力[7]。但是部分患者LVAD 植入术后会经历不同程度的抑郁、焦虑、认知障碍和睡眠障碍,影响患者的生活质量[8]。
3 左心室辅助装置植入后血流动力学评估及调节
虽然离心泵和轴流泵泵血的机制不同,但是它们的血流动力学效应可采用一致的原则进行评估。心室压力容积曲线可以很好地评估不同泵速所产生的血流压力,并评估对心室的持续性卸负荷效应[9]。但由于是一种侵入性比较大的操作,实际应用并不广泛。目前临床上通常使用超声心动图斜坡试验来调定恒流泵泵速以达到最佳的血流动力学状态(使肺毛细血管楔压<15 mmHg,1 mmHg=0.133 kPa)[10]。
4 左心室辅助装置植入后抗凝及抗血小板治疗
4.1 术后抗凝及抗血小板治疗
LVAD 植入术后1 d 如无明显出血,即开始普通肝素治疗,并逐渐延长活化部分凝血活酶时间,术后24~72 h 内开始应用阿司匹林,使患者的国际标准化比值(INR)达到设备所要求的目标值[11]。尽管推荐使用普通肝素作为患者服用华法林前的过渡治疗,但是在HeartMate Ⅱ临床研究中,约有29%的患者未使用肝素作为过渡;与使用肝素的患者相比,未使用肝素的患者因出血而输血的比例降低50%[12]。而且有研究显示,未使用肝素作为桥接的患者,脑卒中发生率下降[13],因此HeartMate Ⅱ植入术后是否应采用肝素作为桥接治疗存在争议。一项针对LVAD 植入后脑血管并发症的Meta 分析显示,长期应用抗血小板药物可降低脑卒中发生率[13]。专家共识推荐使用阿司匹林(81~325 mg/d)进行长期抗血小板治疗,另可根据相应植入设备厂商的推荐,在此基础上添加其他抗血小板药物,例如双嘧达莫、氯吡格雷等[11]。
4.2 长期抗凝管理
指南推荐使用维生素K 拮抗剂(VKA)作为LVAD 植入后的长期抗凝药物,使患者的INR 长期维持在植入设备所要求的目标范围内。VKA 治疗的个体差异较大,INR 在治疗范围内的时间(TTR)只有31%~51%。患者自测凝血功能会提高其TTR,但是尚不清楚这是否会影响患者的预后[14]。LVAD 植入后患者不仅需要长期抗凝,而且应该加强抗凝药物的日常管理。
5 左心室辅助装置植入后相关不良事件及处理措施
国际机械循环辅助协会的报告显示,血泵植入1年内常见的不良事件发生率从高到低依次为出血、感染、心律失常、呼吸衰竭以及脑血管意外[15]。不良事件可以分成以下三类[16]:(1)血泵及其附属结构相关并发症,例如血泵功能不全、控制器故障等;(2)患者自身心脏相关并发症,例如心律失常、瓣膜反流等;(3)血泵-患者接触面相关并发症,例如感染、脑血管意外、泵内血栓等。LVAD 设计和后期药物管理的主要目的在于降低第三类不良事件的发生率。
5.1 出血
LVAD 植入后最常见的不良事件为出血,主要是由于凝血系统中凝血蛋白、血小板、血管性血友病因子异常所导致。有学者指出,患者植入LVAD后乳酸脱氢酶水平> 500 IU/L 且持续增高、无下降趋势,高度提示存在出血事件[17]。LVAD 植入后2周内由于内源性凝血途径激活,导致内源性凝血途径相关因子(Ⅻ因子、Ⅺ因子、缓激肽释放酶原)的消耗[18]。同时,血浆组织因子、E-选择素以及循环内皮细胞表面黏附因子表达水平升高,表明LVAD植入可导致内皮细胞激活,启动外源性凝血途径[19]。内、外源性凝血途径的激活导致凝血因子大量消耗,因此患者在术后容易引发出血。
除了凝血因子的消耗,LVAD 植入后患者常因大量丢失血管性血友病因子多聚体而罹患获得性血管性血友病[20]。此类凝血障碍会加重鼻黏膜和胃肠道黏膜的动静脉畸形出血。目前尚未完全明确动静脉畸形的发生机制,但认为微血管水平上缺少搏动性血流以及氧化应激与之相关[21]。针对以上出血并发症,相关管理指南指出,术后应暂缓并逐渐恢复抗凝治疗[11]。对于出血所引起的贫血,可予以红细胞输注,但须权衡患者将来心脏移植后发生同种异体免疫排斥反应的风险。对于严重的胃肠道出血,推荐使用内镜评估检查并予以局部止血治疗[22]。
5.2 感染
血泵相关感染十分常见,并且与不良预后相关。大部分的感染始于经皮导线进出体内部分的浅层组织,但是可以迁延数月进展为深层组织感染[23]。现在认为,血泵相关感染引起的败血症是导致远期死亡的主要原因,导线周围组织感染诊断后6 个月和12个月内,败血症发生率大约分别为8%和18%[15,24]。虽然血行感染可导致患者死亡,但感染患者若能及时接受心脏移植,临床预后与大部分移植患者仍然相似[25]。目前,关于预防LVAD 植入后感染的推荐治疗策略大多来自于专家意见,因此很难寻找出具有最佳证据的治疗方案。
5.3 脑血管意外
LVAD 植入后脑血管意外(缺血性或出血性脑卒中)的发生会导致严重的不良结局,包括残疾、自主能力丧失甚至死亡,发生率约为0.19/人年。相对而言,缺血性脑卒中的发生率较高,但出血性脑卒中的致残率或致死率更高[15]。因出血而暂时停用抗凝药物,会增加缺血性脑卒中的发生风险,即使两种事件的发生间隔长达4 个月[26]。一项针对HeartWare HVAD 植入后发生脑血管意外的风险因素评估研究显示,平均动脉压>90 mmHg、INR >3.0 以及阿司匹林剂量<81 mg/d 会增加出血性脑血管意外的发生风险,而降低平均动脉压不仅可减少出血性脑卒中发生率,同时不会增加缺血性脑卒中的发生率[27]。
5.4 右心衰竭
大多数终末期心力衰竭患者存在不同程度的右心衰竭,但是严重的右心功能不全是LVAD 终身治疗的禁忌证,因为10%~40%的LVAD 植入后患者早期会出现急性右心衰竭,从而延长患者的住院时间并增加围术期死亡率[28]。另外,LVAD 植入后迟发型右心衰竭已成为难以治疗的临床难题,影响患者的生存率和生存质量。未来可以利用相应的参数建立完整的右心衰竭风险模型,并以此筛选出术后右心衰竭发生风险较高的患者,从而进一步筛选出LVAD 的最佳适应人群。
6 我国左心室辅助装置研究进展
我国LVAD 的研究开展相对较早。1965年上海第二医学院研发出我国首个心室辅助装置。1978年,我国召开的第一次人工心脏会议推动了心室辅助治疗的研究发展。我国主要LVAD 的研发进展见表1。
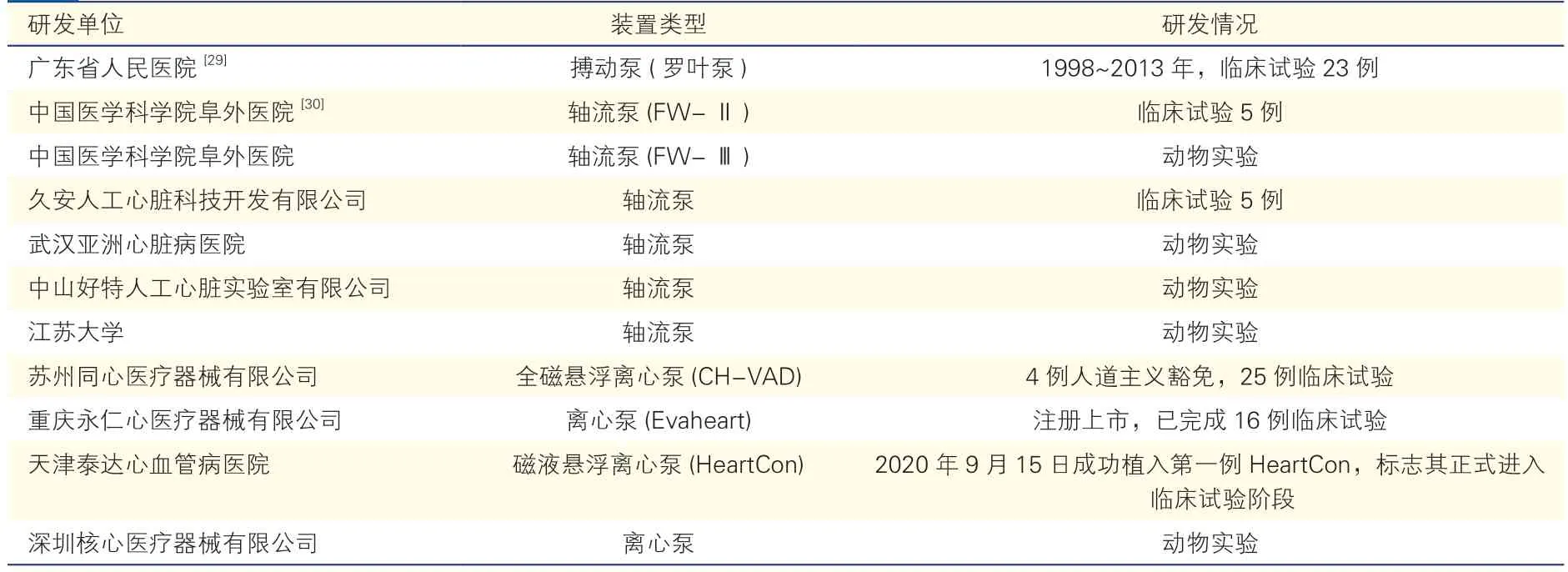
表1 我国左心室辅助装置的研发进展
7 展望
在LVAD 成为心脏移植的替代治疗之前,必须要克服以上主要不良事件的发生,使之可以长期稳定地进行辅助循环;而且在降低不良事件发生率的基础上,应做到体积更小、耐久性更好、可完全植入(无线电能传输)、反馈机体的生理需要并自动调节泵速,以满足患者的日常生活需要,使患者的生活质量进一步提升。近年来,我国LVAD 的研发取得了突破性进展,其有效性及安全性也在临床试验中得到证明。鉴于我国存在的庞大心力衰竭人群,在心脏移植供体稀缺的情况下,LVAD 作为终末期心力衰竭患者的有效治疗手段,其国产化可降低医疗费用。未来我国LVAD 的发展还要着重于跨学科团队的积极合作,促进产、学、研一体化深度融合,继续向高端医疗器械领域前进。
利益冲突:所有作者均声明不存在利益冲突

