伴高尿酸血症突发性聋患者的临床特征及预后*
蒋远伟 蔡志福 戴惠婷 林超凡 潘金霞
突聋的发病机制至今尚未明确,既往大多数研究认为该病的发生可能与感染、微循环障碍、免疫应激和遗传等因素有关[1,2]。近年来,随着基础代谢性疾病的发病率逐年上升,越来越多的研究者关注到高血压、糖尿病、高脂血症和代谢综合征等血管危险因素疾病在突聋的发生及发展中具有重要作用[3~5]。高尿酸血症是一组嘌呤代谢紊乱所致的疾病,其临床特点为血尿酸浓度升高及由此而引起的痛风性急性关节炎反复发作、慢性关节炎和关节畸形、慢性间质性肾炎和尿酸肾结石等并发症[6]。较高浓度的尿酸也可损伤听觉系统,促进慢性感音神经性聋,尤其是老年性聋的发生及发展[7]。然而,既往较少有研究探讨高尿酸血症对突聋的影响,对该类患者的临床特征及预后认识也相对不足。本研究旨在分析近5年来诊治的突聋伴高尿酸血症患者的临床特征及预后,现报告如下。
1 资料与方法
1.1研究对象及分组 选取 2016年1月到2020年12月在莆田学院附属医院耳鼻咽喉科诊治的64例(68耳)伴高尿酸血症突聋患者(高尿酸血症组)为研究对象,年龄29~68岁,中位年龄47岁,其中男44例,女20例。以同时期年龄和性别匹配的430例(445耳)未合并高尿酸血症的突聋患者(非高尿酸血症组)作为对照组,年龄27~65岁,中位年龄45岁,其中男249例,女181例。所有纳入的突聋患者均符合以下标准:符合2015年突发性聋诊断和治疗指南的诊断标准;有完整的临床资料和预后随访资料;年龄>18岁;无耳聋家族史;辅助检查排除外伤、耳部和头部器质性病变等明确病因导致的听力下降;根据高尿酸血症患者是否合并痛风,将高尿酸血症组进一步分为痛风组(22例,25耳)和非痛风组(42例,43耳)。
1.2高尿酸血症及痛风诊断 高尿酸血症的诊断参照中华医学会内分泌学分会最新建议的标准[8]:非同日2 次空腹血尿酸水平超过420 μmol/L,无论男性还是女性。痛风的诊断参照2015 年美国风湿病协会/欧洲抗风湿病联盟推荐的标准[9]:在有症状的关节或者滑膜液中发现尿酸钠结石或者出现痛风石,并且对临床表现、实验室及影像学检查结果相应赋分后,累积积分≥8分。
1.3突聋治疗方法 所有患者入院后根据指南推荐方案均予以常规的综合治疗,包括:甲泼尼龙40 mg,晨起顿服,连用3天,如有效再用2天后停药;银杏叶提取物注射液105 mg+生理盐水250 ml静脉滴注,每日1次,共计10天;甲钴胺片0.5 mg口服,每日3次,共计10天;平坦型和全聋型患者加用巴曲酶注射液,首次10 BU+250 ml 生理盐水静脉滴注,随后5 BU+100 ml 生理盐水静脉滴注,隔日1次,连用5次。所有合并高尿酸血症的患者,请内分泌科医生会诊协助诊治,对于无症状高尿酸血症患者予以别嘌醇口服(治疗前进行HLA-B 5801基因检测,并严格评估肾功能),肾功能正常及慢性肾病(chronic kidney disease,CKD)1-2期的患者起始剂量为100 mg/d,每2~4周增加100 mg/d,最大剂量800 mg/d;CKD3-4期的患者起始剂量为50 mg/d,每2~4周增加50 mg/d,最大剂量200 mg/d;CKD5期患者禁用。对于别嘌醇禁忌的患者,改用非布司他口服,初始剂量为20 mg/d,每2~4周可增加20 mg/d,最大剂量80 mg/d(CKD4~5期患者最大剂量不超过40 mg/d),尿酸控制目标为<420 μmol/L,伴有合并症控制目标<360 μmol/L。对于同时合并痛风的患者或尿酸波动较大的患者可酌情加用小剂量秋水仙碱口服,0.5~1.0 mg/d,维持3~6个月。降尿酸期间定期复查尿酸浓度并根据尿酸水平适当调整用药。激素治疗期间,严格监测血糖、血压及尿酸浓度,指标波动较大或难以控制的患者,立即停用全身激素治疗,改用鼓室给药治疗。
1.4听力损失程度及预后评估 所有患者在治疗前均进行纯音听阈检测,基于患者受损频率的听阈值,计算多个受损频率的均值,进而评估患者的初诊听阈值、听力损失程度分级和听阈曲线类型。所有患者治疗3~4天后复查听力,评估治疗效果,出院时及治疗结束3个月后再次复查纯音听阈,以结束3个月后纯音听阈结果作为最终疗效评估依据。参照2015年突发性聋诊断和治疗指南进行疗效判定,并根据受损频率听力平均提高值将患者分为痊愈、显效、有效和无效四个等级,痊愈、显效及有效三者之和为总有效。
1.5统计学方法 所有统计学分析均在SPSS23.0软件上完成,记录并比较各组性别、年龄、耳侧、双耳发病数、突聋病程、初诊听阈值、耳鸣和眩晕伴发率、高血压及糖尿病伴发率、听力损失程度、听阈曲线类型、听力预后、高尿酸血症病程及并发症情况。计量资料组间比较采用t检验;计数资料组间比较采用卡方检验;P<0.05为差异有统计学意义。
2 结果
2.1高尿酸血症组和非高尿酸血症组临床特征及预后比较 由表1可见,在高尿酸血症组中,患者的初诊听阈值、高血压和糖尿病伴发率、极重度聋和全聋型听阈曲线者所占比例分别为60.22±17.58 dB HL、26.56%、23.43%、36.76%和41.18%,均高于非高尿酸血症组(分别为52.31±13.45 dB HL、14.19%、12.32%、22.70%和27.42%),两组比较差异有统计学意义(均为P<0.05), 而两组间的性别、年龄、耳侧、双耳发病比例、突聋病程、耳鸣及眩晕伴发率差异均无统计学意义(P>0.05)。治疗结束3月后,高尿酸血症组的痊愈率和总有效率分别为13.23%和58.82%,低于非高尿酸血症组(分别为28.76%和73.71%),而无效率为41.18%,高于非高尿酸血症组(26.29%),差异均有统计学意义(均为P<0.05),两组间的显效率和有效率无统计学差异(P>0.05)(表2)。
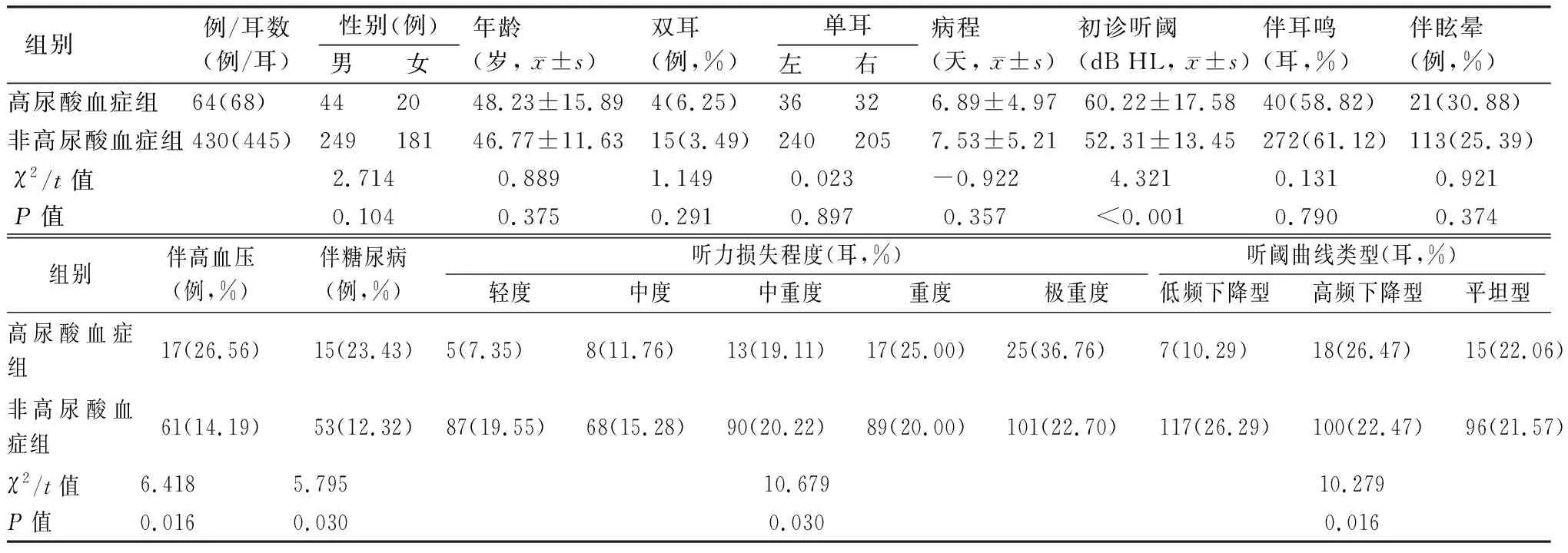
表1 高尿酸血症与非高尿酸血症突聋患者的临床资料比较
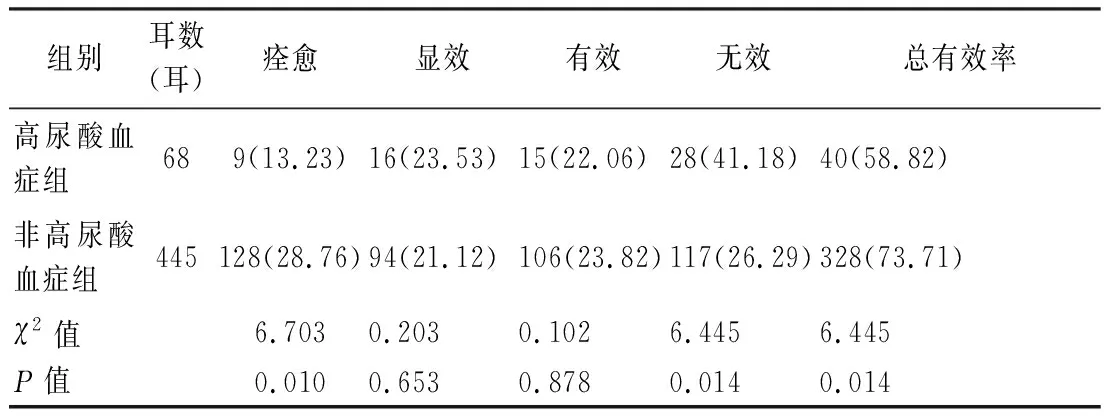
表2 两组患者治疗结束3月后的听力疗效比较(耳,%)
2.2痛风组和非痛风组患者的临床特征及预后比较 由表3可见,痛风组中患者的初诊听阈值和高尿酸血症病程为68.80±21.30 dB HL和60.73±25.42月,高于非痛风组(分别为53.14±15.63 dB HL和49.81±19.63月),差异有统计学意义(P<0.05);两组间患者的听阈曲线类型分布差异有统计学意义(P<0.05),而性别、年龄、耳侧、双耳发病比例、突聋病程、耳鸣及眩晕伴发率、高血压和糖尿病伴发率和听力损失程度差异均无统计学意义(P>0.05)。治疗结束3月后评估患者听力疗效,痛风组患者总有效率为36.00%,低于非痛风组(67.44%)(P<0.05),而两组的痊愈率、显效率和有效率差异均无统计学意义(P>0.05)(表4)。
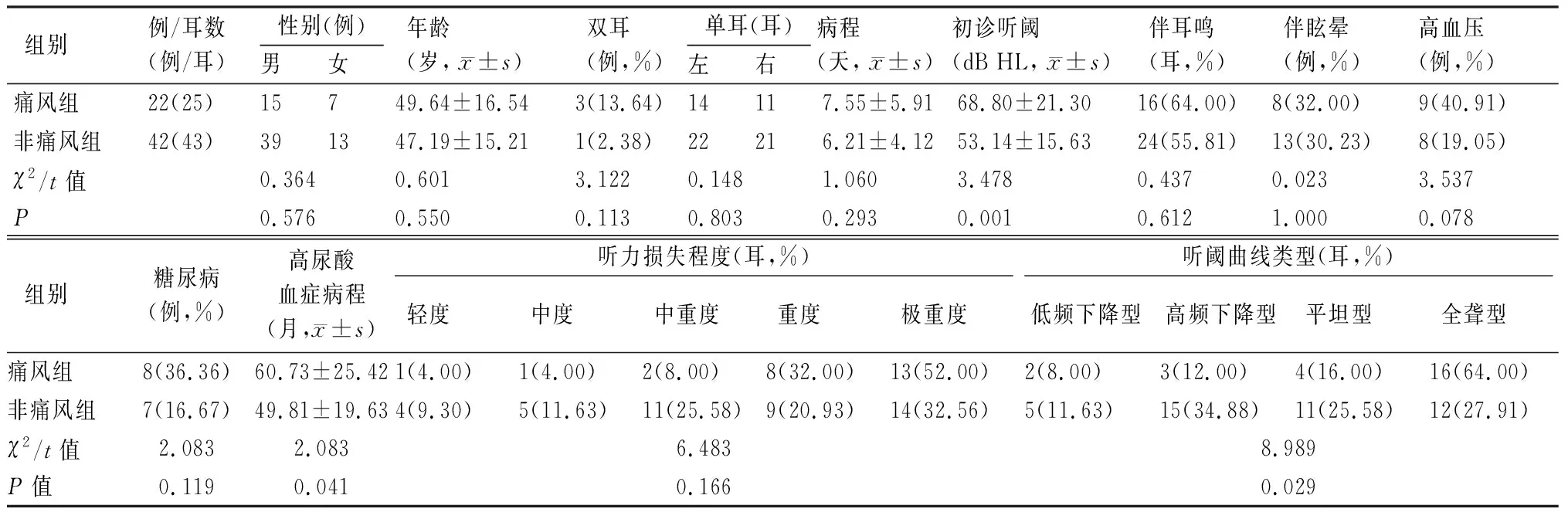
表3 痛风及非痛风突聋患者的临床资料比较
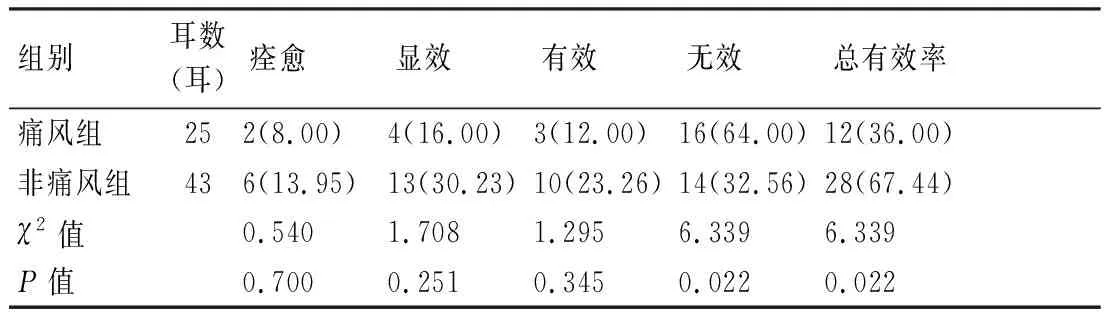
表4 痛风组与非痛风组治疗结束3月后听力疗效比较(耳,%)
3 讨论
高尿酸血症参与突聋发病的机制尚不明确,有研究推测可能与高浓度的尿酸介导的内耳供血动脉损伤有关[10]。既往研究证明高尿酸血症是糖尿病、慢性肾脏疾病、心血管疾病和脑卒中等疾病的独立危险因素[8]。Fasano等[11]对比分析突聋患者和正常对照者的血生化指标,发现突聋患者尿酸浓度明显升高,因此推测高浓度的尿酸可作为血管危险因素参与突聋的发生。Ilancioglu等[12]发现突聋患者和正常对照组的血清尿酸浓度无明显差异,且较高浓度的尿酸有利于突聋的预后,然而,由于该研究的样本量较少,使其结论可靠性不足。在另一项研究中,研究者则认为尿酸对突聋预后的影响具有两面性,较低浓度的尿酸可发挥其抗氧化作用进而促进突聋的听力恢复,而较高浓度的尿酸却能促进炎症反应及微血管损伤,不利于突聋的听力预后[10]。本研究共纳入64例伴高尿酸血症突聋患者,样本量相对较大,文中结果显示伴高尿酸血症突聋患者的听力损伤程度较重,全聋型所占比例较高,治疗预后较差;分析其可能的原因为机体内尿酸浓度长期保持高水平状态,可促进尿酸晶体析出,部分可沉积于内耳供血动脉内壁,诱导内皮细胞向间质细胞转化,导致血管功能障碍;高浓度的尿酸可诱导血小板向血管壁迁移和粘附,促进脂质过氧化并向血管内皮沉积,导致血管内皮细胞的氧化损伤,加剧血管动脉粥样硬化的进程;此外,高浓度的尿酸还能通过多种信号通路诱导单核-巨噬细胞的活化增殖并向血管内皮浸润,引发血管内皮的炎症反应,促进动脉粥样硬化的发生[13,14]。上述病理过程均可能导致内耳迷路动脉微血管病变,管壁增厚及管腔狭窄,严重干扰内耳的正常血供;且内耳属于高代谢器官,对缺血缺氧的耐受性极差,一旦迷路动脉发生痉挛或血管事件,势必导致内耳的血供急剧减少,导致严重的听力损伤。此外,迷路动脉狭窄甚至闭塞,经全身给药的药物不能有效到达内耳发挥治疗效能,因此,损伤的毛细胞不能得到及时有效的修复,患者听力预后差。
高尿酸血症患者由于长期尿酸浓度不能有效控制,可逐渐出现痛风等并发症[8],痛风患者血液中大量析出的尿酸晶体不仅可以给关节带来严重的慢性炎性损伤,也可不同程度地损伤其他组织和器官,包括内耳[15]。长期血尿酸浓度波动,大量血液中析出的尿酸晶体严重影响动脉血管内皮细胞功能,导致血管病变狭窄(尤其是微血管),患者发生血管事件的风险急剧增加[16]。近期流行病学调查报道痛风患者发生听力损伤的风险明显高于正常人群,同时是老年性聋发病的独立危险因素[7]。在本组对象中,高尿酸血症并发痛风的突聋患者其听力损伤程度较重且全聋型比例更高,听力预后更差,分析认为可能与这类患者迷路动脉微血管病变和微血管事件发生有关,也表明内耳微循环障碍可能是该类突聋的发病机制。对于突聋合并高尿酸血症或痛风患者的治疗,目前尚无相关研究报道,前期有研究者通过长期随访高尿酸血症患者,发现通过改变生活方式和药物治疗有效控制尿酸浓度能显著降低动脉粥样硬化发生的几率,降低血管不良事件发生的风险[17];Singh 等[7]认为早期发现高尿酸血症,尤其是痛风患者,并有效控制尿酸浓度可降低尿酸代谢异常引起的氧化应激和慢性炎症反应,降低老年人群听力损伤发生的风险;因此,重视突聋患者的尿酸浓度变化,尤其是对其合并高尿酸血症及痛风的早期诊断,并通过健康教育、改变生活方式及药物治疗有效控制尿酸浓度,可能有利于该类患者的听力预后。
综上所述,伴高尿酸血症尤其合并痛风的突聋患者,其听力损伤程度重,听阈曲线以全聋型为主,患者治疗效果差;微血管病变可能是伴高尿酸血症突聋发病及预后不良的潜在机制。

