贫血对股腘动脉硬化闭塞症患者药物涂层球囊治疗后再狭窄的影响
潘 涛, 田诗云, 张 涛, 纪东华
股腘动脉缺血性疾病血管腔内治疗并发症发生率、死亡率低,恢复时间短,目前已成为患者首选治疗方法。经皮腔内血管成形术(PTA)提供了良好的近期效果,但12个月再狭窄率高达40%~50%[1-2]。金属裸支架解决了PTA术后回缩问题,但内膜增生导致术后12个月支架内再狭窄率仍高达20%~40%[2-3]。药物涂层球囊(drug-coated balloon,DCB)中抗细胞增殖药物紫杉醇可持续存在于血管壁中长达180 d并持续抑制内膜增生,从而提高远期通畅率[4-5]。许多临床前瞻性随机对照试验研究结果显示,DCB治疗股腘动脉狭窄闭塞性疾病与普通球囊血管成形术(plain old balloon angioplasty,POBA)与金属裸支架相比具有更高的远期通畅率、更低的靶病变血运重建(target lesion revascularization,TLR)率[2]。目前关于DCB治疗股腘动脉狭窄/闭塞病变预后的相关危险因素研究较少,贫血因素对DCB术后再狭窄研究鲜有报道。本研究通过回顾性分析DCB治疗股腘动脉硬化闭塞症(atherosclerotic occlusion,ASO)患者临床资料,探讨贫血与术后再狭窄的相关性。
1 材料与方法
1.1 一般资料
回顾性分析2017年1月至2018年12月大连医科大学附属第一医院采用DCB成功治疗的股腘动脉ASO患者临床资料,包括年龄、性别、心脑血管疾病、术前血红蛋白(Hb)、踝-肱指数(ABI)及Rutherford分级等。为单纯评价贫血对DCB术后再狭窄的影响,排除肾功能不全、肝硬化、血液系统疾病等因素造成的贫血及DCB术后应用补救支架患者。共纳入DCB治疗股腘动脉ASO患者91例,平均年龄(70.76±7.51)岁,其中男63例(69.2%),女28例(30.8%);病变长度平均(19.99±11.09)cm,61例(67.0%)为泛大西洋学会联盟(TASC)C/D级,37例(40.7%)累及腘动脉,10例(11.0%)重度钙化[6];术前ABI为0.39±0.25;36例(39.6%)为间歇性跛行(Rutherford 1~3级),55例(60.4%)为重症肢体缺血(crictial limb ischemia,CLI)(Rutherford 4~6级);术前贫血36例(39.6%),术前无贫血55例(60.4%),见表1。

表1 患者基本资料和病变特点
术前Hb定义为术前最后一次测得值。根据世界卫生组织对贫血的标准定义术前贫血(男性Hb<130 g/L,女性Hb<120 g/L)。根据Rutherford分级,分为间歇性跛行组(n=36,Rutherford 1~3级)和CLI组(n=55,Rutherford 4~6级)。
1.2 DCB治疗
术前完善腹主动脉和下肢动脉CTA,常规口服阿司匹林(100 mg/d)、氯吡格雷(75 mg/d)和西洛他唑(100 mg/d)治疗。术中静脉推注3 000~5 000 U普通肝素使全身肝素化,之后普通肝素1 000 U间隔1 h补充。
手术在局部麻醉下进行,根据靶动脉病变位置和特征确定同侧或对侧股动脉穿刺,同侧股动脉穿刺置入6~7 F短鞘(日本Terumo公司)或对侧股动脉逆穿刺翻山至患侧留置6~7 F长鞘(美国Cook公司);0.018或0.035英寸导丝配合CXI支撑导管(美国Cook公司)开通狭窄闭塞段;普通球囊预扩张,紫杉醇DCB(直径比目标动脉直径小1 mm,北京先瑞达医疗科技公司)扩张3 min(若需用另一DCB,至少重叠5 mm);膝下胫前动脉、腓动脉、胫后动脉至少开通一条流出道。
术后72 h内低分子肝素4 250 U间隔12 h皮下注射抗凝治疗,继续长期口服阿司匹林(100 mg/d)、西洛他唑(100 mg/d)和至少口服6个月氯吡格雷(75 mg/d)抗血小板集聚治疗。
1.3 随访
所有患者出院前复查ABI和靶血管多普勒超声,术后1、3、6、12个月进行临床随访和影像学检查。随访终点为12个月一期通畅率。一期通畅率定义为多普勒超声超声、动脉造影或CTA未发现靶病变治疗部位再狭窄(>50%)。
1.4 统计学方法
采用SPSS 24.0软件进行统计学分析。计量资料以均数±标准差(±s)表示,组间比较用t检验;计数资料以频数和构成比表示,用卡方检验和Fisher检验。Kaplan-Meier生存曲线分析12个月一期通畅率,两组生存曲线比较用Log-rank检验。多因素logistic回归法分析再狭窄危险因素。P<0.05为差异有统计学意义。
2 结果
91例患者术后临床症状明显好转,ABI为0.82±0.16(P<0.001),Rutherford分级明显改善(P<0.001)。贫血与无贫血组男性分别为23例与40例(P=0.375),贫血与非贫血组患者基本资料差异无统计学意义(P>0.05)(表1);36例贫血患者中轻度贫血34例(94.4%),中度贫血2例(5.6%),无重度贫血。
Kaplan-Meier生存曲线分析显示,12个月一期通畅率为80.2%(图1①)。共有18例患者发生再狭窄,其中贫血组12例(33.3%),无贫血组6例(10.9%),差异有显著统计学意义(P=0.009)。再狭窄组、无再狭窄组分别有贫血12例(66.7%)、24例(32.9%),差异有显著统计学意义(P=0.009)。再狭窄组患者与无再狭窄组患者相比病变钙化更严重(27.8%对6.8%,P=0.034),腘动脉易受累(61.1%对35.6%,P=0.049),Hb更低[(120.94±19.51)g/L对(134.48±16.28)g/L,P=0.003)],缺血症状更重(CLI 83.3%对54.8%,P=0.027)。12个月一期通畅率在重度钙化、无重度钙化患者分别为60.0%、82.7%(Log-rankP=0.073,图1②),贫血组患者(66.7%)显著低于无贫血组患者(89.1%)(Log-rankP=0.006,图1③),累及腘动脉患者(67.6%)低于未累及腘动脉患者(88.9%)(LogrankP=0.012,图1④),CLI组患者(70.9%)显著低于跛行组患者(94.4%)(Log-rankP=0.008,图1⑤)。多因素logistic回归分析显示,贫血(OR=5.297,95%CI=1.179~23.800,P=0.030)、重度钙化(OR=12.213,95%CI=1.806~82.579,P=0.010)是影响股腘动脉ASO患者DCB术后再狭窄的危险因素(表2)。
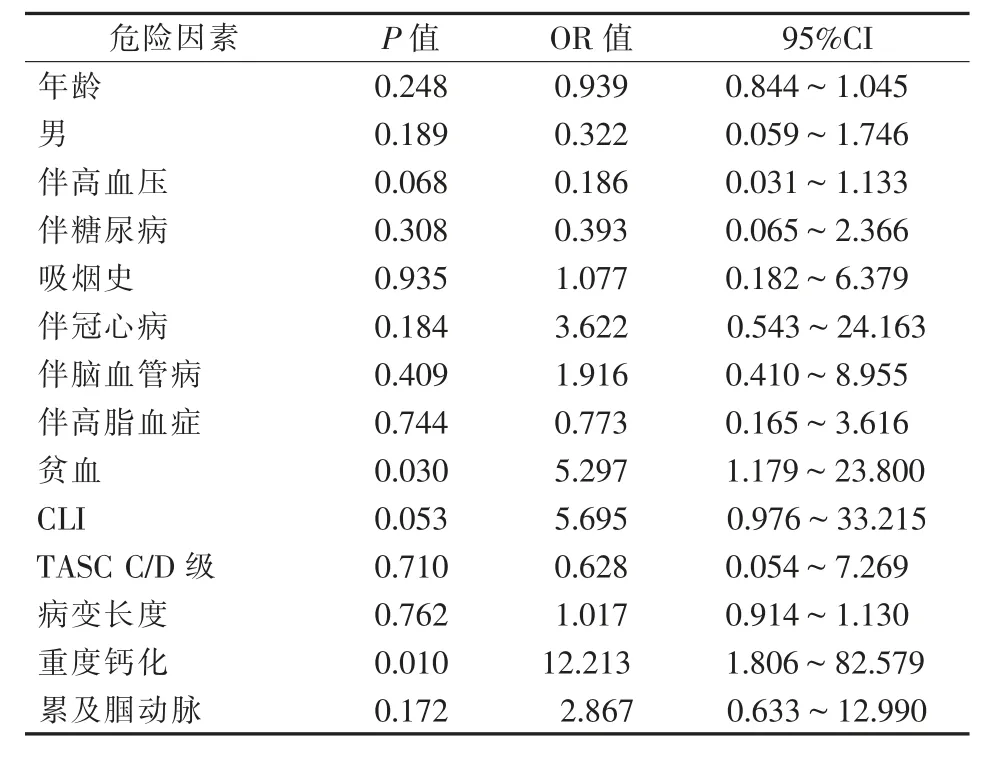
表2 DCB术后再狭窄危险因素

图1 患者术后12个月一期通畅率Kaplan-Meier生存曲线
3 讨论
目前血管腔内技术已成为治疗股腘动脉缺血性疾病首选方式,但术后再狭窄影响其疗效及预后。股腘动脉病变范围通常呈弥漫性和闭塞性,运动时易受腿部周围肌肉压缩及膝关节产生的机械力影响,因此腔内治疗股腘动脉病变具有挑战性,再狭窄发生率较高[7]。股腘动脉缺血性疾病DCB术后再狭窄相关危险因素及其有效防治,一直是临床研究密切关注的重点。贫血作为临床上重要且常见疾病,然而关于股腘动脉缺血性疾病DCB术后再狭窄的影响因素研究鲜有报道。本研究结果初步显示,贫血是股腘动脉ASO患者DCB术后再狭窄的危险因素。
有研究表明,DCB治疗下肢动脉病变的再狭窄率、管腔丢失率及避免TLR率明显优于POBA[4]。早期IN.PACT SFA研究结果显示,DCB组12个月通畅率(82.2%)显著高于POBA组(52.4%)[3]。MDT-2113SFA研究显示,DCB组12个月一期通畅率明显优于PTA组(89%对48%)[8]。LEVANTⅡ研究显示,DCB术后12个月通畅率(65.2%)优于普通球囊组(52.6%),DCB组TLR率(12.3%)低于普通球囊组(16.8%)[9]。DCB治疗长段复杂股腘动脉病变同样取得了良好效果。Tepe等[6]报道DCB治疗股腘动脉慢性完全闭塞(CTO)前瞻性研究,病变长度为平均(22.83±9.76)cm,12个月一期通畅率为85.3%。Schmidt等[10]回 顾 分 析IN.PACT DCB研 究,病 变 长度为平均(24±10.2)cm,1年、2年一期通畅率分别为79.2%、53.7%。本研究中患者病变长度为平均(19.99±11.09)cm,12个月一期通畅率为80.2%,与上述研究结果基本一致。
早期研究发现下肢ASO患者中贫血发生率高,Hb与下肢ASO发生呈负相关[11]。本研究显示贫血与股腘动脉ASO患者DCB术后再狭窄有关。Desormaisa等[12]研究显示贫血与外周动脉疾病(PAD)患者死亡率和截肢率相关,Hb越低死亡率和截肢率越高,贫血及其严重程度是PAD住院患者死亡率和截肢率的独立预测因素。有研究报道CLI患者与跛行患者相比贫血发生更为普遍[13]。也有研究提示术前贫血是CLI患者死亡的危险因素,术前Hb<100 g/L患者30 d内死亡 率更高、1年和5年生 存率更 低[14]。王海瑞等[15]研究表明Hb是影响股腘动脉支架术后支架内再狭窄(ISR)的危险因素,Hb低是ISR独立预测因子。以上研究均表明贫血与下肢动脉粥样硬化性病变患者预后密切相关,临床实践中需对贫血及其严重程度引起足够重视,采取积极有效的治疗措施,以降低再狭窄发生率,提高生存率。
贫血造成股腘动脉ASO患者DCB术后再狭窄发生率增加的可能机制:①动脉粥样硬化性疾病是一种慢性炎症性疾病,贫血可导致心输出量增加、血流动力学改变,加重血管内皮损伤,从而引起血管壁炎性反应,导致再狭窄发生[15];②贫血与氧化应激有关,红细胞是血液抗氧化能力的重要组成部分、流动的自由基清除剂,低密度脂蛋白极易被自由基氧化形成泡沫细胞[16],贫血时红细胞数量减少造成泡沫细胞形成增多,从而加重动脉粥样硬化,导致再狭窄;③贫血时自由基和抗氧化剂失衡诱发氧化应激,同样会导致内皮功能障碍[16],从而使内皮细胞因子分泌紊乱,引起血管收缩、血管平滑肌增殖与迁移、管壁重塑,导致再狭窄;④胆红素是血红素终末代谢产物,具有抗氧化活性[17],贫血引起血清总胆红素水平过低,机体抗氧化能力降低,进而间接导致动脉粥样硬化。已有研究表明胆红素偏低与冠状动脉介入治疗和颅内动脉狭窄支架植入术后ISR发生率增高相关[18-19]。
少数研究对DCB血管成形术后再狭窄危险因素进行了分析。Schmidt等[10]研究显示,男性、严重钙化和肥胖是再狭窄危险因素。IN.PACT SFA研究中男性、病变长度、严重钙化和既往同侧血运重建,被认为是再狭窄危险因素[20]。另有研究显示累及腘动脉和重度钙化是术后通畅率的独立相关因素[21]。Roh等[7]研究表明CLI和高胆固醇血症,是再狭窄独立风险因素。本研究中重度钙化、贫血是DCB术后再狭窄的危险因素,病变长度、累及腘动脉、CLI未显示对通畅率的影响,这可能是患者基本资料及病变特点与其他研究不同所致。
本研究局限性:①单中心回顾性分析样本量有限,需进一步通过前瞻性大样本临床试验研究Hb与DCB术后再狭窄的关系;②仅关注贫血对12个月一期通畅率的影响,需进一步深入探讨贫血与TLR率、生存率、远期通畅率的关系;③仅关注贫血与再狭窄的关系,未针对贫血严重程度和再狭窄进一步分层研究。
总之,DCB治疗股腘动脉ASO患者具有良好的12个月一期通畅率,贫血和重度钙化是DCB术后再狭窄的危险因素。

