体检人群颈动脉、眼底动脉硬化的影响因素分析
赵春燕 彭 军
北京大学第三医院北方院区综合内科,北京 100089
目前,动脉粥样硬化性疾病(如冠心病、脑血管病)的患病率逐年增加,成为威胁我国居民健康的首要问题,其中,不良生活方式、工作超负荷和精神压力大是影响健康的主要因素[1]。2019年国务院印发的《国务院关于实施健康中国行动意见》[2]着重强调要加强心脑血管疾病的防控,全面落实35 岁以上人群首诊测血压,加强血糖、血压、血脂的规范管理。健康体检是早期发现疾病的重要途径。通过体检,可以了解人群的健康情况、疾病谱分布和相关危险因素,实施有效的管理。健康管理,要由传统的针对疾病筛查的体检模式,向控制危险因素的新模式转变[3]。本研究选取来北京大学第三医院北方院区参加健康体检的647例北方公司在职及离退休人员的体检资料进行回顾性分析,观察颈动脉和眼底动脉硬化发生情况,探讨导致动脉硬化的危险因素,旨在为动脉粥样硬化性疾病的防治提供依据。
1 资料与方法
1.1 一般资料
选取2018年5—12月来北京大学第三医院北方院区参加健康体检的647 例北方公司在职及离退休人员的体检资料进行回顾性分析,其中男436 例,女211 例,年龄28~90 岁,平均(52±16)岁。本研究经北京大学第三医院北方院区医学伦理委员会审核及同意。纳入标准:①北方公司在职及离退休人员;②体检资料完整,无缺项;③所有研究对象对调查内容知情同意,且告知研究对象本研究对所选人群没有任何风险。排除标准:①严重躯体疾病,如心脏、肝肾等器官功能不全;②存在感染、手术等应激性疾病;③认知功能障碍或精神疾病。
1.2 方法
1.2.1 临床资料收集和生化指标测定 记录体检者临床资料,包括:姓名、性别、年龄、高血压、冠心病、糖尿病史。安静测量坐位血压:收缩压(systolic blood pressure,SBP)、舒张压(diastolic blood pressure,DBP)。测定空腹血糖(fasting blood glucose,FBG)、尿酸(uric acid,UA)、总胆固醇(total cholesterol,TC)、三酰甘油(triacylglycerol,TG)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)及低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)。
1.2.2 颈动脉检测 受检者取仰卧位,依次探查双侧颈总动脉、颈总动脉分叉部、颈内动脉及颈外动脉,在距颈总动脉分叉近心端2 cm 处测量并记录双侧颈总动脉内中膜厚度(intima-media thickness,IMT)。根据《中国高血压防治指南(2018年修订版)》[4]建议,IMT≥0.9 mm 为增厚,局限性IMT≥1.3 mm 为斑块,具备其中一项诊断为颈动脉硬化。据此,将本研究的647 例体检者分为非颈动脉硬化组(n=437)、颈动脉硬化组(n=210)。
1.2.3 眼底动脉检查 眼底动脉硬化按Keith-Wagener分级法分为4 级。Ⅰ级:视网膜动脉功能性狭窄或合并轻度硬化,此种改变主要发生于第2 级分支及以下分支;Ⅱ级:视网膜动脉的硬化程度比Ⅰ级明显,动静脉交叉处可见不同程度的病理性改变,动脉管径狭窄而不均匀;Ⅲ级:除视网膜动脉狭窄与硬化外,还有视网膜水肿、棉絮状斑、硬性白斑、出血斑等病变;Ⅳ级:除Ⅲ级外,还有视神经水肿。结果判读:Ⅰ~Ⅳ级者为眼底动脉硬化。据此,将本研究的647 例体检者分为非眼底动脉硬化组(n=534)、眼底动脉硬化组(n=113)。
1.3 统计学方法
采用SPSS 21.0 统计学软件进行数据分析,符合正态分布计量资料的均数用均数±标准差(±s)表示,两组间比较采用t检验,不符合正态分布者经过变量转换为正态分布后行统计学分析;计数资料采用率表示,组间比较采用χ2检验;多因素分析采用二分类Logistic回归分析,以P<0.05 为差异有统计学意义。
2 结果
2.1 非颈动脉硬化组与颈动脉硬化组各项临床指标的比较
本研究的647 例体检者中,颈动脉硬化的检出率为32.5%。单因素分析结果显示,颈动脉硬化组的男性占比、年龄、高血压史占比、冠心病史占比、糖尿病史占比、骨密度减低占比、SBP、DBP、FBG、UA 及TC水平高于非颈动脉硬化组,HDL-C 水平低于非颈动脉硬化组,差异有统计学意义(P<0.05);两组的脂肪肝占比、TG 及LDL-C 水平比较,差异无统计学意义(P>0.05)(表1)。

表1 非颈动脉硬化组与颈动脉硬化组各项临床指标的比较
2.2 非眼底动脉硬化组与眼底动脉硬化组各项临床指标的比较
本研究的647 例体检者中,眼底动脉硬化的检出率为17.5%。单因素分析结果显示,眼底动脉硬化组的男性占比、年龄、冠心病史占比、糖尿病史占比、骨密度减低占比、SBP、DBP、FBG 及UA 水平高于非眼底动脉硬化组,HDL-C 水平低于非眼底动脉硬化组,差异有统计学意义(P<0.05);两组的高血压史占比、脂肪肝占比、TC、TG 及LDL-C 水平比较,差异无统计学意义(P>0.05)(表2)。

表2 非眼底动脉硬化组与眼底动脉硬化组各项临床指标的比较
2.3 影响颈动脉硬化发生的Logistic 多因素分析
以颈动脉硬化为因变量(颈动脉硬化=1,非颈动脉硬化=0),以男性(男性=1,女性=0)、年龄(连续型变量)、高血压史(有=1,无=0)、糖尿病史(有=1,无=0)、冠心病史(有=1,无=0)、骨密度减低(有=1,无=0)、SBP(连续型变量)、DBP(连续型变量)、FBG(连续型变量)、UA(连续型变量)、TC(连续型变量)及HDL-C(连续型变量)等为自变量,进行Logistic回归分析。Logistic多因素分析结果显示,男性、年龄、骨密度减低及SBP 是颈动脉硬化的危险因素,HDL-C 为颈动脉硬化的保护因素(P<0.05)。高血压史、冠心病史、糖尿病史、DBP、FBG、TC、UA 不是颈动脉硬化的影响因素(P>0.05)(表3)。
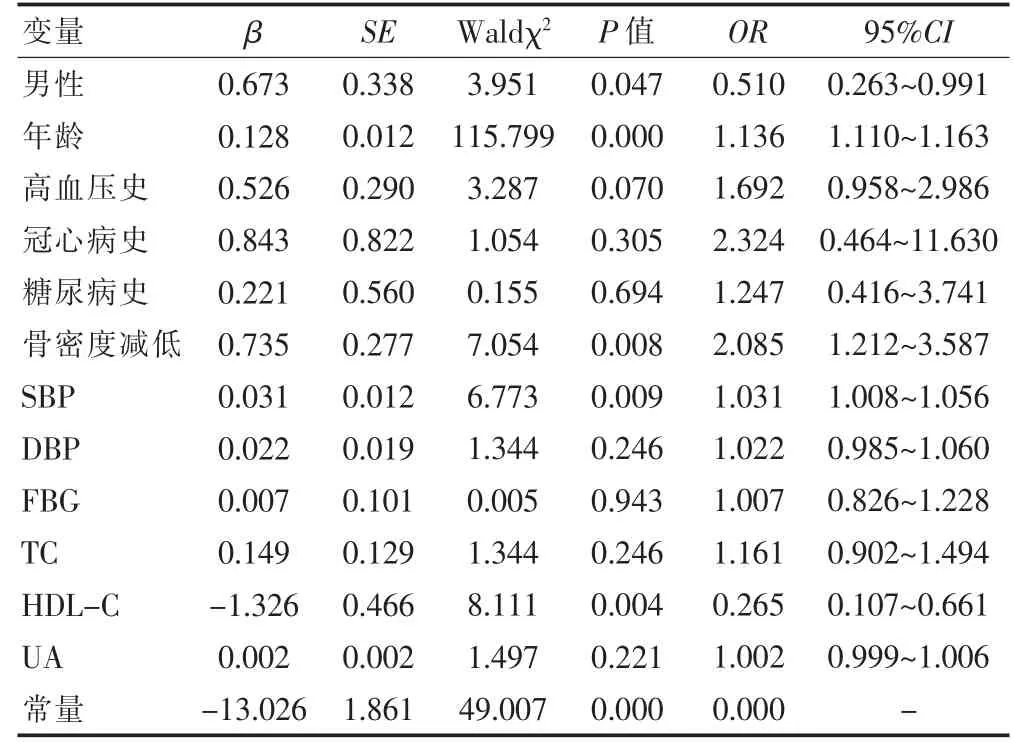
表3 影响颈动脉硬化发生的Logistic 多因素分析
2.4 影响眼底动脉硬化发生的Logistic 多因素分析
以眼底动脉硬化为因变量,以男性(男性=1,女性=0)、年龄(连续型变量)、糖尿病史(有=1,无=0)、冠心病史(有=1,无=0)、骨密度减低(有=1,无=0)、SBP(连续型变量)、DBP(连续型变量)、FBG(连续型变量)、UA(连续型变量)及HDL-C(连续型变量)等为自变量,进行Logistic回归分析。Logistic多因素分析结果显示,年龄、糖尿病史及SBP 是眼底动脉硬化的危险因素(P<0.05)。男性、冠心病史、骨密度减低、DBP、FBG、HDL-C、UA 不是眼底动脉硬化的影响因素(P>0.05)(表4)。
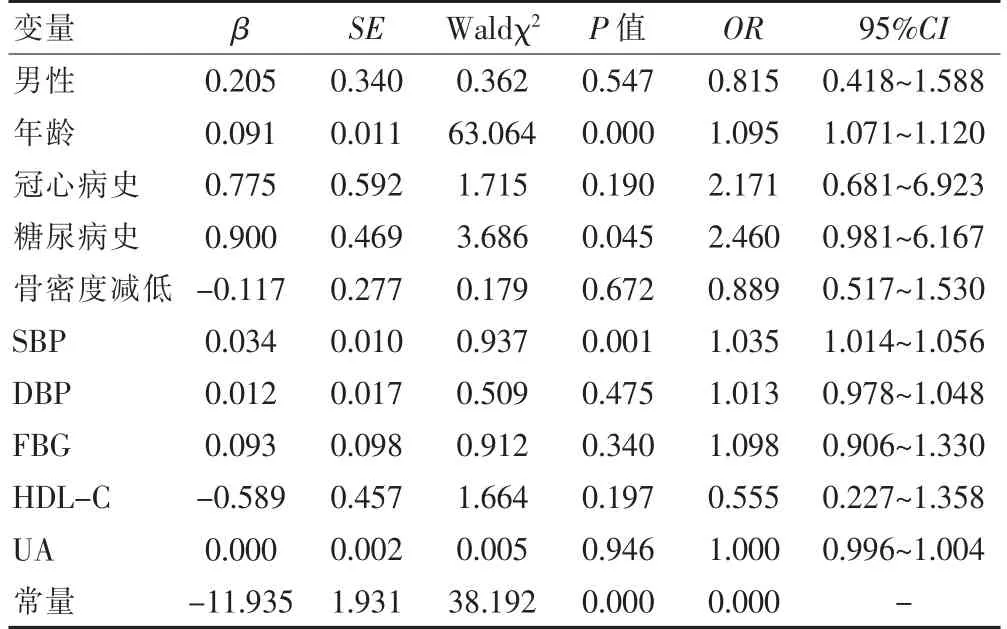
表4 影响眼底动脉硬化发生的Logistic 多因素分析
2.5 不同年龄组中动脉硬化发生情况的分布
将本研究的647 例体检者按照年龄分组如下:<31 岁(n=23)、31~40 岁(n=195)、>40~50 岁(n=119)、>50~60 岁(n=98)、>60~70 岁(n=90)、>70~80 岁(n=105)、>80 岁(n=17)。
不同年龄段中单独发生颈动脉硬化(合计116例)、单独发生眼底动脉硬化(合计19 例)以及发生颈动脉合并眼底动脉硬化(合计94 例)的分布情况见图1~3(封三)。结果显示,颈动脉及眼底动脉硬化发生率均随着研究对象的年龄增长而增加。在31~40 岁出现颈动脉硬化,在>40~50 岁出现眼底动脉硬化,显示颈动脉硬化的发生年龄早于眼底动脉。同时颈动脉、眼底动脉硬化在>70~80 岁年龄段中发生率均最高,分别为36.2%(42/116)和36.8%(7/19),而且颈动脉合并眼底动脉硬化在>70~80 岁年龄段中发生率也是最高,为43.6%(41/94)。
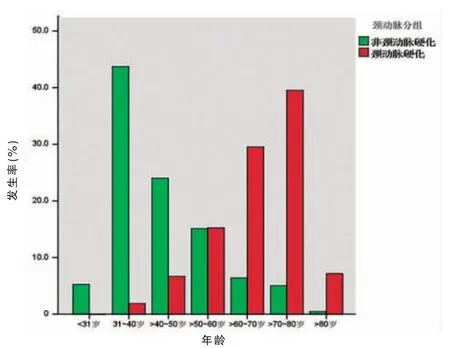
图1 不同年龄组中颈动脉硬化发生率的分布情况
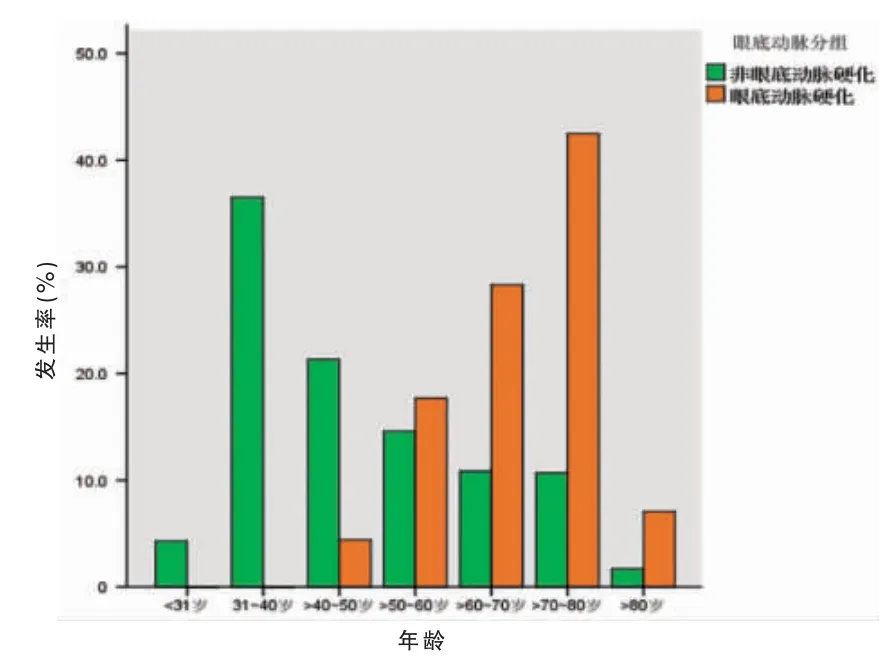
图2 不同年龄组中眼底动脉硬化发生率的分布情况
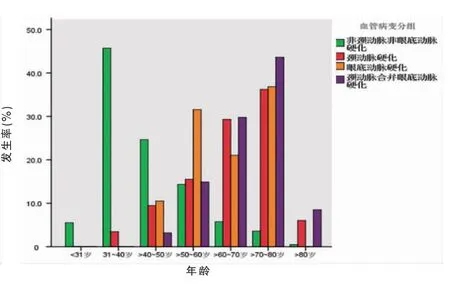
图3 不同年龄组中颈动脉合并眼底动脉硬化发生率的分布情况
3 讨论
随着生活方式的变化和人口老龄化问题的日益突出,动脉粥样硬化的发生逐年增加。病变早期常无任何症状,可仅表现为大血管IMT 增厚和(或)斑块形成,无创性高分辨率B 超检测颈动脉IMT 在一定程度上能反映血管动脉粥样硬化的程度,可作为大血管病变的替代指标[4]。视网膜中央动脉是全身唯一能够直接观察到的小动脉,是了解全身小动脉病变情况的途径。大血管和小血管病变多是共同存在的,两者有相似的发病机制和致病因素[5]。本研究结果显示,颈动脉硬化检出率为32.5%,眼底动脉硬化检出率为17.5%,男性的颈动脉硬化、眼底动脉硬化发病高于女性,差异有统计学意义(P<0.05)。国内文献报道[6],年龄>70 岁的男女动脉硬化检出率比较,差异无统计学意义(P>0.05),而30~70 岁组男性的动脉硬化发生率明显高于女性(P<0.05),考虑与雌激素对抗动脉硬化发展,对心血管系统具有保护作用有关。
动脉粥样硬化是一种炎症反应,在代谢紊乱环境中,LDL-C 沉积于血管内皮,巨噬细胞吞噬胆固醇形成泡沫细胞,此为动脉粥样硬化的病理过程[7]。本研究中,Logistic多因素分析结果显示,男性、年龄、骨密度减低及SBP 是颈动脉硬化的危险因素,HDL-C 为颈动脉硬化的保护因素(P<0.05);Logistic多因素分析结果显示,年龄、糖尿病史及SBP 是眼底动脉硬化的危险因素(P<0.05)。既往研究[8]认为,增龄诱发血管壁的结构及功能发生改变,内皮功能障碍,外弹性膜和斑块体积变大,IMT 随之增厚;增龄使上皮型血管平滑肌细胞数量增加,增加了内皮细胞对炎症因子的敏感性,加重动脉粥样硬化的发生;同时血管暴露于高血压、糖尿病等其他危险因素中,发生血管内皮功能障碍和结构改变,导致血管硬化,动脉阻力指数增加。本研究结果显示,颈动脉、眼底动脉硬化发生率随年龄增长而增加,在31~40 岁出现颈动脉硬化,在>40~50 岁发现眼底动脉硬化,即颈动脉硬化的发生年龄早于眼底动脉。31~50 岁,即为青中年,正是工作的主力军,他们的精神压力和工作强度大,运动时间少,再加上吸烟、饮酒、超重/肥胖、代谢综合征等危险因素逐年增加,使动脉硬化性疾病日趋年轻化。在>70~80岁颈动脉、眼底动脉硬化发生率均最高,所以对于老年人群,更应该每年进行血管检查,控制血管性疾病,降低致残率、致死率。
本研究结果显示,SBP 是颈动脉和眼底动脉硬化的危险因素(P<0.05)。与国内报道一致[9],收缩压、舒张压是脑卒中和冠心病的独立危险因素,血压升高较血压正常者动脉粥样硬化事件增加2~4 倍,可能由于高血压时肾素血管紧张素系统的主要物质血管紧张素Ⅱ(angiotensin Ⅱ,AⅡ)升高,而AⅡ为强力血管收缩剂,促进平滑肌细胞(smooth muscle cell,SMC)的生长,促进粥样斑块的形成。AⅡ也增加SMC 脂质氧化酶的活性,增加炎症反应及LDL 氧化。高血压也有促炎作用,增加过氧化氢及自由基形成,如血浆中超氧阴离子及氢氧离子增加。上述这些物质都减少内皮一氧化氮(nitric oxide,NO)的形成,增加血液中的细胞向管壁黏附及周围血管阻力[10]。周艺等[11]发现,血压严重程度与视网膜病变程度有一定联系,眼底病变等级随血压增高而增高。
本研究结果显示,在颈动脉和眼底动脉硬化组中,糖尿病史的比例均分别高于非颈动脉和眼底动脉硬化组,差异有统计学意义(P<0.05)。刘曼等[12]报道,长期高血糖可发生血管内皮细胞损伤,激活血小板,引起血小板黏附、聚集及释放功能增强,血流动力学改变,组织缺氧,毛细血管基底膜增厚致血管病变。所以,要监测控制血糖,避免血糖波动。
本研究结果显示,颈动脉、眼底动脉硬化组的骨密度减低发生率均分别高于非颈动脉和眼底动脉硬化组,差异有统计学意义(P<0.05)。Logistic多因素分析显示,骨密度减低是颈动脉硬化的危险因素(P<0.05)。于婷婷等[13]报道,骨密度与颈动脉或下肢动脉粥样硬化斑块的形成或狭窄程度呈负相关。本研究结果与于婷婷等[13]报道结果一致。从发生机制[14]考虑认为原因是:血管内皮细胞释放的NO 对成骨细胞和骨转化起着重要作用,而动脉粥样硬化时血管内皮细胞受损释放NO 减少,所以骨质疏松与动脉粥样硬化有相关联的病理生理。
除了已知危险因素,本研究结果显示,颈动脉和眼底动脉硬化组的HDL-C 水平分别低于非颈动脉和眼底动脉硬化组,差异有统计学意义(P<0.05);Logistic多因素分析显示,HDL-C 为颈动脉硬化的保护因素(P<0.05)。HDL-C 能将外周组织如血管壁内胆固醇转运至肝脏进行分解代谢,减少胆固醇在血管壁的沉积,起到抗动脉粥样硬化作用[15]。黄春旺等[16]通过超声射频信号定量评价动脉弹性功能及内皮形态改变技术,证实HDL-C 升高可降低高脂患者的颈动脉IMT 和僵硬度,升高弹性,延缓动脉粥样硬化进展。
综上所述,在体检资料中,笔者发现颈动脉和眼底动脉硬化的发生率较高,而且呈年轻化。男性、年龄、高血压、糖尿病和骨密度减低等是发生动脉硬化的危险因素,其中性别、年龄是不可控因素,而高血压、糖尿病、骨密度减低是可防可治的,因此要进行检测并采取有效控制,同时改善血脂,升高HDL-C 水平,避免血管性疾病的发生。

