碘的质谱测量方法研究进展
李金英,孙嘉忆,张 旭,张东翔,徐熙焱
(1.北京理工大学化学与化工学院,北京 102488;2.中国核学会,北京 100822)
碘有多种价态(-1、0、+1、+3、+5、+7),主要以分子碘(I2)、碘化物(I-)、碘酸盐(IO3-)和有机碘等形式存在,其中挥发性碘可以通过在大气中迁移实现地球化学循环[1]。由于地壳岩石中的碘含量低,土壤和水通常只能从大多数岩石的风化中获得非常少量的碘[1]。相比之下,海洋被认为是大陆环境碘的主要来源,海水中碘含量相对较高,浓度通常在45~60 μg/L之间[2]。在人体中,碘是形成甲状腺素(T4)和三碘甲状腺原氨酸(T3)的必要元素,这些激素对控制细胞代谢、繁殖和生长起着非常重要的作用。人体摄入的碘主要来自食物(如加碘盐、海产品及乳制品等),在饮用水和空气中也可以获得一定量的碘[1]。目前,碘缺乏是全世界人口健康和发展的一个重大威胁,特别是对低收入国家的儿童和孕妇[3],全民食盐加碘和补碘是预防和控制碘缺乏症的有效策略[4]。然而,过多的碘摄入会导致甲亢及自身免疫疾病。
天然存在的碘同位素有127I和129I,其中,127I是唯一的稳定碘同位素,129I是一种长半衰期核素(T1/2=1.57×107年)。自然界中的129I是由238U自发裂变和宇宙射线引起的氙散裂产生的,但目前环境中,129I主要来自核武器试验、核事故和乏燃料后处理等人为释放[5]。129I可以作为示踪剂来研究地质、海洋和环境过程以及监测核环境安全[5-8],通过129I的沉降分布可以对具有相似物理化学性质的131I(T1/2=8.3天)水平进行间接评估,进而评估核事故的污染状况和空间分布[9-10]。放射性碘释放后,由于其流动和挥发的特性,会对较远距离的海洋和农田造成污染,进而通过饮食进入人体诱发甲状腺癌。另外,129I、131I、123I、124I和125I等放射性碘元素有一定的积极作用,在医学诊断与治疗、寻找地下水和测定地下水的流速及流向等方面应用广泛[11-13]。
对碘的分析方法主要包括以下3个应用方面:1) 为了评估碘的营养状况和流行病学,对土壤、植物、食品及生物样品中的碘进行定量分析,催化分光光度法是由Sandell和Kolthoff在1937年开发的经典测量技术[14],该方法基于碘对Ce4+(黄色)和As3+之间的氧化还原反应的催化作用,最终产生无色的Ce3+和As5+离子[14-15],此外还有基于比色反应的分光光度法[16]、X射线荧光光谱法[17]、原子吸收光谱法[18-19]、阴极溶出伏安法[20]、离子色谱法[21]、电感耦合等离子体发射光谱法[22]、电感耦合等离子体质谱法[23];2) 为了保证核环境安全,实现对环境、生物和食物中长半衰期核素129I的监测和分析,目前可以达到环境水平129I的测量方法只有中子活化法和加速器质谱法[24];3) 基于核工业正常生产的分析需求,通常有X射线谱法、伽马谱法、液体闪烁计数法和符合法等放射化学分析方法[25]。
目前已有的分析方法中,电感耦合等离子体质谱法(ICP-MS)已成为碘分析最常用的方法,这是20世纪80年代初发展起来的一种技术,通过特殊的接口技术将电感耦合等离子体与质谱相连接,用于无机元素及同位素分析测定[26-28]。与其他无机元素分析技术相比,ICP-MS分析速度快、灵敏度高、检出限低、线性范围宽,可进行多元素同时分析。另一方面,加速器质谱法(AMS)是20世纪70年代末发展起来的以加速器为基础的现代核分析技术,它不仅是目前测定129I最灵敏的测量技术,还是分析129I/127I原子比低于10-10的核前年代样品的唯一方法[29]。此外,AMS还具有分析速度快、样品用量少的特点,通过对原子直接计数进行测量,主要用于测量长寿命放射性核素与稳定核素的同位素丰度比。
实现碘的高精度分析测量是碘相关研究顺利进行的基础。碘具有易氧化还原、易挥发、易吸附的特性,样品处理过程中易造成碘的损失,测量过程还会产生记忆效应、仪器污染并导致较高的空白,特别是对于碘含量极低的样品,如果处理不当将造成较大的误差,因此碘样品的前处理是分析过程的关键。样品中的碘能够以无机碘化物和碘酸盐、有机伴生碘、矿物和氧化物伴生碘的形式存在[30],因此,在ICP-MS测碘前,通常需要采用一些前处理手段将碘提取出来。酸消解法所用的酸必须具有足够高的氧化电位,以实现将挥发性碘氧化为非挥发性碘,该方法应用较少[31];碱提取法比较温和,应用广泛,但提取液中的复杂基质需要进一步纯化[30];此外,还有燃烧法[32]、微波诱导燃烧法[33]、灰化法[34]、热水解法[35]、微波辅助碱提取法[36-37]等。在使用AMS测碘时,除了对样品中的碘进行提取,还需要进一步分离、富集、纯化以及制备靶样。
碘测量方法的综述已有一些报道[24,38],但未见对质谱法测量碘的总结。本综述将围绕碘的质谱测量方法,总结质谱发展概况、碘样品前处理方法以及国内外总碘、碘同位素和碘形态的质谱测量方法新进展。
1 质谱发展概况
1.1 ICP-MS发展概况
1.1.1ICP-MS仪器技术 ICP-MS是测定碘的强有力工具,目前对于碘的测定,以四极杆电感耦合等离子体质谱(ICP-QMS)的应用最多,已成为最常用的多元素分析仪器之一。早期的ICP-QMS存在一系列的质谱干扰和非质谱干扰问题,随着技术的发展和应用需求的增加,四极杆和多极杆ICP-MS技术不断发展,通过在质量分析器前增加碰撞反应池,通入气体与多原子离子进行碰撞或反应,以消除多种干扰并提高仪器的灵敏度[39]。三重四极杆电感耦合等离子体质谱(ICP-QQQ)是在2个四极杆质谱仪之间增加1个碰撞反应池,也被称为串联四极杆电感耦合等离子体质谱仪。第1个四极杆(Q1)用于扫描和选择目标离子,然后在碰撞反应池中裂解前体离子,再用第2个四极杆(Q2)分析产生的碎片离子[40]。三重四极杆技术的发展进一步提高了碰撞/反应池消除干扰的能力,该技术在测定碘时可以有效消除多原子干扰和来自129Xe+的等压干扰,由此实现了对碘及碘同位素的测定[30,41]。
电感耦合等离子体-飞行时间质谱(ICP-TOF MS)具有极高的精密度和准确度,并且分析速度极快,可以与多种瞬态进样技术联用,如电热蒸发技术[42]、流动注射技术[43]、激光烧蚀技术[44-45]、气相色谱技术[46]等;多接收电感耦合等离子体质谱仪(MC-ICP-MS)安装了多个法拉第杯,是获得精确同位素比值的有力工具,与热电离质谱(TIMS)相比,MC-ICP-MS样品制备量少、样品通量高,且具有电离多种元素的能力,但其存在较严重的仪器质量偏差[47-48];双聚焦扇形磁场电感耦合等离子体质谱(SF-ICP-MS)由磁场分析器和静电场分析器组成,这两种分析器可分别实现方向聚焦和能量聚焦。新一代SF-ICP-MS仪可实现高达14 000(m/Δm)的分辨率,可以有效解决ICP-QMS存在的质谱重叠干扰等问题[49-51],并实现碘的测定[50]。此外,SF-ICP-MS还具有极高的灵敏度和极低的背景水平[51],但价格较贵、维护困难。
1.1.2ICP-MS联用技术 将ICP-MS与色谱技术联用可以实现对元素形态的分离和测定,其中应用最广泛的是高效液相色谱-电感耦合等离子体质谱(HPLC-ICP-MS)[52-54],将高效液相色谱(HPLC)的高分离能力和ICP-MS的高选择性、高灵敏度和宽动态线性范围等优点相结合,使样品溶液经过HPLC分离后进入ICP-MS中测定,从而实现形态分析和元素定量。目前,HPLC-ICP-MS已广泛用于对碘形态的定性和定量分析[55-57],而离子色谱、气相色谱与ICP-MS联用测定碘的报道则较少。
ICP-MS还可以与其他进样系统联用。如与流动注射技术(FI)联用,可通过FI把样品溶液注入到载流中与载流发生混合、反应,从而实现样品的在线分离和富集。FI系统可以在样品进入ICP-MS前分离干扰基质组分和预浓缩超痕量分析物,从而避免高盐含量溶液堵塞雾化器,同时还具有样品通量高、样品传送效率高、可自动化、样品污染风险小等优势[58-59];与激光烧蚀技术(LA)联用,可通过LA直接将样品的固体表面在激光烧蚀室内用脉冲激光束烧蚀,再进行ICP-MS分析。激光烧蚀电感耦合等离子体质谱(LA-ICP-MS)通过LA扫描表面可以构建元素分布图像,主要应用于生物成像[60-62]。毛细管电泳技术(CE)与ICP-MS联用可使溶质在毛细管中的高直流电压下基于迁移速率差异而分离,并保留原有的化学信息[27]。毛细管电泳-电感耦合等离子体质谱(CE-ICP-MS)具有运行成本低、适用范围广、分离效率高、样品用量少、速度快的优点,目前主要用于元素形态分析[63-64]和蛋白质组学[65]研究;电热蒸发技术(ETV)与ICP-MS联用可在导电的蒸发室中直接将固体样品变为气体,从而减少样品处理过程的时间,并将污染降至最低,同时最大限度地提高样品引入效率[66-67]。此外,通过调节温度还可以从基体中选择性地蒸发分析物,降低可能存在的质谱和非质谱干扰[68-69];氢化物发生器(HG)与ICP-MS联用,可通过硼氢化钠等还原剂将待测元素还原为挥发性的共价氢化物,并以气体状态从溶液中分离出来,从而实现待测元素的分离和富集,并减少基质造成的干扰[70]。同时,该技术还可以提高样品的传输效率,进而提高灵敏度[71-72]。
1.2 AMS发展概况
AMS是一种基于加速器和离子探测器的高能同位素质谱,其克服了传统质谱存在的分子本底、同量异位素本底干扰的不足,待测同位素丰度比可低至10-15。AMS最早是1939年由Alvarez和Cornog提出的,他们使用回旋加速器测定3He[73]。随后的近40年间,由于受到重粒子探测技术和加速器束流品质等条件的限制,AMS的研究几乎没有进展。直到1977年,Muller[74]建议用回旋加速器探测14C等长寿命放射性核素,随后AMS迅速发展,其测量的核素由最初的14C到几乎涵盖了整个元素周期表的元素,并在许多领域得到应用[75-76]。使用AMS测量129I的开创性工作可以追溯到Elmore等[77]和后来的Kilius等[78],在此之后,环境中129I的研究显著增加,AMS成为测定环境水平超痕量129I的强有力工具。
自2001年以来,AMS仪器不断朝着低成本、易操作的小型化方向发展。在未来,AMS将摆脱传统负离子源、剥离器系统和串列加速器等核心部件,采用正离子源、低能加速段(100 kV范围)等技术[79]。通过改进核心部件和重新设计系统,使AMS朝着更加小型化和更高灵敏度的方向发展[80]。
2 质谱法测碘的样品前处理技术新进展
2.1 ICP-MS法测碘的样品前处理技术
ICP-MS对基体的耐受性低于原子吸收光谱、原子荧光光谱等,易受高基体样液的干扰,使仪器受到严重损耗,因此,进样前必须对样品进行前处理。由于碘易挥发,在样品处理过程中易形成I2和HI,从而导致碘损失,还会产生明显的记忆效应,研究人员通常使用碱性溶液消解样品来解决这一问题[36,81]。虽然酸也可以用于消解样品,但必须具有足够高的氧化电位,将挥发性碘氧化为非挥发性碘,因此,酸消解样品的应用较少[31]。
样品处理方法的选择不仅与样品种类、待测元素性质有关,还与测量仪器的特性有着密切关系。以下总结了ICP-MS法测碘的几种典型的样品前处理技术,主要涉及到样品的消解方法,其不仅适用于ICP-MS测定总碘的样品前处理过程,还适用于ICP-MS测定碘同位素和碘形态,以及AMS测定碘同位素的样品前处理过程。
2.1.1碱提取法 碱提取法是指采用适当的碱性溶剂将样品中的碘提取到碱性溶液中,该方法温和、操作简单、应用范围广。Huynh等[81]首次报道了四甲基氢氧化铵(TMAH)提取母乳样品中的碘,并用于ICP-MS分析研究,在90 ℃下用TMAH提取母乳样品中的碘,与之前的研究(提取时间2~3 h)相比[82-83],提取时间缩短为1 h,进而缩短了样品处理的总时间;Yang等[30]在90 ℃下用TMAH提取土壤、沉积物和岩石样品中的碘,用K2S2O8氧化TMAH提取液中的有机物并释放出碘,再通过溶剂萃取和反萃取有效去除有机物,以避免在三重四极杆ICP-MS模式分析过程中出现严重的基质效应,同时还去除了Mo、Cd和In等干扰元素。
然而,仅使用TMAH提取,样品基质溶解效率很低。微波辅助法能够有效促进碱性溶剂对样品中碘的提取,从而缩短样品处理时间。Jerse等[36]优化了微波辅助-碱提取法处理植物样品中的碘,选择25%TMAH-H2O(1∶5,V/V)为最佳比例的提取溶剂,并在微波炉中设定温度程序为20 min升温至200 ℃,恒温保持5 min。Romarís-Hortas等[37]研究了微波辅助TMAH同时提取食用海藻样品中碘和溴的可行性,首先确定了TMAH的体积和温度以及二者之间的二阶相互作用具有的统计学意义(置信区间为95%),然后通过优化获得最佳的提取温度200 ℃和提取剂TMAH(12.5%,m/V)的最佳体积10 mL,并且将升温时间和恒温时间分别设为10 min和5 min。微波辅助-碱提取的样品处理方法与ICP-MS的测量技术相结合是一种快速、可靠的分析方法。然而,碱提取法只能消解样品,不能消解有机基质,对于消解后样品溶液中的复杂基质还需要进一步纯化[30]。另外,该方法不适用于碘和金属元素的同时测定,不能充分利用ICP-MS多元素同时测定的优势[84-85]。
2.1.2酸消解法 用酸消解含碘样品一般会生成HI和I2,造成碘的损失,且产生的I2易吸附在仪器中,导致信号不稳定和记忆效应,因此,使用的酸必须具有足够高的氧化电位,通常选择硝酸结合强氧化剂(如H2O2、HClO4)以将挥发性碘氧化为非挥发性碘[31]。此外,高浓度酸会对ICP-MS测定结果造成干扰,有时需要在密封环境中进行,且在使用HClO4消解有机样品时易发生爆炸,因此相比温和的碱提取法,酸消解法的应用较少。但在一些情况下,如在核废料处置的安全性研究中,使用碱提取法会使高价金属沉淀并沉积在样品管和仪器中,从而导致对分析结果的低估[84]。因此,需要对样品中碘和金属元素进行分步处理或者使用酸消解法。另外,也可以在中性pH值和室温条件下用NaOCl氧化碘化物[86],Brix等[84]将这种氧化反应作为简单的样品制备步骤,用于在酸性条件下ICP-MS对高价金属和碘的同时测定,无需附加设备和特殊的反应条件,即使在复杂和高盐度的基质中,也能成功地定量碘和高价金属离子。Leppanen等[87]使用高压灰化器,通过两段消解程序测定奶粉样品中总碘含量。第一阶段使用15.2 mol/L HNO3和30% H2O2在300 ℃下消解样品2 h;第二阶段将消解容器冷却,并加入20%(m/V)Na2S2O8溶液作为附加氧化剂。100 ℃消解30 min后得到透明无色的样品溶液,用于ICP-MS测定样品中碘含量。
微波辅助-酸消解法通常利用微波加热封闭容器(或敞开容器)中的试样和酸消解液,在高温增压环境下快速、完全分解样品。Shah等[88]使用MES 1000封闭式微波消解系统,以65%HNO3和30%H2O2作为消解剂,通过矿化程序将海藻样品完全消解。Fujisaki等[85]用HNO3和H2O2在微波辅助消解中将碘转化为碘酸盐,并将乙酸作为碳源添加到样品和标准溶液中,以防止碳上的电荷转移到碘上。该方法可以同时测定婴儿配方奶粉中的碘和其他12种重要元素(Na、Mg、P、K、Ca、Cr、Mn、Fe、Cu、Zn、Se、Mo)。
2.1.3热水解法 早期研究中,Warf等[89]通过铂组装炉使用水蒸汽加热样品,生成的挥发性产物冷凝后通过滴定来测定。热水解法通常在高温(约1 000 ℃)下进行反应,热水解过程速度慢,加入铀、钒、铝和钨的氧化物通常可以提高反应速度。这一过程释放的挥发性卤素以对应卤素酸的形式经过冷凝器,然后收集在碱性溶液中进行下一步测定。热解法的主要优点是基质和样品完全分离,可提供相对纯净的分析物[35,90]。由于卤化物可以直接分离而无需进行预先的熔融,该方法特别适用于固体样品中卤化物的处理。构建热水解系统可选用相对简单和廉价的材料,在常规分析中优势显著[35]。
2.1.4干灰化法 干灰化法是通过高温灼烧将有机物破坏,用酸溶解剩余的矿物质成分,该方法适合处理固体样品,常用于测定有机物含量较多的样品。孔红玲等[91]采用干灰化法破坏有机物,向植物性农产品中加入K2CO3和ZnSO4,在电热板上以200 ℃炭化1 h排掉炭化的黑烟,加盖放入箱式电阻炉中以200 ℃保持1.5 h,使炭化更完全,再升温至520 ℃灰化2 h。该方法的缺点是高温开放系统,极易产生碘元素的损失。
2.1.5燃烧法 燃烧法是在充满氧气的密闭容器中燃烧分解样品中的有机基质,然后在碱性介质中碘以碘化物的形式被吸收,该方法多用于处理食品和生物样品,与其他方法相比,该方法具有残留碳含量低、可用于多种方法测定的特点。Gelinas等[32]使用Trace-O-Mat氧气燃烧仪,将营养生物样品在氧气流中燃烧后,将燃烧产物在5%水溶性叔胺(CFA-C)中收集,以此来测总碘。Schramel等[92]使用简易的Schöniger烧瓶燃烧生物样品,用氢氧化钠或TMAH作为吸收溶液,该方法可用于测定总碘含量低至约50 μg/kg的生物样品。与Trace-O-Mat系统相比,该方法操作更加简便、设备成本更低。然而,燃烧法存在一些不足,如样品处理量少、消解样品的质量低、安全性低,且不能通过回流步骤提高分析物的回收率[38,93]。微波诱导燃烧法(microwave-induced combustion, MIC)的出现很好地克服了这些局限,通过在密闭石英容器中用氧气加压燃烧样品,用微波点火,燃烧后用碱液吸收气体并通过回流提高回收率。Mesko等[33]用MIC法处理食品中的碘,使用硝酸铵(50 μL 6 mol/L)作为助燃剂,容器充入1.5×106Pa的O2,以MIC和50 mmol/L (NH4)2CO3或56 mmol/L TMAH为吸收液,回流5 min,碘回收率大于99%。Costa等[94]对传统MIC法进行改进用来测定蜂蜜中碘含量,使用微晶纤维素作为助燃剂和聚乙烯薄膜包裹样品,燃烧后用50 mmol/L NH4OH吸收气体,碘的回收率在99%~104%之间,相对标准偏差小于5%。MIC法可分解的样品质量高(可达1 g),最多可同时处理8个样品,消解时间可限制在30 min内,为下一步ICP-MS测碘提供了合适的样品处理途径,可使测量方法检出限达到超痕量水平(6.0 ng/g)[94]。
使用ICP-MS测定各种碘样品的前处理方法及特点列于表1。
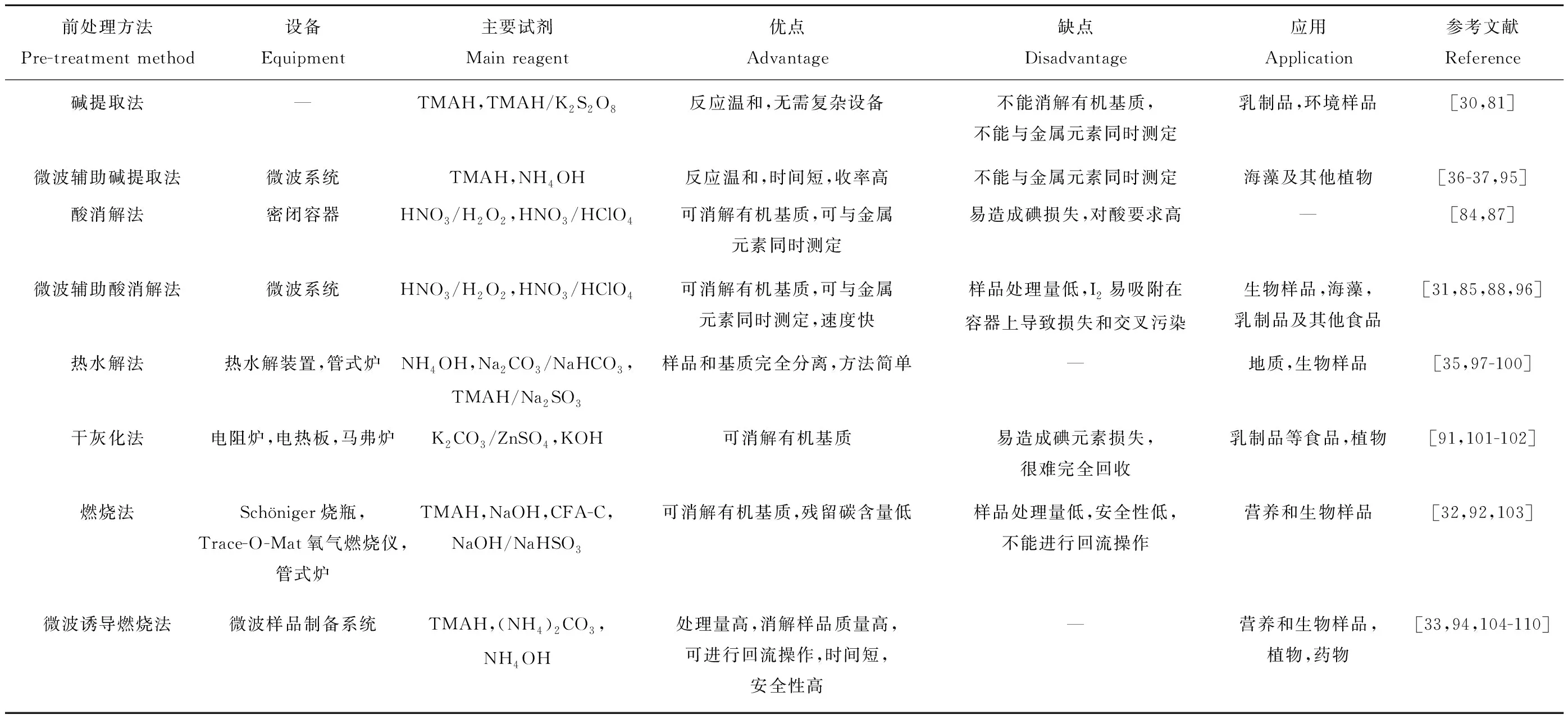
表1 ICP-MS法中含碘样品的前处理方法及特点Table 1 Pretreatment methods and characteristics of iodine-containing samples in ICP-MS
2.2 AMS法测碘的样品前处理技术
使用AMS法分析样品中129I时,通常先用与ICP-MS法相同的样品前处理技术进行消解和提取,然后进一步预浓缩、分离、富集、纯化,最终以固体形式(AgI沉淀)制备分离的碘,并与导热、导电介质混合压入靶中。对于129I含量极低的样品,必须加入稳定127I的载体以提高提取效率[103,111]。对于129I含量超低的样品,由于稳定碘载体中存在的少量129I会对样品造成污染,影响测量结果的准确度,通常选择无载体的样品前处理方法[29,112-113]。此外,Adamic等[114-115]提到了电沉积方法,与沉淀法相比,该方法在银或铌包银导线上电沉积的AgI更容易加载到阴极上,无需使用研钵和研棒混合少量的AgI和金属粉末,避免了样品间可能的交叉污染,但这种方法很少见。
以下主要介绍含碘样品的分离富集纯化和靶样制备的过程。使用AMS测定的各种碘样品的前处理方法及特点列于表2。

表2 AMS法中含碘样品的前处理方法及特点Table 2 Pretreatment methods and characteristics of samples containing iodine in AMS
2.2.1溶剂萃取法 溶剂萃取法是从溶液中分离碘最常用的方法,是利用碘在CCl4(或CH3Cl)中的溶解度远大于在H2O中的溶解度,且CCl4(或CH3Cl)与H2O互不相溶的原理而建立的[116-117]。首先将样品溶液过滤、预浓缩,并将有机碘转化为无机碘,然后转移至分离漏斗中进行萃取。先加入127I载体和125I示踪剂,再加入NaHSO3将IO3-还原为I-,充分混合后用HNO3调整pH值为1~2,再加入CCl4和一定量的NaNO2,将I-氧化为I2并萃取到CCl4相,再加入NaHSO3将I2还原并反萃至水相。重复萃取和反萃取过程,最后将I2反萃至水相。用伽马能谱仪对125I进行计数,计算碘的回收率。为实现AMS对129I/127I比值的测定,还需要加入AgNO3得到AgI沉淀以制备靶样[118]。
2.2.2离子交换色谱法 离子交换色谱法主要用于大体积水样中无机碘的分离,将样品溶液过滤,加入125I示踪剂和NaHSO3后,使用HCl调节pH值为1~2,将IO3-还原为I-,然后装入填充阴离子交换树脂(Bio-Rad AG1-X4,NO3-型,50~100目)的色谱柱中,用0.5 mol/L NaNO3溶液洗涤柱,再用2.0 mol/L NaNO3溶液洗脱吸附在色谱柱上的碘化物。取适量的洗脱液测定125I以得到碘的回收率,并将剩余洗脱液用于共沉淀分离碘[29]。当样品溶液中含有大量有机碘时,使用该方法之前还需要先将有机碘分解并转化为无机碘。
2.2.3AgI直接沉淀法 AgI直接沉淀法具有简便、直接、快速的优点,适用于碘含量相对较高的样品溶液。该方法通常先加入127I载体,再加入NaHSO3和HNO3将IO3-还原为I-,然后直接向制备好的样品溶液中加入AgNO3形成AgI沉淀。对于同时存在Cl和Br的样品,生成AgI黄色沉淀的同时还会产生AgCl和AgBr白色沉淀,需要加入氨水选择性地除去AgCl和AgBr沉淀[103]。
2.2.4AgI-AgCl共沉淀法 对于一些碘浓度极低的样品,分离出的少量碘不足以制备AgI沉淀,而加入稳定碘载体时会因其中含有的微量129I对测量结果造成影响,此时通常选择AgI-AgCl共沉淀的方法[29,112-113,119-120],将样品预处理后,向溶液中加入适量的NaHSO3将IO3-还原为I-,再加入HNO3调至pH值为1~2,随后再加入适量的NaCl和AgNO3,生成AgI-AgCl-Ag2SO3-Ag2SO4共沉淀。再向共沉淀物中加入HNO3和H2O,洗去Ag2SO3和Ag2SO4沉淀,用氨水洗去过量的AgCl,得到AgI-AgCl共沉淀,将其干燥后研磨成细粉,加入2~3倍质量的Nb粉末,混合均匀后压入铜靶进行测量。
2.2.5无化学过程的靶样制备 无化学分离和富集流程的靶样制备只需将样品干燥并研磨均匀,与含有稳定碘载体的Nb粉末混合后直接快速制靶[121-122]。该方法速度快、操作简单且成本低廉,适用于紧急情况下大批量样品中129I的快速筛选分析。由于添加到Nb粉中的稳定碘载体和由原始样品结合的129I原子处于不同的化学状态,在Cs+溅射过程中会存在同位素分馏的可能[122],并且该方法缺少纯化过程,会存在一些分子片段的干扰,从而影响测定结果,因此仅限于筛选和快速评估。
3 碘的质谱测量技术新进展
3.1 总碘的测定
ICP-MS测定总碘过程中存在质谱和非质谱干扰,质谱干扰主要来自双电荷离子、多原子或加合物离子、难熔氧化物、同量异位素;非质谱干扰主要是基体效应,包括空间电荷效应、基体对分析物信号的影响效应以及高盐溶液引起的物理效应、记忆效应等。为减小这些干扰,Xu等[126]建立了ICP-MS法测定不同盐度溶液中Br和I,估算了动能分辨(KED)和标准(STD)模式下与基体有关的等压干扰(来自40Ar39K、40Ar38Ar1H对79Br的干扰),发现以He为碰撞反应气体的KED模式可以有效消除这些干扰。另外,使用Dowex 50W-X8阳离子交换树脂进一步纯化高盐度水样,用来消除基质效应。Fletcher等[41]使用ICP-QQQ测定铀中的P、S、Br、I,消除了分析物中常见的干扰。通过是否使用50 mg/L的铀基质来分析可能的基体效应,结果表明,有无基质对测量结果的差别不大。Zheng等[50]使用SF-ICP-MS在低分辨率模式下测定海水中的碘,该方法具有良好的检出限(0.23 μg/L),并且由于SF-ICP-MS具有较高的灵敏度(通常比ICP-QMS高约2个数量级),只需小样本量的海水(0.1 mL)。这种方法避免了繁琐复杂的有机物分解和氧化还原的处理过程,并且不需要预浓缩和分离,是一种测定海水中总碘的简便、快速的分析方法。
对于复杂基质中多元素的同时测定,Brix等[84]提出了一种通过改变碘形态进行测定的方法。在室温下加入次氯酸钠,将挥发性碘转变成在酸性条件下稳定的非挥发性IO3-,实现了酸性条件、复杂基质中碘和高价金属的同时测定。对于有机总碘(TOI)的测定,Sayess等[127]采用ICP-MS法测饮用水中TOI,并将无机碘分离,使用HNO3将待测水样酸化至pH<1,然后以一定的流速使酸化后的样品通过2个连续的颗粒活性炭吸附柱,经过燃烧、捕集,向捕集液中添加2%(V/V)的TMAH,用ICP-MS进行测量,最后使用0.1%(V/V)的TMAH进行洗涤。该方法可在总碘含量较低的体系中轻松测定环境中TOI的含量。
随着ICP-MS技术的不断发展和仪器灵敏度的不断提高,ICP-MS对总碘含量的测量方法研究十分活跃,应用范围也在不断扩大。目前人们对ICP-MS测定总碘的研究主要是为了克服各种因素的干扰,并使其适用于基质更加复杂的样品。碘的ICP-MS分析方法已广泛应用于环境[98]、生物[94,128]、食品[129]、海洋[130]、核工业[131]等领域中。
3.2 碘同位素的测定
人们对碘同位素的关注主要以长半衰期的129I为主,在使用ICP-MS测定时,由于氩等离子体气体中129Xe的严重干扰、可能存在的127IH2+干扰以及测定129I/127I同位素丰度比灵敏度的不足,普通ICP-MS很难准确地测定129I/127I。随着质谱技术的发展,一些仪器已克服了这些问题。Izmer等[132]使用六极碰撞池电感耦合等离子体质谱(ICP-CC-QMS)测定水溶液和污染土壤样品中的129I/127I。在ICP-CC-QMS在线耦合进样装置中,以氧气为反应气和载气,通过气相从固体环境物质中热脱附碘。采用氧气和氦气混合气体作为反应物,在六极碰撞池中降低129Xe+干扰的本底强度。该方法无需样品制备,优化后,水溶液中129I+检出限为8×10-13g/mL,比SF-ICP-MS提高了2个数量级。通过气相解吸直接测定污染土壤样品中129I+的检出限为3×10-11g/g。Yang等[30]使用ICP-QQQ测定环境样品中129I活度和129I/127I原子比,对样品中的碘用TMAH进行提取并纯化后,用0.01%(NH4)2SO3将I-引入ICP-QQQ,随后采用MS/MS模式进一步消除多原子干扰(127I(H2和D)+、97MoO2+、113InO+和113CdO+)和来自129Xe+的等压干扰。将单MS模式测得的127I质量浓度与MS/MS模式测得的129I/127I原子比相结合,得到129I的质量浓度,然后使用152.90 ng/Bq因子计算出129I活性。
基于敞开式离子化质谱体系的电喷雾萃取电离质谱(EESI)也可用于测定129I,Wu等[133]使用EESI的负离子检测模式,快速测定空气中痕量放射性129I2含量。首先将空气样品通入过量的Na2SO3溶液,把气态129I2完全转化为129I-,再向溶液中加入过量的127I2形成三碘化物离子络合物(即129+127×2I3-),然后进行串联质谱实验以排除假阳性,最后通过定量测定三碘离子复合物的特征碎片离子(即129I-)实现对129I的定量。该方法在核泄漏和核爆炸等领域具有潜在的应用前景。
AMS是目前测定129I最灵敏的方法,能较好地克服ICP-MS法测定129I时来自129Xe的等压干扰问题,从而达到较低的本底和超低的检出限。Li等[118]用旋转蒸发-AMS法快速测定大体积水样中的129I,通过优化实验条件使pH值为7,还原剂浓度5 mmol/L,水浴温度60 ℃,最终浓缩体积100 mL,去离子水碘回收率高达99%。与传统的低温蒸发法相比,旋转蒸发法可以有效地将碘的预富集时间缩短至少4倍。Zhang等[119]利用热解和AgI-AgCl共沉淀法结合AMS,开发了一种用于准确测定气溶胶样品中129I的分析方法。研究发现,样品在800 ℃燃烧1 h后,碘的种类对样品的化学产率没有影响,热解过程中碘的化学产率为(81.4±5.8)%,气溶胶样品中129I的检出限为1.3×104个原子/m3,与使用碱灰分离和溶剂萃取法相比,所需气溶胶样品量至少减少3倍。Hou等[103]通过优化参数,实现了管式炉热解分离碘的安全操作,建立了稳定可靠的生物样品中痕量碘的热解分离方法,回收率达80%以上。经过进一步分离碘,制备靶样,最后使用AMS测定129I,可高效灵敏地测定生物样品中超低水平129I,该方法测得的129I检出限为6×10-17g/g(或0.4 nBq/g)。与常规方法相比,该方法易于操作、碘回收率高、工艺简单且交叉污染少,已成功用于大量植被样品中129I的测定。Liu等[113]研究了一种用于准确测定无载体AgI-AgCl溅射靶中超低水平129I的AMS分析方法,为避免AgI-AgCl粉末与铝发生反应,选择了铜代替铝作为试样夹持材料。选择Nb粉作为导热和导电基体并与AgI-AgCl粉混合,以获得并保持稳定的高碘离子电流强度、低记忆效应和较低的129I本底水平。Dang等[125]利用阴离子交换色谱法和CHCl3萃取法研究了从天然水有机物中释放碘的化学氧化方法,证实了K2S2O8是分解有机物并将有机碘转化为无机碘的理想氧化剂。在最佳条件下氧化后,通过溶剂萃取分离了天然水中超过95%的碘,并且在氧化过程中,无机和有机形式的碘完成了同位素交换,得到与原始水中相同的129I/127I比值,该化学氧化法适用于天然水中释放有机碘,可以分离碘并制备AgI靶。未来,AMS将向着更小型、易操作、易维护的方向发展,使得AMS的应用范围进一步扩大[80]。
放射性碘同位素的分析,除了核工业正常生产中的分析需求以及对核事故周边环境中高浓度碘同位素的监测,人们关注更多的是对环境水平中超痕量129I的分析。其中应用最多的是利用AMS的离子剥离技术和重离子探测器技术解决这一问题,从而达到较低的本底和检出限。
3.3 碘形态的分析
质谱分析碘形态时需要结合分离技术,色谱与ICP-MS联用已成为痕量碘形态分析的有力工具,其中最常见的是HPLC与ICP-MS的结合。该技术可使待测元素从复杂基质中有效分离,常用于复杂样品中碘形态的分析。Doh等[55]用HPLC-ICP-MS法分离鲍鱼中生物有效碘,将鲍鱼样品进行体外透析,采用阴离子交换柱的HPLC系统,在等比例洗脱条件下,用175 mmol/L硝酸铵加5%(V/V)甲醇(pH 4.9)组成的流动相,在单一色谱中分离4种碘(碘化物、碘酸盐、3-碘-L-酪氨酸和3,5-二碘-L-酪氨酸),并验证了HPLC-ICP-MS系统的可靠性。Trinta等[56]利用HPLC-ICP-MS对母乳中必需的微量元素(铁、铜、锌和碘)进行化学形态分析,将母乳乳清注入HPLC,通过柱(流动相0.01 mol/L Tris-HCl,pH 7,流速0.8 mL/min)分离后,进行紫外检测,随后HPLC的流出物立即被引入ICP-MS中,使用反应碰撞池测定同位素(54Fe、56Fe、63Cu、65Cu、68Zn和127I)的信号,以消除多原子干扰。Han等[57]用离子对反相HPLC-ICP-MS法测定海藻和海水中的无机碘(I-和IO3-)和有机碘化氨基酸(MIT和DIT),采用2.0 mmol/L四乙基氢氧化铵、10 mmol/LL-苯丙氨酸和1%甲醇(pH 8.9)作为反相C18色谱柱的流动相,流动相流速1.5 mL/min,柱温25 ℃,IO3-、I-、MIT和DIT的检出限分别为0.061、0.052、0.079、0.24 μg/L。海藻和海水样品中IO3-、I-、MIT和DIT的回收率在90%~110%之间。该方法环境友好、耗时短、灵敏度高,可用于环境和食品领域碘形态的常规分析。
为了更好地测定有机碘化合物并鉴定其结构,一些研究人员建立液相色谱-高分辨质谱(LC-HRMS)测定有机碘的方法。Yang等[134]首先使用LC-HRMS采集产物碘离子的提取离子色谱图,确定未知有机碘化合物的保留时间,通过MS/MS实验并参考标准品信息获得结构信息,再通过鉴定海藻中未知的有机碘化合物证明方法的可行性。在此方法的基础上,Yun等[135]利用LC-HRMS技术鉴定了不同食用碘盐中的有机碘化合物,从中国海藻碘盐中鉴定出38种有机碘化合物及其转化产物。在该研究中,只有能够被C18固相萃取柱吸收并被甲醇溶剂解吸的化合物才能通过LC-HRMS进行分析。此外,其他类型液相色谱与ICP-MS联用的技术也可用于碘形态分析。Yoshida等[136]利用IC分离系统与ICP-MS的联用技术实现了对水样中I-和IO3-的分离和测定,检出限为0.1~1 μg (I)/L,该方法已成功应用于雨水、河水、盐水和土壤溶液等不同类型的环境样品。Kozai等[137]使用尺寸排阻色谱(SEC)在线耦合至紫外可见(UV-Vis)检测以及ICP-MS技术分析地下水中的胶体和离子,并重点研究了铀和碘的形态。Wuilloud等[138]利用尺寸排阻液相色谱-在线UV-ICP-MS法对牛肝菌中多元素形态进行分离和测定,并开发和评估了从蘑菇中提取有机金属物质的不同方法。
高分离能力的色谱与高灵敏度的ICP-MS或HRMS相结合,实现了对痕量碘形态的分析,同时还可以消除复杂基质的干扰。该技术的发展将进一步扩大质谱测定碘的应用领域。
4 总结
碘的性质活泼且易挥发,制样过程中如果处理不当会造成碘的损失和仪器污染,影响测量结果的准确性。ICP-MS分析复杂基质样品时,如果处理不当会造成雾化器堵塞;在AMS分析中,为了制备靶样,在对样品进行消解后,还需要进一步分离富集和纯化。因此,碘测量结果的准确性不仅取决于仪器和测量方法的选择,还与前处理方法密切相关。
ICP-MS和AMS是目前测量碘最主要的两种分析仪器。ICP-MS的发展着力于应对基质更加复杂的样品和解决测量过程中的干扰问题,其灵敏度不断提高。同时,ICP-MS与进样、分离系统的联用技术也在不断发展。AMS将朝着更加小型化和更高灵敏度的方向发展。
在样品前处理方面,目前用于ICP-MS分析的碘样品前处理方法主要有碱提取法、酸消解法、热水解法、干灰化法、燃烧法和与微波辅助相结合的综合手段,以及简便、快速的直接进样方法。这些样品前处理方法促使ICP-MS测碘技术的应用范围不断扩大。用于AMS分析的碘样品在进行消解和碘提取后,还需要进一步分离富集和纯化,主要方法有:溶剂萃取法、离子交换色谱法、AgI直接沉淀法、AgI-AgCl共沉淀法等。对于低碘含量的样品,一般需要加入稳定碘载体,然后制成高稳定性的AgI沉淀,但对于超低129I水平的样品,由于稳定碘载体中存在少量的129I,会对测量结果的准确度造成影响,通常选择无载体或AgI-AgCl共沉淀的方法。合适的样品前处理方法不仅能提高前处理过程中碘的回收率,还能减小对仪器造成的损害。
在碘的测量方法方面,主要以ICP-MS为主。尽管碘的电离效率很低,ICP-MS对碘的测量灵敏度低于其他元素,但仍高于常见的分析方法。随着ICP-MS抗干扰技术、质量检测器技术、联用技术的不断发展,ICP-MS对复杂基质中的总碘、碘同位素、碘形态的测量方法已有大量研究。AMS是目前测定129I最灵敏的技术,也是测量129I/127I原子比低于10-10的核前年代样品的唯一方法,AMS在环境水平129I的分析测定中有着不可代替的地位。

