9种植物源多酚的分离提取及其涩感评价
刘佩 杜国荣 赵鹏涛 张倩婷 王升楠 王晓宇


摘要: 为探究不同植物源多酚物质的理化性质差异及其感官潜质,以9种不同植物材料为研究对象,经提取、分离和纯化后获得多酚提取物,并对其总酚含量、总黄烷醇含量、鞣花单宁含量、蛋白质结合能力、蛋白质沉降能力、涩感及颜色等指标进行分析。结果表明,在9种植物原料中,绿茶、红茶、石榴皮和木瓜皮中总酚物质含量较高,是酚类物质提取的优质原料。唾液蛋白沉降指数(SPI)试验结果表明,供试多酚提取物的蛋白质沉降能力与其总酚含量呈正相关关系。鞣花单宁通过影响蛋白质结合能力进而影响多酚提取物的涩感强度。
关键词: 多酚;鞣花单宁;涩感;蛋白质结合能力
中图分类号: TS255.1 文献标识码: A 文章编号: 1000-4440(2021)04-1025-08
Separation and extraction of nine plant polyphenols and evaluation of astringency
LIU Pei1, DU Guo-rong2, ZHAO Peng-tao1,3,4, ZHANG Qian-ting1, WANG Sheng-nan1, WANG Xiao-yu1,3,4
(1.College of Food Engineering and Nutritional Science, Shaanxi Normal University, Xian 710119, China;2.School of Biological and Environmental Engineering, Xian University, Xian 710065, China;3.National Research & Development Center of Apple Processing Technology, Xian 710119, China;4.Engineering Research Center of High Value Utilization of Western China Fruit Resources, Xian 710119, China)
Abstract: In order to explore the differences in physicochemical properties and organoleptic quality of polyphenols extracted from different plant sources, nine different plant materials were studied. After extraction, separation and purification, the polyphenol extracts were obtained, and its total phenol content, total flavanol content, ellagitannin content, protein binding capacity, protein sedimentation capacity, astringency and color were analyzed. The results showed that among the nine plant materials, green tea, black tea, pomegranate peel and papaya peel had high total phenol content, which were high-quality raw materials for polyphenols extraction. The results of salivary protein sedimentation index (SPI) test showed that the protein sedimentation capacity of the tested polyphenol extract was positively correlated with total phenol content. Ellagitannin affects the astringency intensity of polyphenol extracts by affecting the protein binding capacity.
Key words: polyphenols;ellagitannin;astringency;protein binding capacity
多酚是高等植物的次級代谢产物,其结构复杂,具有多种功效,能够调节免疫系统,预防高血糖和高血脂等慢性疾病[1-2]。植物中的酚类物质不仅具有保健作用,还可通过键合作用与蛋白质相互作用形成复合物,并影响茶、咖啡、葡萄酒、啤酒等饮料食品的风味和色泽[3-5]。如从五味子、橡木、绿茶及葡萄籽中提取的多酚化合物[6],可用于改善葡萄酒的涩感与颜色[7-8]。涩感是由多酚与唾液蛋白结合所形成干燥、粗糙、褶皱的味感,对食品独特口感的形成起到了不可替代的作用[9],多酚与蛋白质的相互作用也是近年来的研究热点[10]。
食品加工副产物中的酚类物质虽受到研究学者的关注,但主要集中于多酚物质的抗氧化功能,而对多酚物质的感官特性研究较少。一些植物废弃物如板栗壳、葡萄皮、葡萄籽,其多酚提取物常作为添加剂用于葡萄酒酿造,以调节葡萄酒的涩感及颜色,提升其感官品质。许多植源性食物富含多酚类物质,具有巨大的应用潜力,但其多酚类物质的利用率较低,且在加工中许多副产物常被作为生产垃圾废弃,造成了资源浪费和环境污染问题。因此研究植物多酚物质的理化特性与其感官潜质具有一定意义。
目前,从绿茶、板栗壳、葡萄皮、葡萄籽中提取的多酚是市场上应用较广的食品添加剂,通过前期的试验研究发现石榴皮、木瓜皮、山楂、红茶和高粱壳是优质的酚类提取原料且具有应用潜力。因此,本试验以这9种植物源多酚为研究对象,对其酚类物质进行提取、纯化后获得多酚提取物,并在测定其总酚含量、总黄烷醇含量的同时,通过荧光光谱法和聚丙稀酰胺凝胶电泳(SDS-PAGE)来研究多酚与蛋白质的结合和沉降能力,通过色差测定和感官鉴评对多酚提取物的颜色及涩感进行分析,为其作为食品添加剂用于调节食物的色泽和味感提供理论依据,以期挖掘这些植物资源的应用潜力,提高综合利用效益。
1 材料与方法
1.1 材料与仪器
石榴、红茶、板栗、高粱壳、葡萄、木瓜皮、绿茶、山楂,购自华润万家超市;福林酚试剂、对二甲氨基肉桂醛(DMACA)、考马斯亮蓝(R250)、牛血清白蛋白(BSA,98%)、三羟甲基氨基甲烷(TRIS),美国Sigma公司产品;氯化钠、碳酸钠、浓盐酸、甘氨酸、十二烷基硫酸钠(SDS)、丙三醇、甲醇、冰乙酸,购自天津天力化学试剂公司;SDS-PAGE凝胶制备试剂盒、4×蛋白上样缓冲液,购自北京索莱宝科技有限公司;低相对分子质量标准蛋白质(1.0×104~1.80×105),购自中国科学院上海生物化学研究所。
RF-6000型荧光分光光度计,上海分析仪器厂产品;DYCZ-24DN 电泳仪,北京六一仪器厂产品;KQ 5200DE RE-52旋转蒸发器,上海安亭科学仪器厂产品;TGL-16B高速台式离心机,上海安亭科学仪器厂产品;UV2600A紫外分光光度计,尤尼柯(上海)仪器有限公司产品;SC-80C全自动色差仪,北京康化仪器有限公司产品;LGJ-18C真空冷冻干燥机,北京四环科学仪器厂产品; 高效液相色谱仪(DAD)U-3000,美国热电公司产品。
1.2 试验方法
1.2.1 多酚物质的提取 对试验材料进行前处理,获得石榴皮、红茶、板栗壳、高粱壳、葡萄皮、木瓜皮、葡萄籽、绿茶和山楂皮,再将它们置于35 ℃烘箱中烘干。除葡萄籽外,对其他样品进行破碎。再取上述9种样品各10 g,置于盛有100 ml 70%乙醇的三角瓶中,将三角瓶置于转速为180 r/min的摇床中浸提5 h,之后经布式漏斗过滤、旋转蒸发仪蒸发除去乙醇后用蒸馏水定容到50 ml,即得到酚类物质粗提液,置于4 ℃的冰箱中保存备用。
1.2.2 多酚物质的纯化 AB-8大孔树脂经95%乙醇浸泡24 h充分溶胀后,置于玻璃层析柱中,用95%乙醇流动清洗至无浑浊,再用蒸馏水冲洗。将酚类粗提液上柱,静置吸附饱和后,用蒸馏水洗脱除去蛋白质、多糖等杂质,洗脱液pH为7时即为洗脱终点,再用2倍柱体积的60%乙醇进行洗脱[11]。将洗脱液旋蒸浓缩后,转移至真空冷冻干燥机进行干燥处理后低温保存。
1.2.3 理化指标的测定
1.2.3.1 总酚、总黄烷醇含量测定 总酚含量测定采用福林酚法[12],总酚含量以没食子酸计(mg/L),以没食子酸标准溶液浓度为横坐标,以在765 nm波长处所测吸光值为纵坐标,所得标准曲线方程为Y=0.001 4x-0.000 6,R2=0.999 2。总黄烷醇含量测定采用4-(二甲基氨基)肉桂醛法(DMACA)[13],总黄烷醇含量以儿茶素计(mg/L),以儿茶素标准溶液浓度为横坐标,以在640 nm波长处所测吸光值为纵坐标,所得标准曲线方程为Y=0.009 3x-0.004 2,R2=0.999 7。所有指标均重复测定3次,将吸光度代入标准曲线回归方程计算溶液中总酚、总黄烷醇含量,按公式(1)计算总酚、总黄烷醇提取率。
W=C×Vm(1)
式中,W为多酚(总黄烷醇)提取率(mg/g),C为提取液中多酚(总黄烷醇)的质量浓度(mg/ml),V为提取液的总体积(ml),m为取样量(g)。
1.2.3.2 鞣花单宁含量测定 鞣花单宁含量测定采用高效液相色谱(HPLC)法。先配制不同多酚提取物甲醇溶液,调整其质量浓度为5 g/L,取1 ml多酚提取物甲醇溶液与1 ml浓盐酸(2 mol/L)在100 ℃下反应2 h[14]。色谱条件如下:Waters XBridge Shield RP18柱(4.6 mm×250.0 mm, 3.5 μm),检测波长为370 nm,柱温为30 ℃,进样量为10 μl,流速为0.6 ml/min。以2%甲酸为水相,以乙腈为有机相,洗脱梯度:0~5 min,0~10%乙腈; 5~10 min,10%~25%乙腈; 10~40 min,25%~35%乙腈。
1.2.3.3 SDS-PAGE分析 唾液的收集与处理参考Zhang等的方法[15],招募4名身体健康且不抽烟的志愿者参加试验,其中男女比例为1∶1,于上午11∶00左右收集其唾液(要求收集前2 h不得摄入食物和饮料)并且混合,然后用离心机在10 000 r/min的条件下离心5 min,取其上清液即为所需的唾液蛋白样品(SP)。
用SDS-PAGE对唾液蛋白进行分离、分析,其中相对分子质量5.4×104~5.9×104和1.5×104附近的蛋白质与涩感相关性最高。用相机将脱色后的凝膠进行拍照,再用化学发光成像仪器对图片进行光分析,记录光密度值,计算样品与唾液蛋白结合前、后蛋白质条带(5.4×104~5.9×104和1.5×104)光密度值降低的百分比,即得到唾液蛋白沉降指数(SPI)[16],用来分析葡萄酒与蛋白质的结合能力,预测涩感强度。
样品前处理:分别取9种多酚提取物溶于30%的乙醇,得到2 g/L的多酚乙醇溶液,将其与唾液蛋白(HS)以1∶2(V/V)的比例进行混合并反应5 min,之后在离心力为10 000 g的条件下离心10 min,将上清液与4×上样缓冲液以3∶1(V/V)的比例混合后煮沸5 min [17]。
测定条件:Marker上样量为10 μl,样品15 μl;初始电压为100 V,通过分离胶区域时电压调整为120 V;经0.1%的考马斯亮蓝染色后,在脱色液(10%冰乙酸,10%甲醇)中脱色,每30 min更换一次脱色液,直至脱色液无色为止。
1.2.3.4 荧光光谱分析 取10 mg多酚提取物与10 ml的5×10-6mol/L的BSA溶液充分混合后静置5 min使其充分反应,之后在280 nm的波长处进行光谱扫描,扫描速度为600 nm/min,激发和发射狭缝宽度分别为5 nm和10 nm,数据间隔为0.2 nm,波长范围为285~450 nm。
1.2.3.5 感官鉴评 感官鉴评小组由11名经过专门感官训练的食品专业学生组成。小组成员首先接受培训,使他们熟悉涩感强度范围。首先采用硫酸奎宁(0.25 g/L)、硫酸铝(3.00 g/L)、和酒石酸(4.00 g/L)水溶液来确定苦味、涩味和酸味。再分别用50 mg/L、500 mg/L、1 000 mg/L、2 000 mg/L和4 000 mg/L的硫酸铝对小组成员进行收敛性培训,确定主要感受到的收敛性浓度范围。按照0~10分制对不同质量浓度的单宁模型溶液(50 mg/L、500 mg/L、1 000 mg/L、2 000 mg/L和3 000 mg/L)的收敛性进行评估(表1),以确定成员在品尝不同样品之间的重复性[18]。感官品尝环境为室温,品尝溶液为10 ml溶于30%乙醇的多酚溶液(1 g/L),保持8 s后吐出,之后用去离子水清洁口腔2次,等待30 s后品尝下一个样品。每个多酚溶液的评价在5 min内完成,按照培训的标准对涩感进行评分[19]。
1.2.3.6 多酚溶液颜色的测定 利用色差计测定不同多酚溶液颜色参数:亮度 (L*),其值越大,亮度越高;红度 (a*),正值表示接近红色,负值表示接近绿色;黄度 (b*),正值表示接近黄色,负值表示接近蓝色。总色差 (△E*) 使用下列公式(2)计算:
△E*= (△L*)2+(△a*)2+(△b*)2(2)
式中,△L*、△a*和△b*是处理样品颜色值与空白对照样品颜色值之间的差值。
1.3 数据处理
各试验组均重复3次,测定结果用“平均值±标准差”表示。数据进行单因素方差分析(ANOVA)、Pearson相关性分析以及Duncans显著性分析。P<0.05为显著性。数据用SPSS 18.0处理,图、表使用originPro 9绘制。
2 结果与分析
2.1 不同原料中酚类物质含量的比较
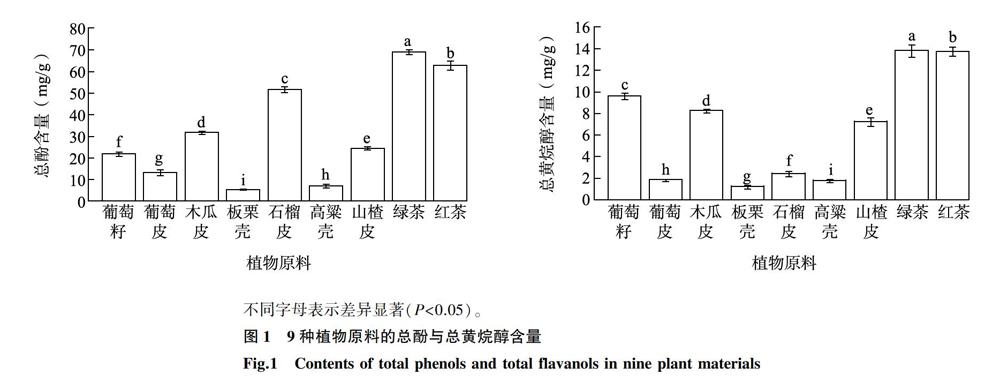
不同食物原料中酚类物质的含量差异见图1。由图1可知,绿茶、红茶和石榴皮的总酚含量较高,均达到50 mg/g以上;而葡萄籽、木瓜皮和山楂皮的总酚含量为20~35 mg/g,葡萄皮、板栗壳和高粱壳的总酚含量较低,均低于20 mg/g;葡萄皮、籽的总酚含量分别为13.12 mg/g和21.76 mg/g,与Canals等人的研究结果基本一致[20]。绿茶和红茶中黄烷醇类物质含量较高,分别为13.79 mg/g和13.74 mg/g,这是由于绿茶中儿茶素含量占茶多酚总量的70%~80%, 红茶中含有较多的茶黄素等黄烷醇氧化产物[21-22]。葡萄籽、木瓜皮和山楂皮的总黄烷醇含量为7.25~9.61 mg/g,葡萄皮、板栗壳、石榴皮和高粱壳的总黄烷醇含量较低,其含量为1.26~2.47 mg/g。石榴皮的总酚含量很高,但是总黄烷醇含量较低,可能是因为石榴皮中的多酚主要是水解单宁[23]。
2.2 多酚提取物中总酚、总黄烷醇含量
酚类化合物通常被分成2类:类黄酮物质和非类黄酮物质。类黄酮包括花青素和黄烷醇,其中黄烷醇是苦味以及与收敛性相关的主要成分。不同原料多酚提取物中总酚、总黄烷醇含量差异见图2。从图2可知,9种多酚提取物中的总酚含量在250.43~523.05 mg /g。多酚提取物中总酚含量由高到低分别是石榴皮、山楂皮、木瓜皮、板栗壳、葡萄皮、葡萄籽、绿茶、红茶、高粱壳,分别为523.05 mg /g、464.95 mg /g、425.19 mg /g、390.90 mg /g、306.14 mg /g、302.81 mg /g、263.29 mg /g、254.24 mg /g和250.43 mg/g。由图2可知,总黄烷醇含量最低和最高的是石榴皮和葡萄籽多酚提取物,含量分别为13.71 mg /g和172.57 mg /g,这是因为葡萄籽中含有较多的儿茶素、表儿茶素和表儿茶素没食子酸酯等黄烷醇类物质,而石榴皮多酚提取物中黄烷醇含量很少[24-26]。
2.3 多酚提取物中鞣花单宁含量
植物中单宁按结构可分为缩合单宁和水解单宁,缩合单宁由黄烷-3-醇单体、二聚体以及高聚物组成,水解单宁是葡萄糖的单糖酯连接至少一个没食子酸(没食子单宁)或鞣花酸(鞣花单宁)形成。多年来,缩合单宁一直被认为是与收敛性有关的单宁,但一些人类感官试验结果表明鞣花单宁也可影响收敛性 [27]。多酚提取物中鞣花单宁含量见图3,在葡萄籽、葡萄皮、木瓜皮和山楂皮中未检测到鞣花单宁,高粱壳、绿茶和红茶中鞣花单宁含量均低于5 mg/g,板栗壳和石榴皮中鞣花单宁含量分别为25.27 mg/g和46.90 mg/g。此结果与其他研究学者的试验结果基本吻合,Russo等[28]和张建伟等[29]分别发现石榴皮和板栗壳中的鞣花单宁含量豐富。
2.4 不同多酚提取物与蛋白质沉降能力的比较
对不同多酚提取物进行电泳分析,测定在1.5×104和5.4×104~5.9×104这2条蛋白质条带处的光密度值,并计算唾液沉降指数(SPI)(图4)。由图4可知,木瓜皮、石榴皮、高粱壳和山楂皮多酚提取物的SPI较高,表明其蛋白质沉降能力较强;葡萄皮、葡萄籽、红茶和绿茶多酚提取物的SPI较低。以9种不同多酚提取物的多酚含量为横坐标,SPI为纵坐标,所得线性拟合方程为Y=0.169 1x-6.757 2,R2=0.934 5,表明总酚含量与SPI存在正相关性,多酚提取物中总酚含量越高,其与蛋白质的沉降能力越强。
2.5 不同多酚提取物与蛋白质的结合能力
由9种多酚提取物与BSA相互作用后的荧光光谱峰值(图5)可知,与蛋白质结合能力从强到弱依次为石榴皮、木瓜皮、板栗壳、高粱壳、红茶、绿茶、葡萄籽、山楂皮和葡萄皮多酚提取物。由以9种不同多酚提取物与BSA的荧光差值为横坐标,分别以总酚含量、总黄烷醇含量和鞣花单宁含量为纵坐标,进行Pearson拟合,得到R2分别为0.006 27、0.426 21和0.213 93,表明多酚提取物与蛋白质结合能力与总酚含量、总黄烷醇含量和鞣花单宁含量不构成线性关系。由图2与图3可知,总酚和总黄烷醇含量较高的多酚提取物表现出较低的蛋白质结合能力,而鞣花单宁含量较高的多酚提取物却表现出很高的蛋白质结合能力,表明总酚与总黄烷醇对多酚提取物蛋白质结合能力的影响较小,但鞣花单宁会影响蛋白质结合能力。板栗壳和石榴皮的多酚提取物蛋白质结合能力较强,可能是因为它们含有大量鞣花单宁会通过疏水作用和氢键与BSA结合生成不具有荧光特性的复合物[30]。上述结果表明多酚提取物中总酚含量与蛋白质结合能力关系不大,但与多酚的种类具有一定的关联。
2.6 不同食物源多酚提取物的涩感
不同多酚提取物的涩感差异见图6,多酚提取物涩感评分由低到高分别为石榴皮、板栗壳、木瓜皮、高粱壳、红茶、绿茶、葡萄籽、山楂皮和葡萄皮多酚提取物。9种多酚提取物中,石榴皮涩感强烈;板栗壳、木瓜皮、高粱壳和红茶涩感较强,口感粗糙;绿茶、葡萄籽和山楂皮多酚提取物有干燥、褶皱的味感;葡萄皮多酚提取物涩感较弱。以9种不同多酚提取物与BSA荧光差值为横坐标,涩感强度为纵坐标,所得线性拟合方程为Y=1.331 4x+4.058 8,R2=0.933 9,多酚提取物的涩感强度与其荧光差值呈正相关关系,表明多酚提取物涩感强度与其蛋白质结合能力存在一定的相关性。
2.7 不同食物源多酚提取物的色度
不同多酚提取物的颜色差异见表2。对色泽指标 L*、 a*、 b*和总色差值△E分别进行Duncans显著性分析,结果显示除葡萄籽和板栗壳以外的多酚提取物L*值间均存在显著差异,除葡萄籽和红茶以外的酚提取物a*值差异显著,除葡萄籽和石榴皮以外的多酚提取物b*值差异显著,葡萄籽和山楂皮以外多酚提取物的△E*间存在显著差异。
以9种不同多酚提取物的颜色参数L*、 a*、 b*和△E*作为横坐标,分别以总酚含量、总黄烷醇含量和鞣花单宁含量为纵坐标,进行Pearson拟合,得到的12组R2值均小于0.6,表明多酚提取物颜色参数与总酚含量、总黄烷醇含量和鞣花单宁含量无线性关系。
由表2可知葡萄皮和高粱壳多酚提取物的a*值较高但L*值较低,表明它们的透光性因红色较深而相对较差,这与葡萄皮中花色苷含量和高粱壳中红色素含量较高有一定的关联[24,30]。红茶和高粱壳多酚[31]提取物的L*值和b*值均较高,表明黄色对其透光性影响较小。以上结果表明,多酚提取物被应用于食品时,同等添加条件下,9种植物源中葡萄皮和高粱壳多酚提取物会对食物的色泽产生较大影响,其余7种对色泽影响程度相对较小。
3 结论
高粱殼、葡萄皮、木瓜皮等9种植物源提取物的酚类物质含量差异明显,总酚含量范围为5.32~69.05 mg/g,其中板栗壳和石榴皮中鞣花单宁含量较高。9种植物提取物的总酚含量与其蛋白质沉降能力呈正相关关系,总酚含量高更容易呈现较强的蛋白质沉降能力。总酚与总黄烷醇含量对多酚提取物的蛋白质结合能力影响不大,而鞣花单宁含量会直接影响多酚提取物的蛋白质结合能力。多酚提取物的涩感强度与其蛋白质的结合能力有一定的关联,鞣花单宁含量较高的板栗壳和石榴皮的多酚提取物涩感相对较强。对这9种植物多酚的化学性质以及感官特性的研究,可以为这些植物提取的多酚在食品工业中的应用提供理论依据。
参考文献:
[1] VISIOLI F, DE LALASTRA C A, ANDRES-LACUEVA C, et al. Polyphenols and human health: a prospectus[J]. Critical Reviews in Food Science & Nutrition, 2011, 51(6):524-546.
[2] DE ARAJO F F, FARIAS D D P, NERI-NUMA I A, et al. Polyphenols and their applications: an approach in food chemistry and innovation potential [J]. Food Chemistry, 2020, 338:127535.
[3] CHEYNIER V. Polyphenols in foods are more complex than often thought [J]. American Journal of Clinical Nutrition, 2005, 81(1 Suppl):223-229.
[4] SOARES S, BRANDO E, GUERREIRO C, et al. Tannins in food: insights into the molecular perception of astringency and bitter taste [J]. Molecules, 2020, 25(11): 2590.
[5] GARCA-ESTVEZ I, ALCALDE-EON C, PUENTE V, et al. Enological tannin effect on red wine color and pigment composition and relevance of the yeast fermentation products [J]. Molecules, 2017, 22(12): 2046.
[6] RICCI A, OLEJAR K J, PARPINELLO G P, et al. Antioxidant activity of commercial food grade tannins exemplified in a wine model[J]. Food Additives & Contaminants, 2016, 33(12):1761-1774.
[7] MA W, GUO A Q, ZHANG Y L, et al. A review on astringency and bitterness perception of tannins in wine [J]. Trends in Food science & Technology, 2014, 40(1):6-19.
[8] NIKOLANTONAKI M, DAOUD S, NORET L, et al. Impact of oak wood barrel tannin potential and toasting on white wine antioxidant stability [J]. Journal of Agricultural and Food Chemistry, 2019, 67(30):8402-8410.
[9] 李 超,李 輝,孙佳莹,等.多酚化合物单宁对葡萄酒口感影响的研究进展[J].北方园艺, 2017(4):182-186.
[10]姚其凤,吴正奇,陈小强,等.茶多酚-蛋白质相互作用的研究进展[J].食品工业科技,2019, 40(8):337-342,349.
[11]季 红,贾 荣,郭 鑫.大孔树脂对山葡萄籽多酚提取物的纯化工艺优选[J].吉林大学学报(医学版),2017,43(6):1272-1277.
[12]SINGLETON V, ROSSI J A. Colorimetry of total phenolics with phosphomolybdic-phosphotungstic acid reagents [J].American Journal of Enology & Viticulture, 1964, 16 (3):144-158.
[13]LI Y G, TANNER G, LARKIN P. The DMACA-HCl protocol and the threshold proanthocyanidin content for bloat safety in forage legumes [J].Journal of the science of Food & Agriculture, 2015, 70(1):89-101.
[14]MICHEL J, JOURDES M, LE FLOCH A, et al. Influence of wood barrels classified by NIRS on the ellagitannin content/composition and on the organoleptic properties of wine[J].Journal of Agricultural & Food Chemistry, 2013, 61(46):11109-11118.
[15]ZHANG Q T, CHEN T G, WANG X Y, et al. Influence of simulated grape crushing process on phenolic compounds extraction, astringency and color of Cabernet Sauvignon model wine[J].LWT- Food Science and Technology, 2020, 128:109514.
[16]RINALDI A, GAMBUTI A, MOIO L. Application of the SPI (saliva precipitation index) to the evaluation of red wine astringency[J].Food Chemistry, 2012, 135(4):2498-2504.
[17]LEI X Q, ZHU Y Y, WANG X Y, et al. Wine polysacch arides modulating astringency through the interference on interaction of flavan-3-ols and BSA in model wine [J].International Journal of Biological Macromolecules, 2019, 139:896-903.
[18]BASALEKOU M, KYRALEOU M, PAPPAS C, et al. Proanthocyanidin content as an astringency estimation tool and maturation index in red and white winemaking technology[J].Food Chemistry,2019, 299(30):125-135.
[19]马 婧.红葡萄酒涩感的化学评价方法研究[D].杨凌:西北农林科技大学,2015.
[20]CANALS R, LLAUDY M C, VALLS J, et al. Influence of ethanol concentration on the extraction of color and phenolic compounds from the skin and seeds of Tempranillo grapes at different stages of ripening [J].Journal of Agricultural & Food Chemistry, 2005, 53(10):4019-4025.
[21]张英娜,嵇伟彬,许勇泉,等.儿茶素呈味特性及其感官分析方法研究进展[J].茶叶科学,2017,37(1):1-9.
[22]ROBERTSON A, BENDALL D S. Production and HPLC analysis of black tea theaflavins and thearubigins during in vitro oxidation [J].Phytochemistry, 1983, 22(4):883-887.
[23]CAM M, HISIL R. Pressurised water extraction of polyphenols from pomegranate peels [J].Food Chemistry, 2010,123 (3):878-885.
[24]GONZLEZ-MANZANO S, RIVAS-GONZALO J C, SANTOS-BUELGA C. Extraction of flavan-3-ols from grape seed and skin into wine using simulated maceration [J].Analytica Chimica Acta, 2004, 513(1):283-289.
[25]DU LI J, HUANG J P, WANG B, et al. Carbon molecular sieve based micro-matrix-solid-phase dispersion for the extraction of polyphenols in pomegranate peel by UHPLC-Q-TOF/MS.[J].Electrophoresis, 2018, 39(17):2217-2218.
[26]AMBIGAIPALAN P, DE CAMARGO A C, SHAHIDI F. Phenolic compounds of pomegranate byproducts (outer skin, mesocarp, divider membrane) and their antioxidant activities [J].Journal of Agricultural & Food Chemistry, 2016, 64(34):6584-6604.
[27]MICHEL J, JOURDES M, LE FLOCH A, et al. Influence of wood barrels classified by NIRS on the ellagitannin content/composition and on the organoleptic properties of wine[J].Journal of Agricultural & Food Chemistry, 2013, 61(46):11109-11118.
[28]RUSSO M, FANALI C, TRIPODO G, et al. Analysis of phenolic compounds in different parts of pomegranate (Punica granatum) fruit by HPLC-PDA-ESI/MS and evaluation of their antioxidant activity: application to different Italian varieties[J].Analytical & Bioanalytical Chemistry, 2018, 410(15):3507-3520.
[29]張建伟.板栗壳斗鞣花单宁及其代谢产物鞣花酸和尿石素的生物活性研究[D].北京:北京林业大学, 2015.
[30]SOARES S, MATEUS N, FREITAS V D. Interaction of different polyphenols with bovine serum albumin (BSA) and human salivary alpha-amylase (HSA) by fluorescence quenching[J].Journal of Agricultural and Food Chemistry, 2007, 55(16): 6726-6735.
[31]王金亭.天然高粱壳红色素研究与应用进展[J].粮食与油脂,2012,25(11):7-11.
(责任编辑:张震林)
收稿日期:2020-12-18
基金项目:陕西省重点研发计划项目(2020ZDLNY05-08);西安市农业项目(20193041YF029NS029)
作者简介:刘 佩(1996-),女,陕西安康人,硕士研究生,主要从事葡萄酒化学研究。(Tel)17809297966;(E-mail)liupei123@snnu.edu.cn
通讯作者:王晓宇,(E-mail)wangxiaoyu@snnu.edu.cn

