百蕊草根系总RNA提取方法比较及优化
刘波 张晓明 郭巧生 等
摘要:百蕊草根系富含多糖、多酚和其他次生代谢产物,用传统方法提取总RNA难以有效将这些杂质去除。以百蕊草根系为材料,比较TRIzol法、CTAB-LiCl法、SDS/酚法及改进TRIzol法4种方法对百蕊草根系总RNA的提取效果,并以电泳检测、D260 nm/D280 nm比值测定、RT-PCR试验等对结果进行分析评价。结果表明,4种方法均能提取百蕊草根中总RNA,提取效果差异显著;改进TRIzol法提取总RNA的28S和18S条带清晰,无弥散,28S亮度比18S加倍,完整性好,无明显DNA或其他杂质污染,D260 nm/D280 nm值为1.8~2.0,D260 nm/D230 nm值大于2.0,总RNA得率仅次于TRIzol法;用改进TRIzol法提取总RNA,反转录cDNA片段大小分布在0.2~2.5 kb,可扩增出目的基因片段,提取的总RNA完全适用于后续的分子生物学研究。
关键词:百蕊草;总RNA提取;多糖;多酚;TRIzol法;RT-PCR
中图分类号: Q522文献标志码: A文章编号:1002-1302(2015)01-0044-03
收稿日期:2014-03-25
基金项目:国家自然科学基金(编号:81202867)。
作者简介:刘波(1989—),男,浙江衢州人,硕士,主要从事药用植物栽培生理研究。E-mail:2011104175@njau.edu.cn。
通信作者:郭巧生,博士,教授,主要从事药用植物资源开发。E-mail:gqs@njau.edu.cn。百蕊草(Thesium chinense Turcz.)为檀香科百蕊草属半寄生植物,全草入药,具有清热解毒、止咳化痰等功效[1],被称为植物抗生素[2],具有重要的药用价值。百蕊草根系可形成寄生根侵入寄主植物[3-4],通过寄生根从寄主植物获得水分和养分。目前,对百蕊草的研究主要集中在药理成分、提取工艺、组织培养等方面[2,5-9],在分子水平上的研究较少,至今未见有关百蕊草根系总RNA提取方面的报道。
植物组织RNA的提取是开展后续植物分子生物学研究的必要前提。进行RT-PCR、cDNA合成、Northern印迹杂交、SSH筛选差异基因等分子生物学相关研究,均需要完整性好、纯度高的RNA。因此,如何提高RNA纯度和经济快捷获得足够量的RNA是当前研究人员十分关注的问题。百蕊草根系化学成分复杂,富含多糖及酚类物质[10]。酚类化合物容易氧化产生褐化效应[11],在RNA提取过程中与RNA不可逆结合,导致RNA降解或RNA活性丧失[12];多糖能与RNA共沉淀形成难溶的胶状物,抑制许多酶的活性[13]。为此,本试验开展TRIzol法、CTAB-LiCl法、SDS/酚法[14-16]、优化改进TRIzol法提取百蕊草根系总RNA研究,以期筛选出一种理想的百蕊草根系RNA提取方法,为今后利用分子生物学研究百蕊草寄生机理提供技术参考。
1材料与方法
1.1试验材料
野生百蕊草采集于南京市附近,选挖长势良好的植株,清洗根系,立即投入液氮中冷冻保存,备用。原植物经南京农业大学郭巧生教授鉴定为檀香科植物百蕊草。
1.2总RNA提取方法
1.2.1TRIzol法取0.1 g植物组织,在液氮中研磨至粉末状后转移到1.5 mL离心管中;加入1 mL预冷的TRIzol,涡旋混匀,室温放置5 min;加入200 μL氯仿,振荡1 min,室温放置15 min,4 ℃、12 000 r/min离心15 min;吸取上层水相至新离心管中,加入500 μL预冷的异丙醇,振荡混匀,室温放置 10 min,4 ℃、12 000 r/min离心10 min;弃上清,加入1 mL 75%乙醇,振荡,使沉淀浮起,悬浮1 min,4 ℃、7 500 r/min离心5 min;弃置上清,空气中干燥5 min,加入50 μL ddH2O溶解,-70 ℃保存。
1.2.2CTAB-LiCl法将2×CTAB 提取液于65 ℃水浴锅中预热;取0.2 g样品于液氮中研磨成粉末,转入2 mL离心管中,加700 μL提取液和20 μL β-巯基乙醇,剧烈振荡混匀;65 ℃水浴10 min,其间振荡数次,冷却到室温后加等体积比例为25 ∶24 ∶1的苯酚、氯仿、异戊醇混合液,充分振荡,冰浴10 min,4 ℃、12 000 r/min离心10 min;取上清至2 mL新离心管中,重复上述步骤,再抽提1次;取上清于1.5 mL离心管中,加入1/4体积的10 mol/L LiCl溶液,4 ℃过夜,4 ℃、12 000 r/min 离心20 min;弃上清,沉淀用500 μL ddH2O溶解,加等体积比例为24 ∶1的氯仿、异戊醇溶液再抽提1次,4 ℃、12 000 r/min离心10 min;上清液中加入1/10体积、pH值为52、浓度3 mol/L的乙酸钠和等体积预冷的异丙醇,-20 ℃ 沉淀3 h,4 ℃、12 000 r/min离心10 min;弃上清,用75%乙醇清洗沉淀,室温干燥,ddH2O溶解,-70 ℃保存。
1.2.3SDS/酚法取0.2 g样品于液氮中研磨成粉末,加入80 ℃预热的提取缓冲液850 μL;加入PVP和β-巯基乙醇,充分混匀,冰浴15 min,4 ℃、12 000 r/min离心15 min;上清液中加入1/3体积、pH值为4.8、浓度为5 mol/L的乙酸钾,冰浴15 min,4 ℃、12 000 r/min离心15 min;上清液中加入等体积、比例为24 ∶1的氯仿、异戊醇溶液,充分混匀,冰浴 10 min,4 ℃、12 000 r/min离心15 min;上清液中加入等体积预冷异丙醇,-20 ℃放置3 h,4 ℃、12 000 r/min离心15 min;弃上清液,用600 μL重悬缓冲液重悬沉淀,4 ℃、12 000 r/min离心15 min;75%乙醇清洗沉淀,室温干燥,ddH2O溶解,-70 ℃ 保存。
1.2.4改进TRIzol法在TRIzol法基础上,在加入TRIzol试剂的同时,加入20 μL β-巯基乙醇,用异丙醇沉淀后,加入500 μL ddH2O溶解沉淀,加入1/4体积的10 mol/L LiCl溶液,-20 ℃下静置6 h,4 ℃、12 000 r/min离心20 min;弃上清,沉淀用500 μL ddH2O溶解,加等体积比例为24 ∶1的氯仿、异戊醇溶液再抽提1次,4 ℃、12 000 r/min离心10 min;取上清,加1/10体积pH值为5.2、浓度为3 mol/L的乙酸钠和等体积预冷的异丙醇,-20 ℃沉淀3 h,4 ℃、12 000 r/min离心10 min;弃上清,用75%乙醇清洗沉淀,室温干燥,ddH2O溶解,-70 ℃保存。
1.3总RNA质量检测
1.3.1总RNA完整性检测分别取由4种总RNA提取方法获得的百蕊草根系总RNA,在1.2%非变性琼脂糖凝胶上电泳检测,3次重复。
1.3.2总RNA纯度及得率检测用紫外分光光度计测定所提取RNA样品的D230 nm、D260 nm、D280 nm值,计算D260 nm/D280 nm、D260 nm/D230 nm,评价总RNA纯度;同时,测定总RNA浓度并计算得率。
1.4改进TRIzol法提取总RNA完整性的RT-PCR检验
cDNA第1链的合成参照Thermo Scientific公司RevertAid First Strand cDNA Synthesis Kit操作说明书进行。采用25 μL PCR反应体系:1 μL逆转录产物, 1 μLTcActin正向引物:5′-ACCACTGCTGAGCGGGAAA-3′, 1 μL反向引物:5′-CTGCAATGCCAGGGAACA-3′,15.3 μL 灭菌ddH2O, 2.5 μL 10×PCR buffer,2 μL 25 mmol/L MgCl2 ,2 μL 2.5 mmol/L dNTP ,0.2 μL Taq DNA聚合酶。PCR反应程序为:94 ℃预变性5 min;94 ℃变性30 s,58 ℃退火30 s,72 ℃延伸1 min,28个循环;72 ℃延伸5 min。反应完毕后取5 μL于1.5%琼脂糖凝胶上进行电泳分析。
2结果与分析
2.1不同提取方法对总RNA完整性的影响
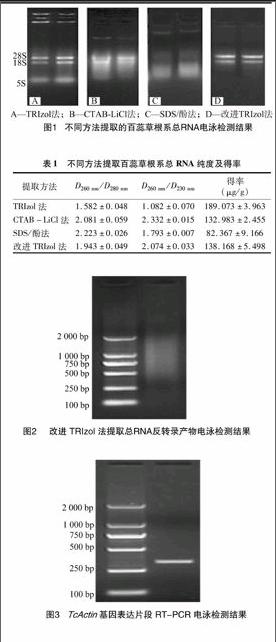
由图1可见,4种方法提取的总RNA完整性和基因组DNA残留程度有较大差异;TRIzol法提取的RNA电泳条带清晰,可见28S、18S、5S条带,且28S的亮度较18S高,RNA完整性较好,但靠近电泳点样孔附近有亮斑,可能存在蛋白质、糖类等杂质残留;CTAB-LiCl法提取的RNA电泳呈弥散分布,28S和18S处略微可见且亮度较高,但条带不够清晰,这说明此方法提取的RNA已经有所降解,提取的RNA中可能存在基因组DNA;SDS/酚法提取的RNA电泳弥散最为严重,存在基因组DNA残留;改进的TRIzol法提取的RNA电泳可见清晰的28S和18S条带,且28S比18S亮度加倍,且完整性好,提取的RNA样品中无明显基因组DNA残留。
2.2不同提取方法的总RNA纯度和得率
D260 nm/D280 nm和D260 nm/D230 nm是对提取的核酸纯度和产率进行定量分析的通用方法,高纯度的RNA溶液D260 nm/D280 nm应介于1.8~2.0之间,D260 nm/D230 nm应大于2.0。由表
1可见,TRIzol法提取的RNA溶液D260 nm/D280 nm仅为1.582,可能存在蛋白质和酚等有机物残留,纯度过低;CTAB-LiCl法、SDS/酚法、改进TRIzol法D260 nm/D280 nm分别为2.081、2223、1.943,均有效去除了蛋白质和酚等物质;CTAB-LiCl法和改进TRIzol法D260 nm/D230 nm均大于2.0,即对酚类和糖类等有机物质可以有效去除;4种方法中,RNA提取产率最高的为TRIzol法,而CTAB-LiCl法、SDS/酚法、改进TRIzol法提取RNA的产率与TRIzol法相比,依次约能达到TRIzol法的70.3%、43.6%、73.1%。
表1不同方法提取百蕊草根系总RNA纯度及得率
提取方法D260 nm/D280 nmD260 nm/D230 nm得率
(μg/g)TRIzol法1.582±0.0481.082±0.070189.073±3.963CTAB-LiCl法2.081±0.0592.332±0.015132.983±2.455SDS/酚法2.223±0.0261.793±0.00782.367±9.166改进TRIzol法1.943±0.0492.074±0.033138.168±5.498
2.3改进TRIzol法提取总RNA的完整性验证
以改进TRIzol法提取的总RNA为模板进行反转录,产物经1.5%琼脂糖凝胶电泳检测,可看出反转录的cDNA片段呈弥散分布,大小主要集中分布在0.2~2.5 kb(图2)。该结果基本吻合植物RNA长度的一般范围,反映该cDNA的模板mRNA比较完整,提取的RNA质量较高,可以满足后续分子生物学试验要求。
对百蕊草TcActin基因保守区序列进行RT-PCR扩增,以进一步验证改进方法提取RNA的完整性。由图3可见,百蕊草TcActin基因保守区序列能得到片段长度约为330 bp的扩增产物,PCR产物经测序长度为333 bp,扩增片段长度与预计的檀香科Actin基因保守区序列长度一致,这说明改进的TRIzol方法提取总RNA保持了表达基因的完整性。
3讨论
纯度高、完整性好的RNA是进行分子克隆及基因表达分析的基础[17]。近年来,关于植物RNA提取方法的报道逐渐增多[18-20]。由于多数植物材料成分复杂,特别是糖类和酚类等有机物质对RNA提取的干扰很大[21-22]。酚类物质容易氧化形成褐化效应,与RNA不可逆结合,严重降低了RNA的质量和产率;含有多糖的RNA沉淀难溶于水,即使通过加热等方式溶解,溶液也呈黏稠状。目前,去除多糖的方法主要有高浓度NaCl沉淀法、LiCl沉淀法、乙酸钾沉淀法等。
TRIzol试剂原本用于提取动物组织RNA,因其操作步骤简便,全程只需1~2 h,后被开发提取植物组织RNA,且对多种植物组织RNA的提取十分有效[18]。较高浓度的CTAB不仅对植物细胞具有良好的裂解作用,有效形成核蛋白与核酸的复合物,而且还能与β-巯基乙醇联合作用使蛋白变性,抑制RNA酶的活性[23]。CTAB作为阳离子表面活性剂成分,从富含多糖、多酚材料中分离出高质量RNA已经在多种植物材料中得到验证。
传统TRIzol法提取的百蕊草根系总RNA沉淀呈褐色,且很难溶于水中,稍加热溶解沉淀后有淡黄色的膜状物质,不能有效去除酚类和糖类物质,但是通过凝胶电泳检测发现,TRIzol法提取的总RNA完整性良好,对RNA酶的抑制能力强,可有效避免降解;CTAB-LiCl法获得的RNA沉淀沾水即溶,结合凝胶电泳及OD值测定,该方法可有效去除蛋白质、酚类、糖类等有机物质,但存在基因组DNA污染,且不能有效抑制RNA酶的活性,出现RNA降解,这意味着提取的失败。
结合TRIzol法能够有效抑制RNA酶活性和CTAB-LiCl法能有效去除蛋白质、酚类、糖类等有机物质的特点,优化百蕊草根系总RNA提取方法,形成改进的TRIzol法,即在提取时加入β-巯基乙醇,该物质不仅能打开蛋白酶的二硫键使酶失活,从而抑制酚类氧化酶和RNA酶的活性,也能与酚类产生竞争性氧化,可有效避免褐化现象[24]。另外,LiCl沉淀可去除部分多糖,多次的酚/氯仿抽提也基本去除了蛋白质、酚类、糖类等有机物质。改进TRIzol法提取总RNA,虽然RNA的得率有所降低,但获得的RNA质量高,可以满足后续的分子生物学试验。
参考文献:
[1]江苏新医院. 中药大辞典上册[M]. 上海:上海科学技术出版社,1977:866.
[2]钟方丽,王晓林,纪萍萍,等. 百蕊草中总黄酮的提取工艺研究[J]. 吉林化工学院学报,2008,25(4):5-7.
[3]罗夫来,郭巧生,王长林,等. 百蕊草生物学特性研究[J]. 中国中药杂志,2012,37(2):176-180.
[4]Guo Q S,Luo F L. Comparative studies on the growth,chlorophyll,amino acids and minerals of Thesium chinense (Santalaceae) in association with different hosts[J]. Nordic Journal of Botany,2010,28(5):632-640.
[5]袁艺,龙子江,许霞,等. 百蕊草野生苗与组培苗抑菌抗炎实验比较的研究[J]. 药物生物技术,2006,13(3):219-222.
[6]杨军,王静,高美华,等. 百蕊片药理作用的实验研究[J]. 中国中药杂志,1999,24(6):47-49.
[7]曹明成. 百蕊草提取工艺研究[J]. 现代中药研究与实践,2004,18(1):57-58.
[8]Jiang Q,Dong L,Ning Z Y,et al. Establishment of somatic cell clones in Thesium chinense Turcz and its in vitro rooting technique[J]. Agricultural Science and Technology,2008,9(5):53-55,68.
[9]Luo F L,Guo Q S. Influences of host species on transpiration,photosynthesis,chlorophyll and mineral contents of medicinal hemiparasite Thesium chinense Turcz[J]. Acta Physiologiae Plantarum,2010,32(6):1093-1102.
[10]罗夫来,郭巧生. 百蕊草药材内在品质研究[J]. 中国中药杂志,2011,36(15):2042-2046.
[11]Su X,Gibor A. A method for RNA isolation from marine macro-algae[J]. Analytical Biochemistry,1988,174(2):650-657.
[12]Schneiderbauer A,Sandermann H,Ernst D. Isolation of functional RNA from plant tissues rich in phenolic compounds[J]. Analytical Biochemistry,1991,197(1):91-95.
[13]Fang G,Hammar S,Grumet R. A quick and inexpensive method for removing polysaccharides from plant genomic DNA[J]. BioTechniques,1992,13(1):52-54,56.
[14]董占强,翟晓巧,范国强,等. 泡桐叶片RNA提取方法的研究[J]. 河南农业大学学报,2009,43(1):40-43.
[15]李岩,王铁梅,卢欣石. 根蘖型苜蓿根部RNA提取方法的比较[J]. 草业科学,2010,27(5):67-71.
[16]张今今,王跃进,王西平,等. 葡萄总RNA提取方法的研究[J]. 果树学报,2003,20(3):178-181.
[17]张玉刚,成建红,韩振海,等. 小金海棠总RNA提取方法比较及cDNA的LD-PCR扩增[J]. 生物技术通报,2005,4(4):50-53.
[18]尹慧,陈莉,李晓艳,等. 百合叶片总RNA提取方法比较及优化[J]. 中国农业大学学报,2008,13(4):41-45.
[19]陈高,单雷,周丽侠,等. 花生总RNA提取方法比较研究[J]. 中国农学通报,2011,27(1):214-218.
[20]冯延芝,袁德义,张琳,等. 枣花蕾总RNA提取方法的比较[J]. 经济林研究,2012,30(2):88-90.
[21]王暑辉,徐倩,徐筱,等. 富含多糖多酚的侧柏叶片总RNA提取方法[J]. 吉林农业大学学报,2012,34(1):76-80,89.
[22]Wang G F,Wang G,Zhang X W,et al. Isolation of high quality RNA from cereal seeds containing high levels of starch[J]. Phytochemical Analysis,2012,23(2):159-163.
[23]覃芳,王军民,何海旺,等. 山药组织总RNA提取方法的比较与分析[J]. 基因组学与应用生物学,2009,28(4):755-759.
[24]黄月琴,徐有明,薛建平. 半夏块茎高质量总RNA提取的一种有效方法[J]. 中国中药杂志,2008,33(15):1810-1813.杜民,牛宝珍,刘艳红,等. 2个鲤鱼群体遗传多样性的RAPD分析[J]. 江苏农业科学,2015,43(1):47-49.