扶正消瘤颗粒联合卡瑞利珠单抗与阿帕替尼治疗晚期原发性肝癌临床观察*
杨 荷 陈晓琦 王新亭 张传雷 袁长威 杨芳明 陈欣菊△ 赵文霞
1.河南中医药大学第一临床医学院 (河南 郑州,450046) 2.河南中医药大学第一附属医院
中国是全世界范围内的原发性肝癌高发区之一,2018年全球841 080例新发肝癌病例中,中国肝癌发病例数占全球总数的46.71%,2008~2017年中国肿瘤登记地区肝癌死亡率介于(24.70~26.67)/10万[1]。早期肝癌的治疗上,手术切除、肝动脉栓塞及射频消融是公认的有效治疗手段[2]。然而晚期肝癌往往伴有血管侵犯甚至远处转移,手术切除等不具有适应证,选择合适有效的全身治疗可延长晚期患者生存时间,改善生活质量。在既往3期临床试验中,抗血管生成靶向药物甲磺酸阿帕替尼在中晚期肝癌(BCLC分期B或C期)治疗上疗效确切,与安慰剂组的中位生存期6.8个月相比,阿帕替尼可延长肝癌患者中位生存期至8.7个月[3]。但不良反应发生率高,大部分患者不能耐受常规剂量,只能减量服用,因此影响疗效[4]。近年来,免疫检查点抑制剂以激活自身免疫应答的独特治疗方式为晚期肝癌患者带来了新的希望,在许多晚期肿瘤治疗中有着突破性的进展。纳武单抗(nivolumab)及帕博利珠单抗(pembrolizumab)作为二线药物被美国食品药品管理局(FDA)批准用于原发性肝细胞癌。在国内,自主研发的卡瑞利珠单抗是首个获批原发性肝细胞癌适应证的PD-1抑制剂,卡瑞利珠单抗联合甲磺酸阿帕替尼(双重抗 PD-1/VEGFR-2)在中晚期肝细胞癌(BCLC分期B或C期)2期试验(RESCUE研究)中,在一线队列中的客观缓解率(ORR)达到了46%,双药联合疗效显著,但带来更多的不良反应也使安全性受到了挑战[5]。研究证实中药在抑制肿瘤细胞增殖、改善症状、减毒增效、提高生存质量、延长生存期等方面具有独特的优势[6]。前期研究发现扶正消瘤颗粒可以降低早中期肝癌综合介入后复发率[7],临床中发现其对晚期肝癌也有较好疗效。本研究系统性回顾了44例晚期不可切除的原发性肝癌患者(BCLC分期C期)应用卡瑞利珠单抗联合甲磺酸阿帕替尼,同时服用扶正消瘤颗粒,观察其不良反应发生率、中位无进展生存期(PFS)及中位总生存期(OS),初步探讨中医药在原发性肝癌的双重抗 PD-1/VEGFR-2疗法方面的减毒增效作用。
1 资料和方法
1.1 一般资料 本研究为回顾性研究,选取2017年12月1日至2020年12月1日于我院接受免疫检查位点抑制剂(卡瑞利珠单抗)联合靶向药物(甲磺酸阿帕替尼)及中药治疗的44例晚肝癌患者,患者的一般资料见表1。
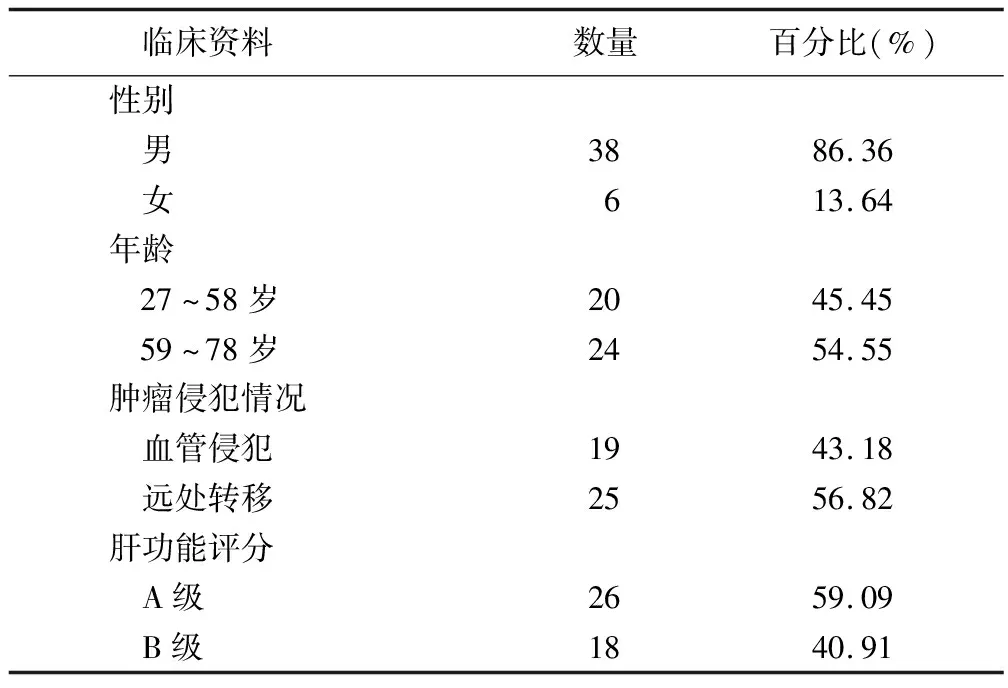
表1 44例患者临床资料
1.2 纳入与排除标准 纳入标准:①巴塞罗那(BCLC)分期为C期的原发性肝癌患者;②卡式功能状态量表(KPS)评分≥70;③无肝动脉化疗栓塞(TACE)适应证或经多次TACE及或消融治疗仍继续进展的患者;④根据mRECIST评价标准,至少有一个可测量的靶病灶,包括原发灶、转移灶及淋巴结;⑤接受≥2个周期的卡瑞利珠单抗治疗,期间联合甲磺酸阿帕替尼及扶正消瘤颗粒治疗。排除标准:①观察期间合并TACE、射频消融及125I粒子治疗的患者;②治疗期间合并应用免疫调节剂(如胸腺肽α1)的患者。
1.3 治疗方法 ①基础治疗:常规抗病毒、保护肝功能、营养支持对症处理等。②免疫治疗:每3周为1个治疗周期,每周期第1天给予卡瑞利珠单抗治疗(SHR-1210,江苏恒瑞生物制药有限公司,200 mg静脉滴注)。所有患者均接受了≥2个周期卡瑞利珠单抗治疗,直到病情进展或不可耐受。③靶向药物为甲磺酸阿帕替尼片250~500 mg(根据患者耐受情况调整用量),每日1次,连续服用,直到病情进展或不可耐受。④扶正消瘤颗粒:黄芪、白术、丹参、牡蛎、白花舌蛇草各30 g,菝葜、鳖甲、党参、白芍各15 g,陈皮12 g,柴胡10 g,甘草6 g。用法:1剂/d,温水冲至100 ml,分早晚2次服。持续服用直至患者不能耐受或要求停药。
1.4 随访 通过电话、门诊或查阅病例的方式进行随访,44例患者获得有效随访,随访截止仍未出现疾病进展或死亡的患者按截止时间处理。最末入组患者随访时间≥6个月,随访截止日期为 2021年5月31日。
1.5 疗效评价 治疗期间每2周期复查CT或MRI评价疗效,根据mRECIST标准评价患者近期疗效,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。记录ORR,ORR=(CR+PR)/(CR+PR+SD+PD)×100%,疾病控制率(DCR),DCR=(CR+PR+SD)/(CR+PR+SD+PD)×100%。PFS定义为入组患者自开始使用联合方案的时间起至有客观证据记录的疾病进展或死亡的时间;OS定义为入组患者自开始使用该联合方案的时间起至死亡的时间。
1.6 不良事件 采用通用术语标准(CTCAE)v5.0记录不良事件并对其分级。
1.7 统计学方法 采用SPSS 25.0软件对44例患者数据进行统计学分析,计数资料用构成比表示,应用Kaplan-Meier法对患者的PFS、OS进行估计。
2 结果
2.1 疗效评价 根据评价标准,其中0例CR,7例PR(15.91%,7/44),23例SD(52.27%,23/44)和14例PD(31.82%,14/44)。ORR为15.91%,DCR为68.18%。
2.2 生存分析 44例患者接受卡瑞利珠单抗治疗的中位治疗次数为5次,最多达23次。17例存活,27例死亡,总生存率为38.64%,3个月生存率为90.91%(40/44),6个月生存率为65.91%(29/44)。Kaplan-Meier法估计中位PFS为5个月,见图1;中位OS为11个月,见图2。
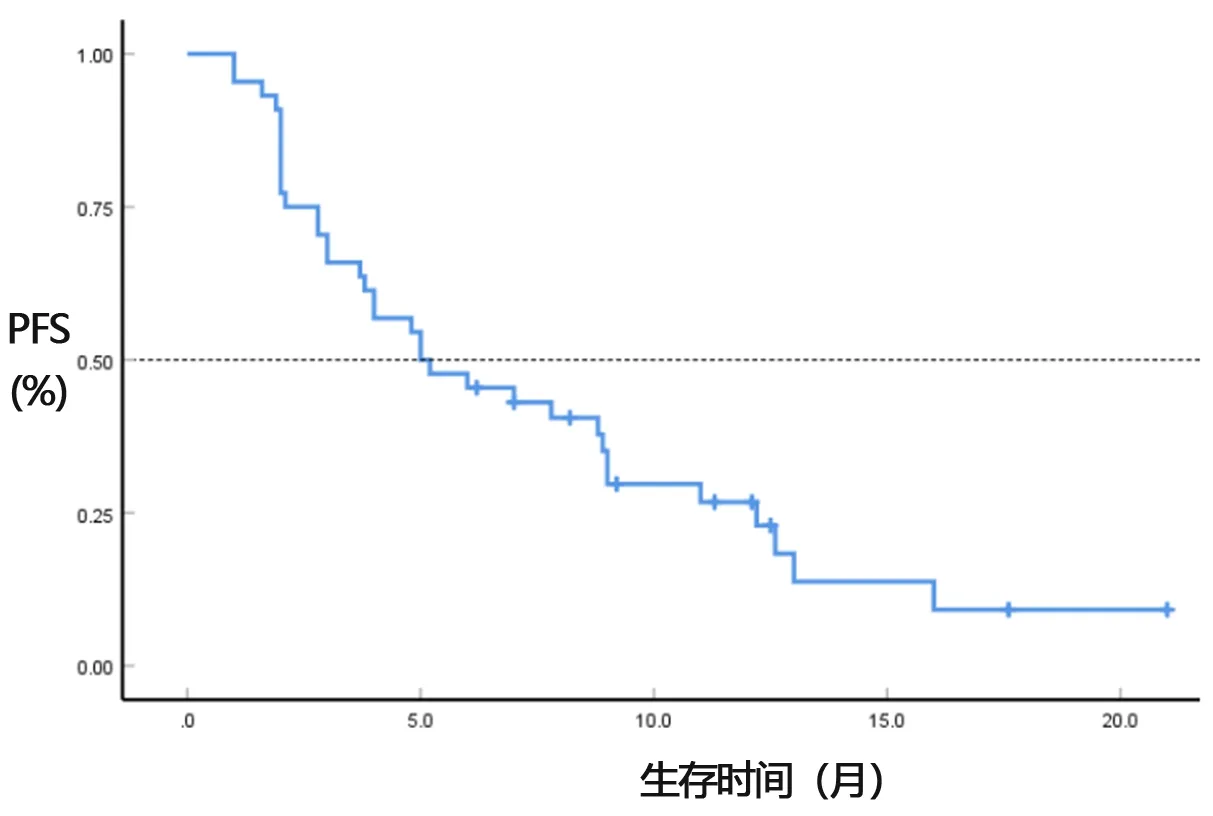
图1 PFS Kaplan-Meier生存分析
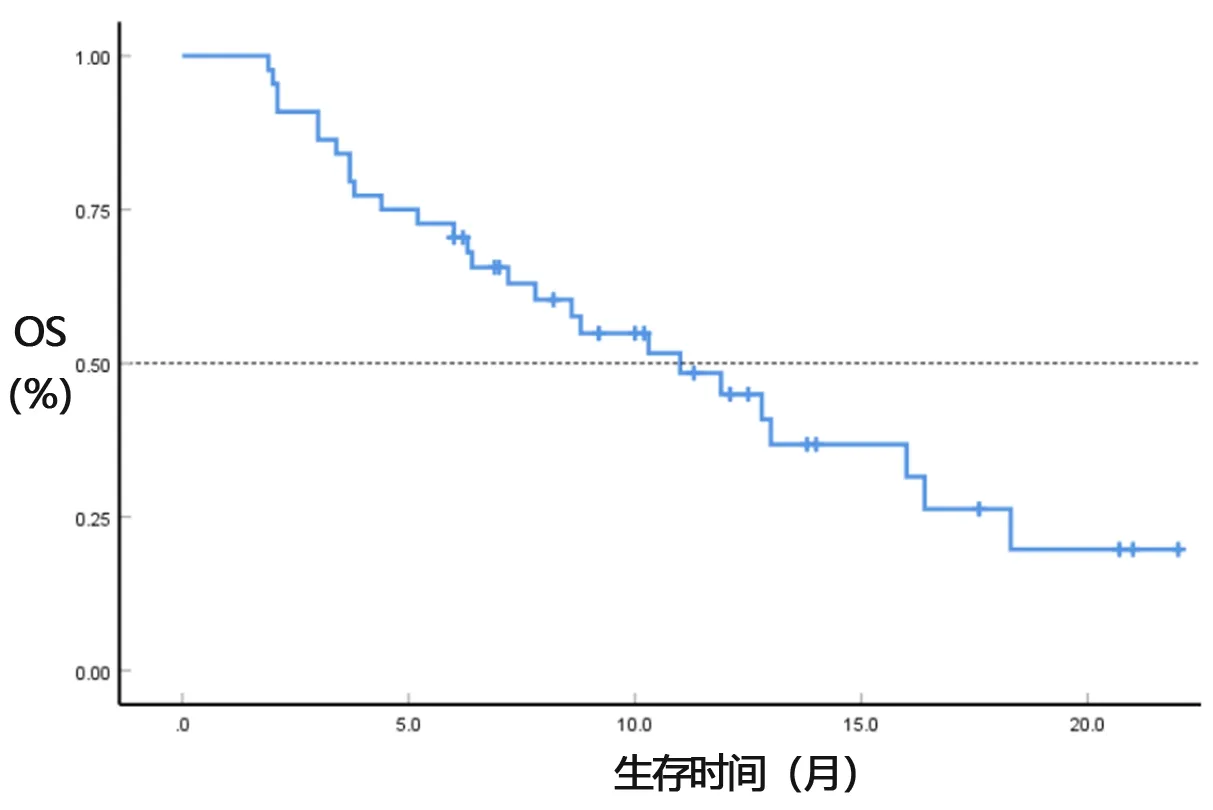
图2 OS Kaplan-Meier分析
2.3 不良事件分析 相关不良反应事件发生率为59.09%(26/44),3级及以上不良反应发生率为11.36%(5/44)。见表2。
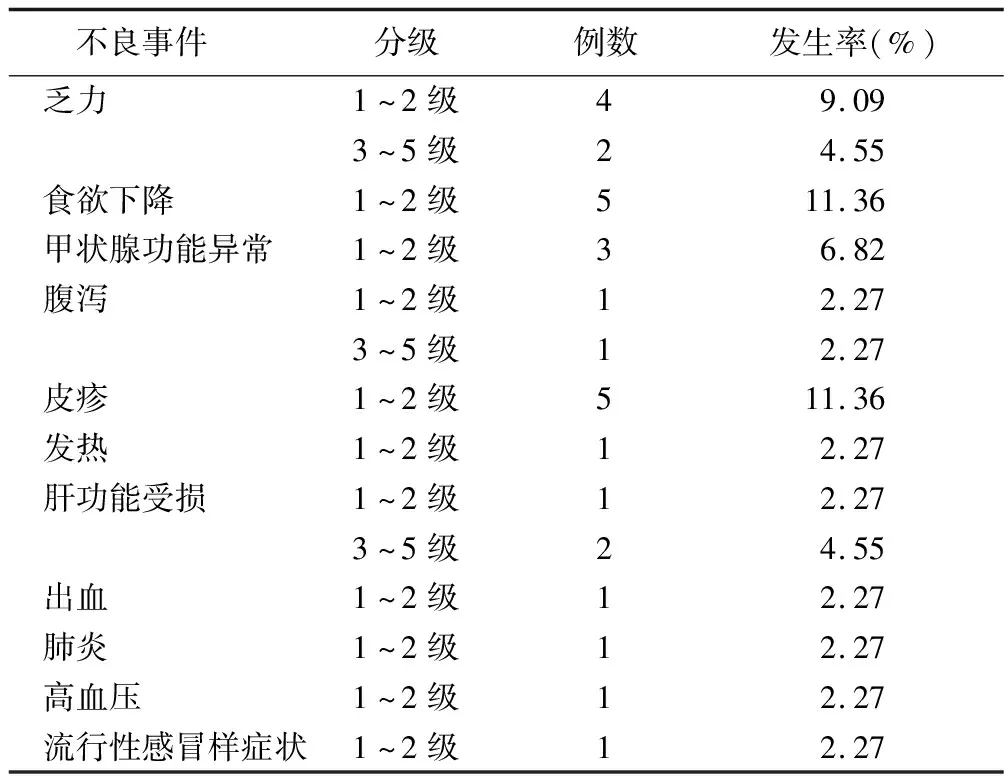
表2 44例中晚期肝癌患者不良事件分析
3 讨论
我国肝癌患者生存率低,国家癌症中心报道2003~2005年中国肝癌患者5年生存率仅为10.1%,2012~2015年为12.1%[8]。肝癌早期尚可通过手术等治疗方式取得良好疗效,但肝脏晚期肿瘤转移快,复发率高,预后极差,研究发现血管内皮生长因子(VEGF)过表达是肝癌转移的重要因素,为抑制VEGF合成,进而抑制肿瘤新生血管的生成,络氨酸激酶抑制药的应用必不可少[9]。但其临床效果仍不理想。一项关于卵巢癌的实验发现,程序性细胞死亡配体1(PD-L1)可直接与血管内皮生长因子受体-2(VEGFR2)相互作用,激活FAK/AKT通路,进而诱导血管生成和肿瘤进展,导致卵巢癌患者预后不良[10]。此实验提示PD-L1抑制剂可辅助增加抗血管生成药物疗效。另一项小鼠肝癌实验发现阻断VEGFR-2可明显升高CD4+细胞中PD-1的表达,在抗VEGFR-2抗体的治疗下,联合PD-1抑制剂治疗时,CD8+细胞的浸润和活化明显增加,CD4+细胞开始促进正常血管的形成,调节性T淋巴细胞(Treg)和CCR2+单核细胞浸润明显减少,肝癌免疫微环境得到重新编程[11]。结果显示,免疫检查位点抑制剂联合抗血管生成药物疗法拥有更加持久的抗血管作用,并提高了抗PD-1治疗的临床效果。
但两者联合也意味着更多的不良反应发生率,例如选择性靶向抗VEGFR2的药物阿帕替尼,已被证明对中国肝癌患者有效。但其手足皮肤反应的发生率很高,研究回顾阿帕替尼在中国肝癌患者中的手足综合征发生率约为50.5%,其中1/2级和3级分别为38.8%和11.6%[12]。阿帕替尼在既往3期临床试验中,最常见的3级或4级治疗相关不良事件是高血压(28%),手足综合征(18%),血小板计数减少(13%)[3],而免疫治疗相关不良反应几乎可影响人体所有的组织器官,在单药研究中,抗PD-1/PD-L1免疫治疗最常见的不良事件是乏力,抗PD-1和PD-L1治疗中乏力的发生率分别为16%~37%和12%~24%[13]。在卡瑞利珠单抗联合阿帕替尼的治疗晚期肝细胞癌的2期临床试验(RESCUE研究)中,不良反应发生率为99.5%,最常见的是天冬氨酸转氨酶升高(71.1%)、血小板计数降低(65.8%)、丙氨酸氨基转移酶升高(60.0%)、掌趾红肿综合征(56.8%)。反应性毛细血管增生症的发生率为29.5%,多为1~2级不良反应[5]。众多不良反应使联合应用有了更多的挑战,不良反应的避免及管理刻不容缓。中医药在辅助治疗肿瘤方面有显著优势,而且对化学性治疗具有减毒增效作用[14]。前期研究发现,扶正消瘤颗粒可降低HIF-1α水平,下调VEGF的表达,抑制肿瘤血管生成,进而控制肿瘤侵袭转移,同时可减轻患者乏力、疼痛、腹胀、腹泻等不良症状,显著改善患者的生活质量[15]。在目前肿瘤靶向免疫治疗时代,中医药在免疫方面的双向调节作用不但可增强疗效,而且可减轻由免疫过激引起的不良反应。安方玉等[16]发现黄芪总皂苷可通过调节免疫来抑制小鼠肝癌细胞的增殖,同时黄芪皂苷也可抑制多种炎症物质如脂多糖(LPS)诱导的炎症反应,从而抑制由免疫炎症介导的肿瘤的发展[17]。白花蛇舌草和菝葜均可抑制由过激的免疫引起的炎症反应而达到清热解毒抗炎作用[18,19]。甘草提取物甘草甜素具有类皮质激素样作用,可减轻炎症调节免疫反应[20]。中药(党参、白术、茯苓等)可通过调节肠道菌群、重构辅助性T细胞1(Th1)/Th2动态平衡、激活调节性T淋巴细胞(Treg)等方式干预免疫不良反应[21]。总之,中药的抗炎和对免疫反应的双重调节作用在肿瘤治疗领域将有广阔的前景。
本研究回顾性分析了应用扶正消瘤颗粒、PD-1单抗及甲磺酸阿帕替尼的44例晚期肝癌患者,最终不良反应事件的发生率为59.09%(26/44),3级及以上不良反应发生率为11.36%,明显低于RESCUE研究。本研究44例患者的中位PFS为5个月,与RESCUE研究结果基本相符,中位OS为11个月,低于RESCUE研究,原因为RESCUE研究纳入BCLC分期B~C期、肝功能A级患者,本研究44例患者均为巴塞罗那C期,肝外转移患者占56.82%,B级肝功占40.91%,肝功能储备较差、分期靠后,因此,仍显示了中医药联合PD-1单抗及抗血管生成药物治疗晚期肝癌的优势。
该研究初步验证了扶正消瘤颗粒可提高双重抗PD-1/VEGFR-2疗法对晚期原发性肝癌的治疗效果,降低其不良反应发生率,为中西医结合治疗晚期肝癌提供一定临床依据。

