靶向hIL-4Rα单克隆抗体的开发
郭锦林
摘要:本研究我们通过杂交瘤技术筛选得到了特异性识别人IL-4Rα的高亲和力单克隆抗体Mab236,该抗体能够抑制hIL-4、hIL-13与hIL-4受体的结合和其介导的下游信号通路的活化。Mab236与hIL-4Rα ECD-flag的亲和力KD经Biacore检测为93.1 pM。Mab236浓度依赖性地抑制了hIL-4和hIL-4Rα的结合,ELISA检测抑制IC50为285.1 ng/ml。在TF-1细胞的增殖抑制实验中,TF-1细胞经hIL-4或/和hIL-13诱导后,细胞增殖均显著增加,加入Mab236后,抗体对不同条件诱导的TF-1细胞增殖均有浓度依赖的显著抑制作用。在人PBMCs培养体系中,Mab236浓度依赖性地抑制了hIL-4或/和hIL-13誘导PBMCs分泌的TARC水平。
关键词:IL-4Rα;单克隆抗体;哮喘
Abstract In this study, we screened the high affinity monoclonal antibody Mab236 that specifically recognizes human IL-4Rα by hybridioma technology, and this antibody can inhibit the binding of hIL-4 and hIL-13 to hIL-4 receptor and the activation of downstream signaling pathway mediated by it. The affinity KD between Mab236 and hIL-4RαECD-Flag was 93.1 pM by Biacore. Mab236 inhibited the binding of hIL-4 to hIL-4Rα in a concentration-dependent manner, and the inhibition IC50 was 285.1 ng/ mL by ELISA. In an experiment that inhibits TF-1 cell proliferation, the proliferation of TF-1 cells was significantly increased after the induction of hIL-4 or/and hIL-13, After the addition of Mab236, antibody had a concentration-dependent significant inhibition effect on the proliferation of TF-1 cells under different inductive conditions. In the culture system of human PBMCs, Mab236 concentration-dependent inhibited the TARC secreted by hIL-4 or/and hIL-13 induced in PBMCs.
Key Words IL-4Rα, Monoclonal antibody, Asthma
1引言
支气管哮喘作为一种由多种细胞及细胞因子参与的慢性气道炎症,被世界卫生组织列为四大顽症之一,是仅次于癌症的世界第二大致死和致残疾病。哮喘患者往往出现反复发作的喘息、气促、胸闷、咳嗽等症状。哮喘的标准疗法为吸入式糖皮质激素+/-长效β2受体激动剂,长期使用该种疗法有较强的副作用,且5~10%的患者当前仍无有效的治疗药物[1]。
目前,全球约有3亿哮喘患者,预计到2025年将增长至4亿,中国现在20岁及以上成年哮喘患者已经达到4570万。据中国哮喘联盟流行病学2018年调查显示,仅有28.8%的哮喘患者得到诊断,全国哮喘患者控制率为40.5%,完全控制率仅为15.6%。实际上,哮喘已成为了我国第二大呼吸道疾病,死亡率达36.7/10万,全球最高[2]。
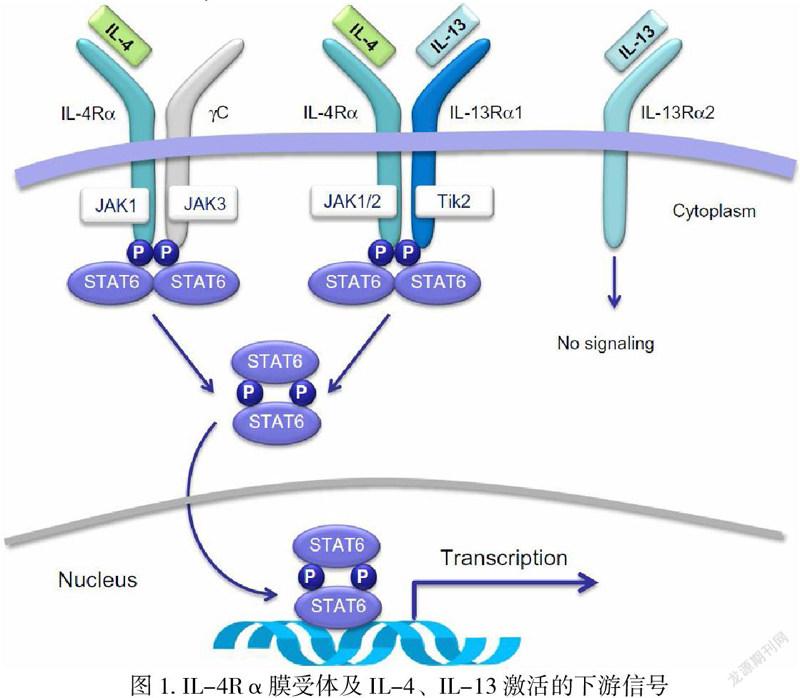
研究表明, Th2型细胞应答在大多数哮喘疾病的发生过程中起着非常关键的作用,其中Th2型细胞因子IL-4和IL-13的上调是哮喘等疾病中炎症反应的主要驱动因子[3]。IL-4Rα属于Th2型炎症通路中I型受体和II型受体的关键组成部分,阻断IL-4Rα可同时阻断Th2型免疫反应的两个强效调节因子IL-4和IL-13分别通过I型受体和II型受体发挥作用,从而抑制Th2型炎症的中枢通路[4][5] (见图1)。
本文我们通过筛选hIL-4Rα的单抗来抑制hIL-4或/和hIL-13激活的下游信号,从而抑制Th2型细胞应答的水平。我们表达了hIL-4Rα ECD-hFc的融合蛋白作为抗原免疫小鼠,通过传统的杂交瘤技术,筛选靶向结合hIL-4Rα的鼠单抗。我们验证了鼠单抗抑制hIL-4与hIL-4Rα结合的作用,抑制hIL-4或/和hIL-13诱导TF1细胞增殖的作用,以及降低在hIL-4或/和hIL-13诱导下人PBMCs分泌TARC的水平。希望该抗体经过后续进一步的开发能用于哮喘、特应性皮炎等Th2型炎症疾病的治疗。
2材料与方法
2.1材料
SP2/0细胞、TF1细胞,购买于中科院细胞库;人PBMCs,购买于TPCS;重组hIL-4Rα ECD-hFc、hIL-4Rα ECD-flag及阳性抗体Dupilumab为本实验室通过HEK293细胞瞬转后纯化得到;重组hIL-4、hIL-4-His、hIL-13购买于Sino Biological;鼠单抗Mab236为筛选得到的杂交瘤细胞无血清培养后经proteinG纯化得到;PEG(1450)购买于sigma;Human CCL17/TARC Quantikine ELISA Kit购买于R&D Systems,货号:DDN00;CCK-8试剂盒购买于Dojindo,货号CK04。
2.2方法
2.2.1 鼠单抗的杂交瘤筛选
hIL-4Rα ECD-hFc抗原与弗氏佐剂等体积混匀乳化后,免疫4~6周龄的Balb/c雌鼠三次,2周/次,血清滴度>10000时可用于杂交瘤融合。融合与筛选过程如下:按照脾细胞∶sp2/0细胞=10∶1的比例混合两种细胞,1500rpm离心7分钟;吸去上清液,1分钟内加入1ml PEG(1450),轻摇90秒,在2.5分钟内缓慢滴加无血清DMEM培养液5ml,然后一次性加5ml无血清培养液终止反应,静置5分钟,1280rpm离心8分钟。将融合后的细胞铺于96孔板中,并用含HAT加压筛选,每3~4天进行半量换液一次,一周后改用HT培养基培养,待杂交瘤细胞覆盖96孔板底部的约30%时,取细胞上清用hIL-4Rα ECD-hFc抗原包被的酶标板进行ELISA检测。挑选出阳性杂交瘤克隆并通过有限稀释法进行二轮亚克隆。获得稳定表达抗体的杂交瘤株后进行保种及无血清培养。
2.2.2 Biacore检测Mab236与hIL-4Rα ECD-flag的亲和力
通过筛选确定PH 4.0 10 mM乙酸钠为偶联用溶液,将hIL-4Rα ECD-flag用乙酸钠溶液稀释至20 μg/ml,通过程序偶联至活化后的CM5芯片上。最终hIL-4Rα ECD-flag的偶联量为50.6Ru。将Mab236用1×HBS EP+溶液稀释,从400 nM开始进行2倍梯度稀释,共9个浓度。循环条件为:在FCs所有通道中以30 l/min注射分析物2 min,解离时间为20 min,然后以30 l/min速率注射再生液30 s进行表面再生。各个浓度循环结束后利用Biacore T200 Evaluation Software Ver 1.0计算捕获抗体的信号和无捕获抗体的信号差值及相互作用的亲和力。
2.2.3 抗体对hIL-4与hIL-4Rα ECD-hFc体外结合的抑制分析
Anti-his抗体以2 μg/ml的浓度包被酶标板,用含1% BSA封闭液封闭;hIL-4-His以1 μg/ml的浓度加入封闭好的酶标板中,100 μl/孔,室温孵育1 h后洗板2次;Mab236与Dupilumab以100 μg/ml的起始浓度进行3倍稀释10个梯度,与200 ng/ml 的Biotin-hIL-4Rα ECD-hFc等体积混匀,室温孵育1 h;用排枪吸取上述抗体混合液100 μl加入封闭好的ELISA板中,设立两个复孔,室温孵育1.5 h;洗板后加入Streptavidin-HRP抗体室温孵育1 h;PBST洗板4次,每孔加100 μl显色液,显色5min后每孔加终止液60 μl终止反应;立即用酶标仪在450 nm波长处测量各孔的OD值并分析数据。
2.2.4 抗体对hIL-4或/和hIL-13誘导的TF1细胞增殖的抑制分析
处于对数生长期的TF1细胞用含5%胎牛血清的RPMI 1640培养基洗2遍;TF1细胞计数,悬浮成5E4/ml的密度;Mab236抗体先稀释成20ug/ml的浓度,再以3倍的稀释度梯度稀释10个梯度,设立Dupilumab阳性对照。将稀释好的抗体加入96孔细胞培养板中,100μl/孔,设立两个复孔;hIL-4或/和hIL-13以终浓度10ng/ml加入TF1细胞中,充分混匀后立即加入上述已加好抗体的96孔细胞培养板中,100μl/孔,在37℃、5%CO2条件的孵箱中孵育培养;7天后96孔细胞培养板每孔加入20μl CCK-8溶液,在37℃孵箱中继续培养4~6h,混匀后酶标仪读OD450值,GraphPad Prism6进行数据分析。
2.2.5 抗体对hIL-4或/和hIL-13诱导的人PBMCs 分泌TARC的抑制分析
Mab236与Dupilumab分别用含5%胎牛血清的RPMI 1640培养基稀释成100 μg/ml、20 μg/ml和4 μg/ml的浓度,加入96孔细胞培养板中,50 μl/孔;将新鲜人PBMCs浓度调整为2E6 /ml,接种到上述加好抗体的96孔细胞培养板中,100 μl/孔,设立两个复孔。将培养板置于37℃细胞培养箱中孵育1小时;hIL-4或/和hIL-13各稀释成40 ng/ml的浓度,分别加入或等体积混合后加入到上述孵育好的细胞中,50 μl/孔;96孔板置于37℃培养箱中孵育2天,收取细胞培养液上清用Human CCL17/TARC Quantikine ELISA Kit检测上清中TARC的含量。
3结果
3.1 Mab236与hIL-4Rα ECD-flag的亲和力
经过三轮杂交瘤的融合与筛选,我们一共得到了66株与hIL-4Rα ECD-hFc具有高亲和力的鼠单抗,我们对这些鼠单抗的亲和力及生物学活性进行了多轮的比较分析,结果表明鼠单抗Mab236亲和力及生物学活性综合表现最佳。本文我们展开了对Mab236体外生物学活性的分析。
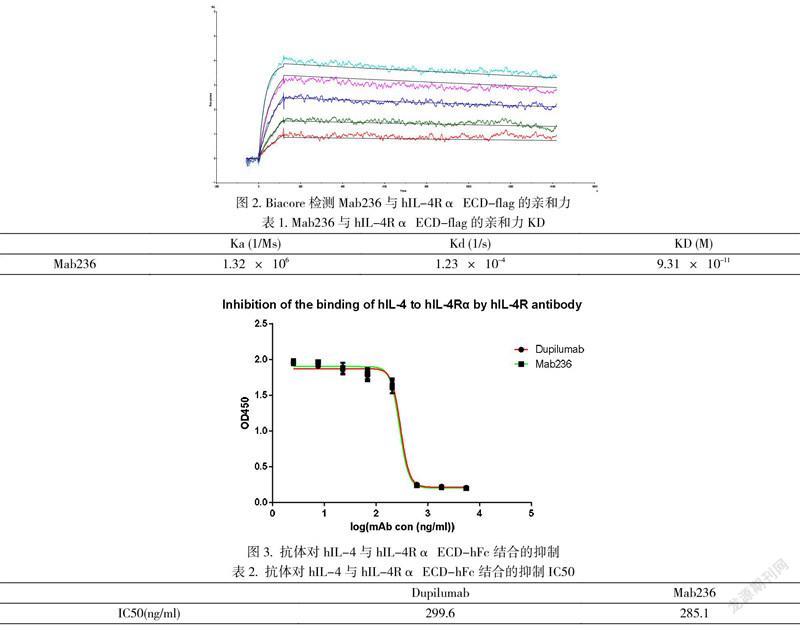
首先,我们用Biacore的方法将Mab236进行了亲和力的测定。实验结果显示,Mab236与hIL-4Rα ECD-flag有很高的亲和力(见图2),亲和力KD为93.1pM(见表1)。Mab236与hIL-4Rα的高亲和力是其后续表现出较好生物学活性的一个必要前提。
3.2 抗体抑制hIL-4与hIL-4Rα ECD-hFc体外结合的作用
IL-4Rα可以与γc链形成异二聚体,成为I型IL-4受体,由IL-4激活;也可以与IL-13Rα1形成异二聚体,成为II型IL-4受体,由IL-4或IL-13激活。I型和II型受体被激活后,可活化下游信号通路,介导炎症细胞的增殖、活化等功能[6]。因此抑制IL-4、IL-13与其受体结合是抑制其下游信号活化的前提。
我们通过竞争抑制ELISA证实,Mab236可高效抑制IL-4与hIL-4Rα ECD-hFc体外的结合(见图3),Mab236抑制IC50为285.1 ng/ml (见表2)。此实验为进一步验证抗体抑制IL-4和/或IL-13激活的细胞下游信号提供了作用机理的基础。
3.3 抗体对hIL-4或/和hIL-13诱导TF1细胞增殖的抑制作用
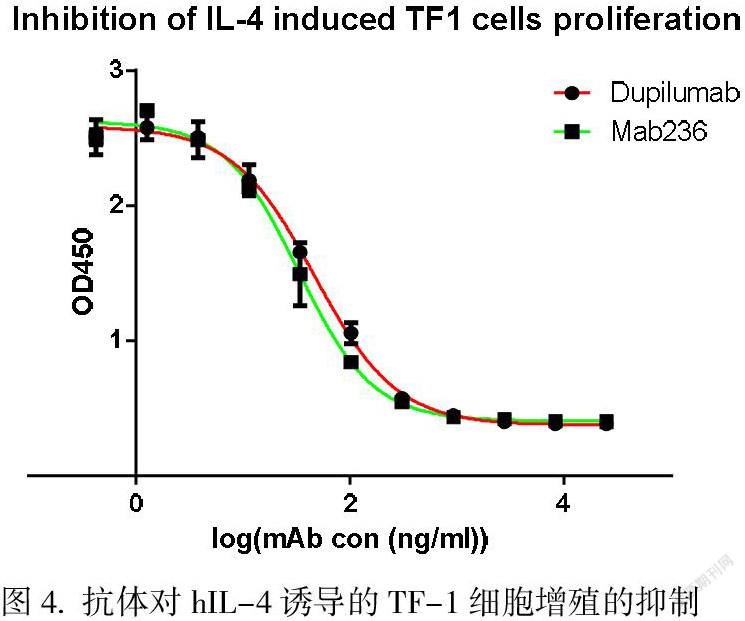
人红系白血病细胞TF-1表达hIL-4Rα和hIL-13Rα1受体,其增殖可由hIL-4或/和hIL-13诱导[7]。抗体特异性结合TF-1细胞表面hIL-4Rα,抑制hIL-4和/或hIL-13与其膜受体的结合,可抑制其下游信号的活化。本研究通过考察不同抗体浓度下由hIL-4和/或hIL-13诱导的TF-1细胞增殖的水平,评价抗体对TF1细胞在不同诱导条件下增殖的抑制活性。
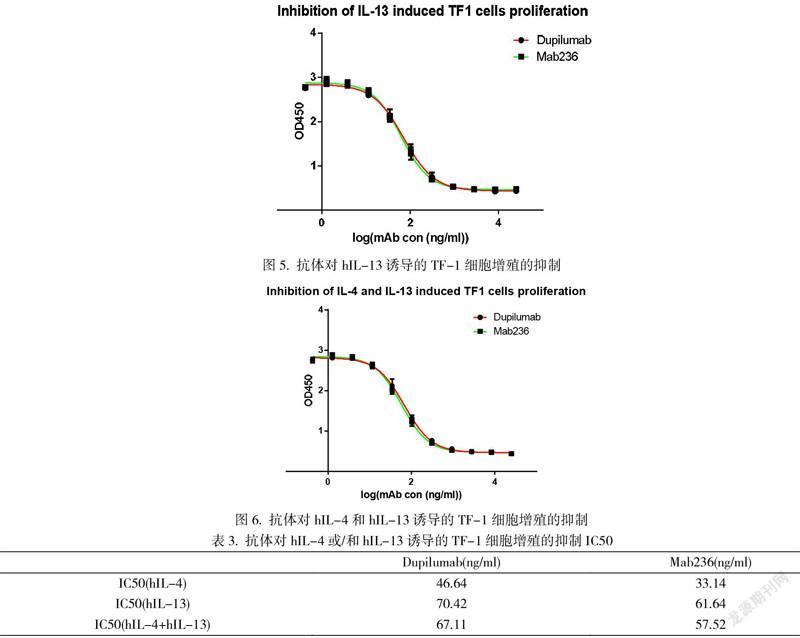
实验结果显示,TF-1细胞经10 ng/ml hIL-4、10 ng/ml hIL-13或10 ng/ml hIL-4 + 10 ng/ml hIL-13诱导后,细胞的增殖水平显著增加。在培养体系中加入Mab236或Dupilumab后,三种不同条件诱导的TF-1细胞增殖均出现了抗体浓度依赖的显著抑制作用(见图4、图5、图6),Mab236对hIL-4、hIL-13、hIL-4 + hIL-13诱导TF1细胞增殖的抑制IC50分别为:33.14 ng/ml 、61.64 ng/ml 、57.52 ng/ml (见表3),均显示了抗体高效抑制TF-1细胞中IL-4Rα受体下游信号的生物活性。
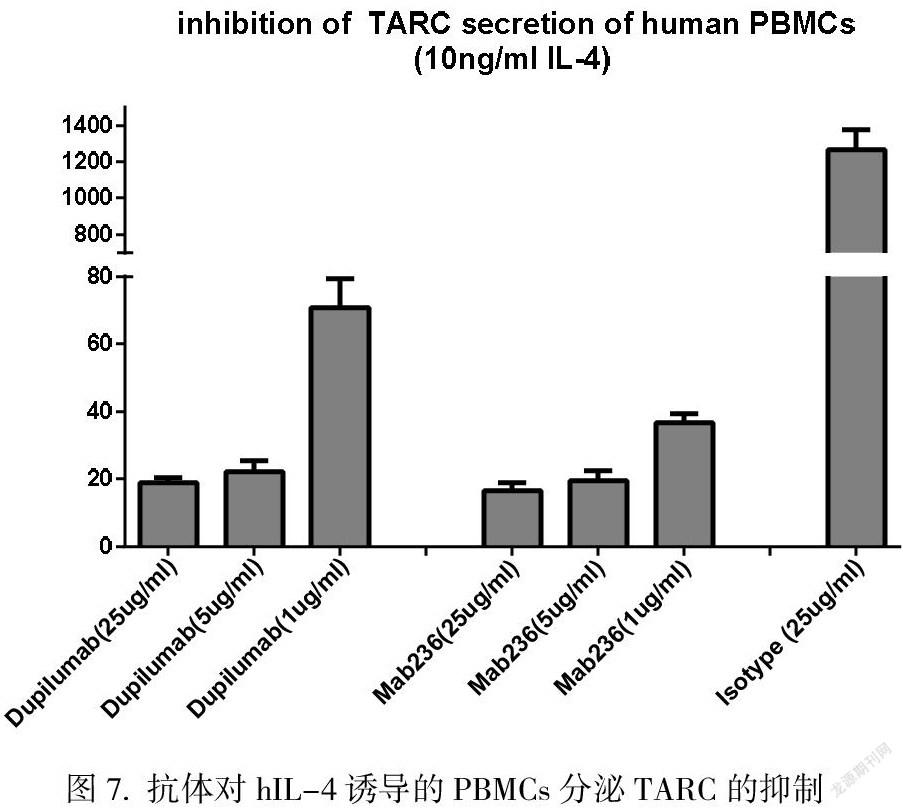
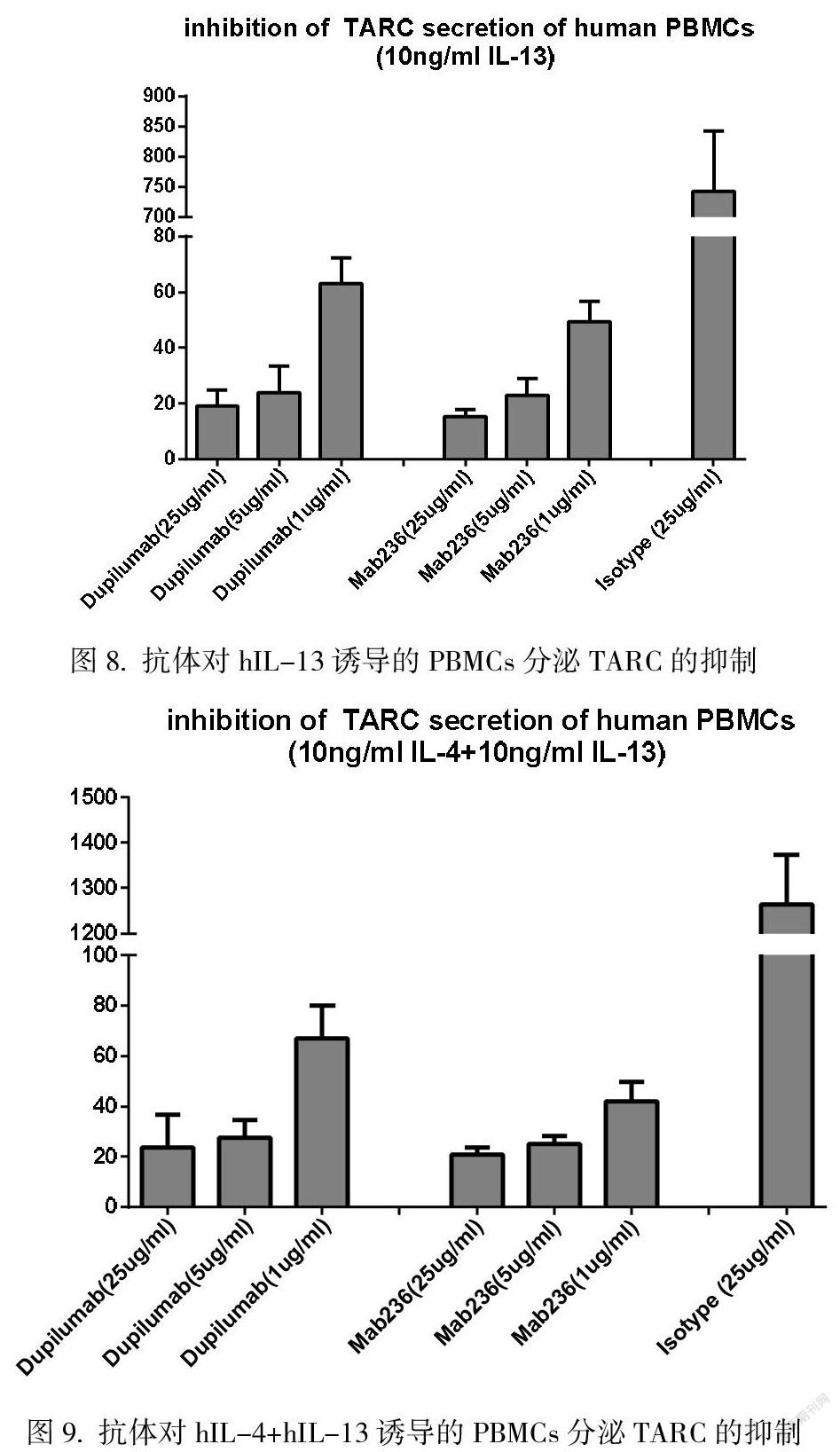
3.4抗体对hIL-4或/和hIL-13诱导的人PBMCs 分泌TARC的抑制作用
IL-4和IL-13的重要作用机理之一是诱导T细胞分泌趋化因子—胸腺活化调节趋化因子(thymus and activation regulated chemokine, TARC,又名CCL17),募集活化炎症细胞至炎症部位,介导炎症应答反应。IL-4Rα的I型受体与II型受体分别主要在造血细胞与非造血细胞上表达,人PBMCs中IL-4Rα的I型受体与II型受体均有广泛表达[8]。本研究我们检测了抗体对hIL-4或/和hIL-13诱导人PBMCs分泌TARC的抑制作用。
Mab236对10 ng/ml hIL-4、10 ng/ml hIL-13或10 ng/ml hIL-4 + 10 ng/ml hIL-13诱导人PBMCs分泌TARC的抑制作用如图7、图8和图9所示。实验结果显示,在培养体系中加入IL-4或/和IL-13均显著诱导了PBMCs中TARC的分泌,在应用较高抗体浓度时,5 μg/ml和25 μg/ml的Mab236均能将PBMCs分泌的TARC抑制到很低的水平,且该抑制作用具有浓度依赖性。此实验证实Mab236可抑制人PBMCs由hIL-4或/和hIL-13激活的下游信号。由此推测,在人体内若该抗体也能实现对趋化因子TARC分泌的有效抑制,將能抑制炎症细胞被募集至炎症部位,从而降低体内炎症级联应答的水平。
4 讨论
在本文研究中,我们以同靶点抗体药物Dupilumab为参照,评价了Mab236的体外生物学活性。研究结果表明,Mab236可高效结合hIL-4Rα,并抑制hIL-4与hIL-4Rα的结合。在用hIL-4或/和hIL-13诱导TF-1细胞的体外增殖试验中,加入Mab236后,不同诱导条件下的TF-1细胞增殖均被抗体浓度依赖性地显著抑制。在人PBMCs中,Mab236浓度依赖性地抑制了hIL-4或/和hIL-13诱导PBMCs分泌的TARC,揭示其有望实现在人体内抑制由TARC诱导的炎症细胞向炎症部位的迁移和活化,从而降低Th2型炎症应答水平。
IL-4 和 IL-13 被认为是哮喘和特应性皮炎等炎症反应的主要驱动因子。在全球范围内,靶向IL-4Rα仅有的已上市抗体药物是赛诺菲和再生元共同研发开发的Dupilumab(通用名:达必妥),Dupilumab已获批用于中重度特应性皮炎、伴鼻息肉鼻窦炎和哮喘的治疗[9] [10]。截至目前,Dupilumab已在全球40多个国家地区获批上市,为赛诺菲每年带来超过20亿欧元的收入。根据 Evaluate Pharma 报告指出,Dupilumab 将成为赛诺菲未来增长的关键驱动力,随着临床适应症的不断增加以及市场的不断扩张,该药在 2024 年将成为继艾伯维修美乐之后的全球第二大畅销抗炎药,销售额将达到 80.58 亿美元。
本研究我们筛选得到的鼠单抗Mab236可同时抑制由hIL-4 或/和 hIL-13 激活的下游信号,在本文评价的体外实验中显示出了略优于Dupilumab的生物学活性,后续我们将进一步考察其体内生物学活性以及工艺开发的可行性,希望将来能应用于Th2型炎症疾病(包括哮喘、特应性皮炎、特发性荨麻疹、慢性鼻息肉性鼻窦炎以及食物过敏等疾病)的治疗。
参考文献
[1] Camilla Boslev Barnes, et al. Asthma and adherence to inhaled corticosteroids: current status and future perspectives[J]. Respir Care. 2015;60(3):455–468.
[2] Huang K, et al. Prevalence, risk factors, and management of asthma in China: a national cross-sectional study. Lancet[J]. 2019;394:407-18.
[3] Bagnasco D, et al. A critical evaluation of anti-IL-13 and anti-IL-4 strategies in severe asthma[J]. Int Arch Allergy Immunol, 2016, 170(2):122-131.
[4] LaPorte SL, et al. Molecular and structural basis of cytokine receptor pleiotropy in the interleukin-4/13 system[J]. Cell. (2008) 132:259–72.
[5] Vatrella A, et al. Dupilumab: a novel treatment for asthma[J].J Asthma Allergy. 2014 Sep 4;7:123-30
[6] LaPorte SL, et al. Molecular and structural basis of cytokine receptor pleiotropy in the interleukin-4/13 system[J]. Cell. (2008) 132:259–72.
[7] Ma L, Zou Y. TF-1 Cell Proliferation Assay Method for Estimating Bioactivity of Nerve Growth Factor[J]. Journal of Applied Virology. 2013; 2 (2):32-37.
[8] Wirnsberger G, et al. IL-4 induces expression of TARC/CCL17 via two STAT6 binding sites[J]. Eur J Immunol. 2006; 36: 1882-1891.
[9] Gandhi N A, et al. Targeting key proximal drivers of type 2 inflammation in disease[J]. Nature Reviews Drug Discovery,2016,15:35-50.
[10] Le Floc’h A, et al. Dual blockade of IL-4 and IL-13 with dupilumab, an IL-4Rα antibody, is required to broadly inhibit type 2 inflammation[J]. Allergy . 2020;75(5):1188–1204.
(上海麥济生物技术有限公司 上海 201203)

