基于化学核心素养的思维模型建构
徐舒宁

摘 要:依据中学盐类水解教学实际,结合课标中“宏观辨识与微观探析”及“证据推理与模型认知”的素养要求和思维模型建构的相关文献,从溶液混合的分类、特殊用量关系、平衡常数以及图像中的特殊点等视角,探寻微粒在水溶液中的行为,进行盐类水解相关模型的建构实践,以帮助学生快速解决问题。
关键词:盐类水解;思维建模;特殊用量
盐类的水解是对平衡知识的延伸,从不同盐类的水溶液呈现的不同酸碱性,通过微观视角分析粒子间的相互作用,从而深刻认识盐类水解的本质及规律。《普通高中化学课程标准(2017版)》[1]对“盐类的水解”的相关内容提出如下要求:(1)能从化学平衡的角度认识盐类水解的原理,通过探究对氯化铁水解的促进或抑制说明影响盐类水解程度的主要因素,发展学生平衡观。(2)能从微观视角,通过泡沫灭火器、铝盐和铁盐的净水作用等,认识盐类水解的关键是弱酸根离子、弱碱阳离子的变化,发展学生的微粒观和守恒观。(3)选取学生熟悉的弱酸根离子和弱碱阳离子,引导学生关注对应弱电解质电离平衡常数的对比、电离平衡常数与水解平衡常数的转化,深刻体会不同离子水解程度的大小。
从近些年高考化学试卷来看,水解与电离平衡图像题是高考命题专家的最爱。而在检索到的有关盐类水解的文献中,不少学者对该部分内容的复习教学做了一些有益的探索,比如对水解平衡图像题的认知模型的建构,将图像与pH、pOH、粒子浓度等相结合形成坐标系[2],培养学生接受、吸收、整合化学信息的能力,分析和解决化学问题的能力。然而教学实践中发现,由于学生“宏观辨识与微观探析”素养的缺失,对盐溶液中的微粒观念淡薄,无法动态理解盐类水解时微观粒子间的相互作用。同时缺乏“证据推理与模型认知”素养,在分析多溶质体系中弱电解质的电离、盐类的水解及其相互影响关系上存在着较大的困难。因此,笔者认为,在此部分内容的复习教学中应从物质的分类、反应类型的辨识、物质间的定量关系、图像归类等角度帮助学生建立解题思维模型,以提高学生分析问题和解决问题的能力,帮助学生克服解题时存在的思维阻碍。
一、建构物质混合模型,看清化学问题实质
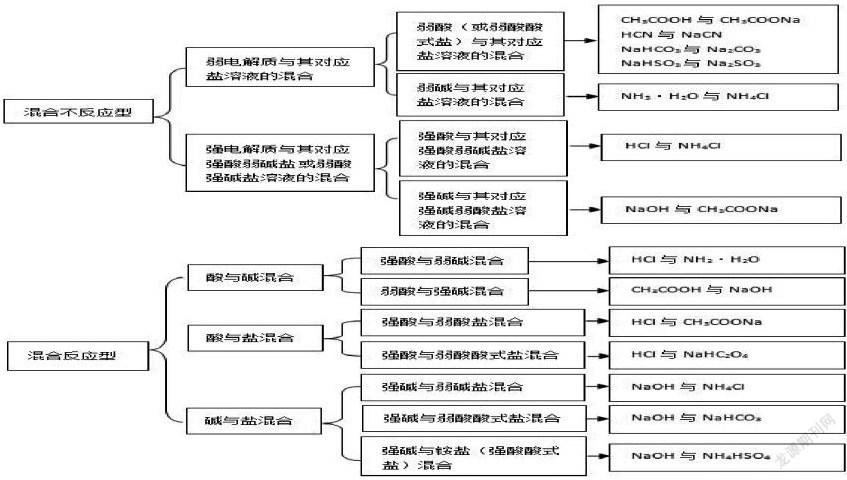
在盐类水解的复习教学中,溶液混合类型的题目比较常见。有的混合后两物质之间并没有发生化学反应,但有的物质混合之后会发生一定的化学反应,然后再分析水溶液中存在的弱电解质的电离及盐类的水解问题。因此,在对具体的溶液混合类题型的复习教学中,应该要引导学生将溶液的混合类型建构成模型,化抽象为具体,从而认清化学问题的实质。溶液的混合类型可通过以下模型来展现:
二、架构物质间的用量比模型,培养学生的定量思维
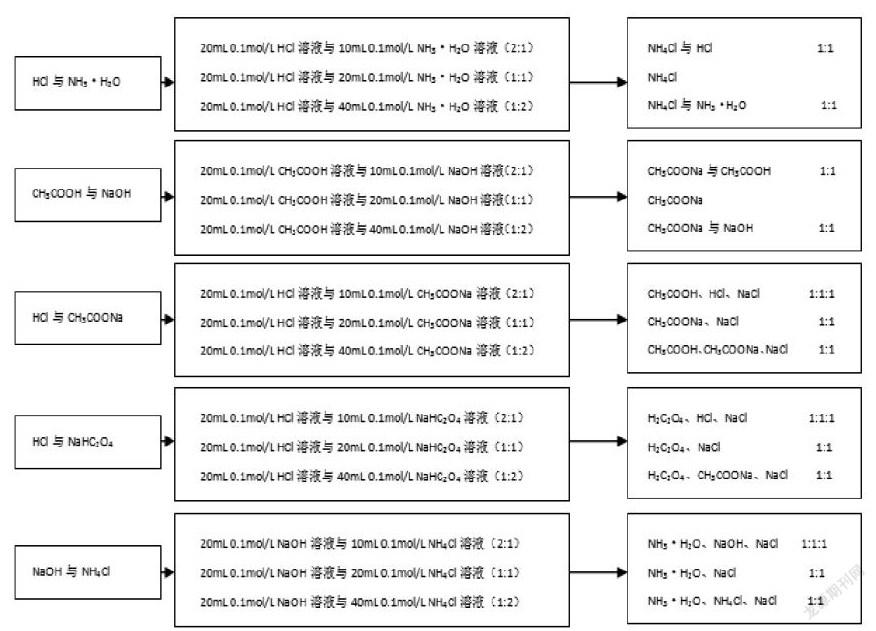
在与盐类水解有关的溶液混合反应型的题目中,在已知信息里有时会给出各物质的物质的量浓度和溶液的体积;有时题目中会先呈现出某一种物质的物质的量浓度和体积,而后给出图形坐标系,用横坐标的变化来表示所添加的另一种反应物的使用量,通过坐标中某几个特殊用量下所得溶液的pH让学生判断溶液中存在的溶质,并进一步分析离子浓度的前后变化与大小关系。而学生对此类题型由于缺乏相应的认知模型,思维固化,简单利用书中所学的碎片化知识进行解题,导致找不到解题的切入点,得分率比较低。因此,笔者认为,在此类题型的讲解中应该需要让学生看清题目中的几个特殊用量,尤其是这几个特殊用量下所隐藏的常见的物质间的比例关系,通过架构物质间的用量比模型,树立物质反应中的定量意识,分析混合后溶液中的溶质成分,培养学生定量分析化学反应的能力,并让学生学会建构模型、使用模型。
三、构建平衡常数模型,培养学生的逻辑思维
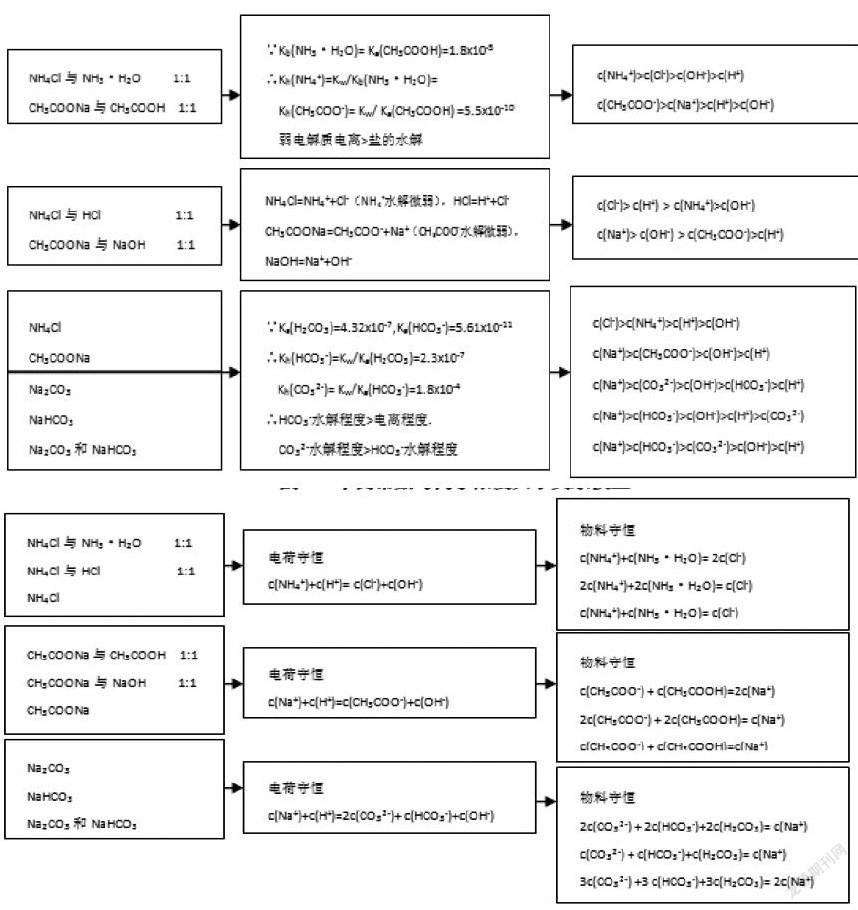
有了物质间用量比模型的建构,学生就可以很清楚地分析出混合后的水溶液中所含的物质及其相互之间的比例关系,为进一步分析溶液中所含微粒浓度的大小关系奠定了坚实的基础。然而,在模型建构的过程中发现,最后所得的水溶液中,有时溶质中只含某种易水解的盐,有时是盐与酸或盐与碱的混合物,有时又是易水解的正盐与其酸式盐的混合物,而有时还可以是盐与盐的混合物。因此,要想解决溶液中微粒浓度大小关系的对比问题,就需要学生能够对酸、碱、盐及酸式盐的性质有清晰的认识,知道哪些酸或碱存在电离平衡,哪些盐存在水解平衡,尤其要学会利用弱酸根离子或弱碱阳离子的水解平衡常数与其对应弱酸或弱碱的电离平衡常数的大小关系或相互之间关系式的换算来对比分析弱电解质与其对应盐的混合溶液中弱电解质的电离程度和其对应盐的水解程度的大小问题,进而判断出溶液中离子浓度的大小关系。
四、解构滴定图像模型,提高学生的解题效率
在近些年的高考化学试题中,水解与电离平衡的坐标图像题不断推陈出新,。如何能够让学生快速、准确而又有效地解出此类试题成为许多一线教师重点关注的问题。正如分析多溶质体系中弱电解质的电离、盐类的水解及其相互影响关系上建构的用量比模型那样,图像问题的分析更需要让学生看清几个特殊用量下所隐藏的常见的物质间的比例关系,树立定量意识,因此关注图像上的特殊点是最好的解决问题的切入点。目前常见的图像有酸碱中和滴定曲线、微粒分布曲线、对数图像等,而图像上的特殊点主要有起点、半等点、中性点(常温下pH=7)、恰好完全反应点、过量点等[3]。
除此以外,学生要能够通过对图像上特殊点的分析得出对应点溶液中的溶质,并结合纵坐标的变化趋势,如溶液的pH变化、微粒的浓度变化、微粒浓度比值的变化、微粒所占的百分数变化等,尤其在近几年的高考复习中要特别关注对数与浓度的转化关系,从而进一步分析出溶液中水的电离程度的变化、盐类的水解程度的变化、弱电解质电离程度的变化及其相互之间的大小关系等,进而得出微粒浓度的大小关系,进行平衡常数的有关计算以及守恒表达式的书写等。
总而言之,盐类的水解部分是高中化学教学中的重要概念,也是学生感觉难度比较大的考点,对应题型呈现出来的综合性比较大,时常与弱电解质的电离部分进行融合考查。而题目中往往以图像分析题居多,并富含比较大的信息量,对知识的综合应用要求较高。因此,教师在平时对此部分的习题进行讲解时,要多通过对溶液混合分类模型、比例模型、平衡常数与微粒浓度大小关系模型以及图像模型的建构,让学生在解题中学会重点关注并分析特殊用量下水溶液中所包含的微粒及其相互之间的浓度大小关系,让学生学会“证据推理和模型认知”。让学生多从微观视角分析化学反应原理,培养学生“宏观辨识与微观探析”的核心素养。引导学生在分析问题和解决问题的过程中学会建构模型,将知识、题目情境和解题思维有效结合。学会利用模型来分析问题和解决问题,從而看清问题实质。同时在模型的应用过程中还要注意引导学生多注意审题,将所学知识进行迁移应用,将题目中呈现的信息与所构建的模型进行融合运用。
当然已建构出来的模型也并不是十分完美,新题目还在不断涌现,题目情境也在不断翻新,对知识点的考查也更加灵活,同时具有一定的隐蔽性。因此,要求教师和学生在日常的做题和讲题中解题思维还需要不断深入,还需在平时各类试题的训练中不断补充和完善模型,只有这样才能让建构出来的模型具有可持续性的使用价值。
参考文献
[1]中华人民共和国教育部,普通高中化学课程标准(2017版).北京:人民教育出版社,2018.
[2]范东旭、吴林.水解电离平衡图像题解题模型建构及教学启示[N].中学生导报,2020-06-16.
[3]邢泰宇.离子图像题的教学思考:2017年全国新课标I卷第13题分析[J].化学教学,2018(3):82.

