水和二甲基亚砜协同改善Cs4PbBr6纳米晶的光学性能
石子宽,杨宇,林良武
水和二甲基亚砜协同改善Cs4PbBr6纳米晶的光学性能
石子宽,杨宇,林良武
(中南大学 轻质高强结构材料重点实验室,长沙 410083)
采用以丙酮、油胺(OM)和油酸(OA)为前驱体,水和二甲基亚砜(DMSO)为辅助剂的配体辅助再沉淀法,制备高发光、稳定的Cs4PbBr6纳米晶。通过透射电子显微镜(TEM)、X射线衍射仪(XRD)、漫反射吸收光谱、荧光光谱、和傅里叶变换红外光谱(FTIR)分析水和二甲基亚砜对Cs4PbBr6光学性能的协同影响机理。结果表明,水和二甲基亚砜的引入可以完全占据铅离子的空位,使溴离子更容易嵌入位点,从而促进结晶;二者协同作用能有效促进配体与Cs4PbBr6表面相结合,从而优化钝化效果;同时,可以促使Cs4PbBr6纳米晶基体中产生Cs4Pb- Br6/CsPbBr3的镶嵌结构,极大地改善了Cs4PbBr6纳米晶的光学性能。
Cs4PbBr6纳米晶;Cs4PbBr6/CsPbBr3;水;二甲基亚砜;钝化效应
2016年,CHEN等[1]和SAIDAMINOV等[2]报道了具有强而稳定的绿色光致发光(PL)的Cs4PbBr6粉末。不久之后,第一批关于Cs4PbBr6纳米晶体(NCs)的报道随即出现[3−4]。与CsPbBr3相比,Cs4PbBr6具有更好的稳定性,如防潮、耐热等。此外,Cs4PbBr6与其它类型铅基钙钛矿一样属于离子晶体,因此在遇到强极性的水时易分解。但是研究发现在合成过程中少量水不仅不会使Cs4PbBr6的光学性能下降,反而会显著改善其光致发光量子产率。ZHOU等[5]使用水/二甲基亚砜/二甲基甲酰胺体系合成了Cs4PbBr6,其中水的引入可以有效地解决Cs+离子的溶解问题,并且产物产率高达73%,光致发光量子产率高达76%。WANG等[6]采用溶液法制备了Cs4PbBr6纳米晶,其研究结果表明水提供的羟基能与Cs4PbBr6基体形成缺陷能级,从而改善光学性能。而二甲基亚砜作为一种合成Cs4PbBr6晶体的常用辅助剂,它能与Pb2+进行配位形成Pb—O键,诱导产物转化为Cs4PbBr6晶体[5],并且在二甲基亚砜中合成的Cs4PbBr6晶体,通常以Cs4Pb- Br6与CsPbBr3混合的形式存在[7],其光学性能并不能得到有效地改善。然而水和二甲基亚砜协同对Cs4-PbBr6光学性质的影响机理尚未见报道。本文将探讨水和二甲基亚砜协同改善Cs4PbBr6光学性能的机理。以期为解决钙钛矿的水解问题提供参考依据。
1 实验
1.1 实验原料
溴化铯(CsBr,99.5%)、溴化铅(PbBr2,AR,99.0%)、油胺(OM,80%~90%)和二甲基亚砜(DMSO)购自上海阿拉丁有限公司。油酸(OA、AR)和丙酮购自国药集团化学试剂有限公司。
1.2 Cs4PbBr6纳米晶的合成
在室温下将25 mL丙酮装入150 mL锥形瓶中,随后,向锥形瓶中加入5 mL油酸和2.5 mL油胺,搅拌1 min使其均匀分散,并在室温静置6 h得到前驱液。然后通过控制辅助剂中水和DMSO的添加,分成了4组实验:不添加水和DMSO (1#)、只添加水(2#)、添加水和DMSO(3#)和只添加DMSO(4#),以此来探究水和二甲基亚砜对Cs4PbBr6光学性能的协同影响机理。其中在实验3#中,将1 mmol PbBr2(0.367 g PbBr2溶于4 mL DMSO)和1 mmol CsBr (0.213 g CsBr溶于0.5 mL去离子水中)加入锥形瓶中(其它实验中水或DMSO的添加量与3#实验保持一致),剧烈地搅拌(2400 r/min)20 min。通过紫外线照射,可以看到强烈的绿色荧光,这表明成功地合成了Cs4PbBr6。将产物7 000 r/min离心10 min,得到沉淀物,分散于10 mL丙酮中,超声清洗5 min,再7 000 r/min离心10 min,室温下真空干燥24 h,制得粉末。
1.3 表征
采用瑞士Advance D8型X射线衍射仪(XRD)进行物相分析,选用Cu靶的Kα射线,工作电压和电流分别为40 kV和200 mA,步长0.02 (°)/s,扫描范围 10°~60°。在场发射扫描电子显微镜(JEM-2100F,日本)上进行显微观察。在全功能荧光光谱仪(FLS-1000,英国爱丁堡)上获得光致发光光谱(PL)、光致发光激发光谱(PLE)和光致发光衰减谱。用UV-3600紫外−可见分光光度计(日本京都岛津)测量紫外可见光吸收光谱。在傅里叶红外光谱仪器(iS5,Thermo,美国)上测量3 800~4 000 cm−1范围内的傅里叶变换红外光谱(FTIR)。
2 结果与讨论
2.1 光学性能
通过控制前驱体中水和DMSO的添加,分成了4组实验:原始(1#)、水(2#)、水和DMSO(3#)和DMSO (4#)。图1(a)为4#样品的XRD图,在20.7°,29.6°,36.4°,42.2°,47.4°,52.4°处角度分别对应于CsBr (JCP- DS 73-0391)的(100),(110),(111),(200),(210),(211)晶面,无其它物相的杂峰,产物为溴化铯,无法合成Cs4PbBr6纳米晶。因此,下文不再对4#样品进行讨论。
图1(b)和(c)所示为在环境光和紫外线灯下1#、2#和3#样品分散在丙酮中的光学照片。从图中可以清楚地看到,3组样品无论是在环境光还是紫外光下都有显著的差异。并且可以看到3#样品相较于其它两个样品有更强烈的绿色荧光效应,这说明水和二甲基亚砜协同显著地改善了Cs4PbBr6样品的光学性能。由光致发光发射光谱(激发波长:360 nm)图1(d)所示可以看到,与1#样品(峰值520 nm)相比,水的加入(峰值527 nm)使其红移,而水和二甲基亚砜共同加入(峰值513 nm)使其蓝移,且能显著提高Cs4PbBr6的荧光强度和半高宽(23 nm)。这是因为水可通过部分溶解反应物和加速纳米粒子内的质量传输来改善纳米粒子形成期间的重构过程,从而降低缺陷密度对非辐射复合通道的抑制影响[8]。由图1(e)中可以看出,吸收光谱由约320 nm处的尖锐吸收峰和宽吸收带(360~550 nm)组成。320 nm附近的强吸收峰与Cs4PbBr6有关,源于孤立的PbBr64–八面体中局域态之间的光学跃迁[9]。LI等[10]报道,纯CsPbBr3纳米粒子的吸收峰位于510 nm左右,因此,可以推测,图1(d)~(e)中520 nm附近的吸收峰和强PL峰来自CsPbBr3纳米粒子的干涉。
2.2 显微组织
为了证明CsPbBr3的存在,通过高分辨透射电镜对样品的微结构进行表征。如图2(a)所示,正方形纳米晶均匀分布且尺寸相对均一(约15 nm)。右侧插图的快速傅立叶变换(FFT)图像证实了原始样品中的单斜CsPbBr3和六角形Cs4PbBr6共存。两条红色条纹的晶面间距为0.44 nm,属于六方Cs4PbBr6(JCPDS 74-2378)的(300)晶面。黄色条纹的晶面间距分别为0.46 nm和0.63 nm,分别属于单斜CsPbBr3(JCPDS 73-2463)的(021)和(012)晶面。如图2(b)所示,添加水和二甲基亚砜后,可以清楚地看到CsPbBr3嵌入Cs4PbBr6中形成CsPbBr3/Cs4PbBr6镶嵌结构,晶面取向也发生变化,这是因为在合成过程中,水和二甲基亚砜完全占据了铅离子的空位[11],这使得溴离子更容易嵌入该位点,从而具有更好的结晶效果。

图1 (a) 4#样品的XRD图谱;(b) 环境光下1#、2#和3#样品分散在丙酮中(浓度为50 mg/mL)的光学图片;(c) 紫外灯下3个样品对应的光学图片;(d) 1#样品、2#样品、3#样品的光致发光发射;(e) 3个样品的吸收光谱

图2 1#样品(a)和3#样品(b)的高分辨透射电镜(HRTEM)图像
如图3所示,XRD清楚地显示形成了六方Cs4PbBr6(JCPDS 74-2378)。1#样品中,角度在18.7°、21.8°处的峰分别对应PbBr2(JCPDS 85-1089)的(002)、(012)晶面,角度在29.5°、52.3°处的峰分别对应CsBr (JCPDS 73-0391)的(110)、(211)晶面,说明原料没有充分反应,这是由于两种原料(PbBr2和CsBr)在溶液中溶解度较小,导致无法充分反应。相比之下,2#样品和3#样品为无残留的Cs4PbBr6,并且XRD没有属于CsPbBr3的峰,说明CsPbBr3的含量很低。同时,窄而尖的峰表明样品的高结晶度。此外,晶格应变与晶格缺陷有关,可用Hall-Williamson方法计算,计算结果列于表1中。1#样品和2#样品的晶格应变比3#样品的晶格应变高一个数量级,对应于光致发光发射光谱的发光强度(图1(d)),这也为Cs4PbBr6晶体结构的发光提供了证据。说明水和二甲基亚砜的加入可以有效地改善Cs4PbBr6纳米晶的晶格完整性。
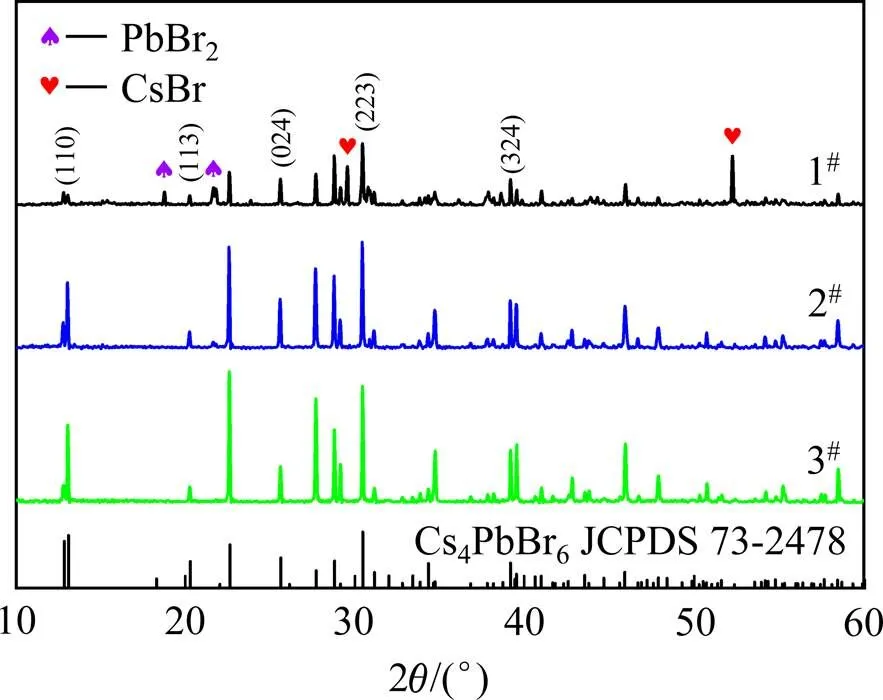
图3 1#、2#和3#样品的XRD图

表1 Cs4PbBr6的参数和晶格应变
OM和OA通常用作表面配体,在合成的过程中起到很好的钝化作用[12]。图4(a)所示为3组样品的傅里叶变换红外光谱(FTIR),图中可以看出,3 450、2 930、2 850、1 710、1 560、1 470和1 410 cm−1处峰强度均有变化。3 450 cm−1处的峰来自于水的—OH,从图中可以看出,1#样品也出现了属于—OH的峰,这可能是由于吸收了空气中的水。2#样品和3#样品有较强的—OH峰,这是由于合成过程中极少量的水进入Cs4PbBr6的晶格,与基体发生结合形成羟基子亚能 带[13]。1 710 cm−1处的峰为C=O在COO—中的反对称拉伸振动,而1 560 cm−1处的峰为质子化NH3基团的对称弯曲振动,证实了质子化油酸胺的存在[14]。1 470 cm−1和1 410 cm−1处的峰为C—N,表明油酸与油胺反应生成长碳链有机配体。此外,为了证明小分子水进入Cs4PbBr6晶格之中,测定25 ℃和100 ℃退火2 h后3#样品的FTIR谱,如图4(b)所示。可以看出退火前后3 450 cm−1处峰强明显不一致,100 ℃退火2 h可以基本去除样品表面附着的水,但退火后3#样品仍存在较强的属于—OH的峰(3 450 cm−1),由此证明了小分子水进入Cs4PbBr6晶格之中。同时相较于25 ℃退火样品3#的—OH峰,峰强的变化也显示表面有水 附着。

图4 (a) 为1#样品、2#样品、3#样品的FTIR谱;(b) 为25 ℃和100 ℃退火2 h后3#样品的FTIR谱;(c)~(e) 为1#样品、2#样品、3#样品的光致发光衰减谱
图4(c)~(e)为3组样品的光致发光衰减谱。ZHENG等[15]的研究表明,长的载流子复合寿命(即量子寿命)意味着较低的表面缺陷浓度,较好的钝化效果。样品的荧光强度()符合双指数衰减模型,如下 所述:

平均量子寿命的计算公式[17]:
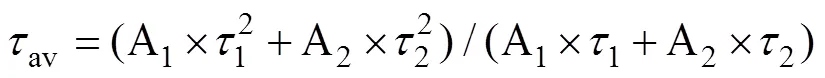
式中:A1和A2为常数,为时间;1,2分别为与陷阱辅助复合和载流子辐射复合有关的短寿命和长寿命[16]。光致发光衰减曲线可以由式(1)进行拟合,根据式(2)获得平均量子寿命(av)。通过式(1)和(2)的拟合和计算;得到各个样品的平均量子寿命,列于表2,3个样品的平均量子寿命分别为3.69、4.15和4.91 μs。结果表明,水和二甲基亚砜的协同作用能有效降低Cs4PbBr6纳米晶缺陷密度,优化钝化效果,这与上述FTIR结果相印证。
2.3 水和二甲基亚砜协同改善Cs4PbBr6光学性能机理分析
结合上述分析,总结出水和二甲基亚砜协同改善Cs4PbBr6光学性能机理,如图5所示。对于合成初期形成的纯Cs4PbBr6,水和二甲基亚砜的引入改善了Cs4-PbBr6纳米晶的结晶性和表面缺陷,优化了钝化效果。同时,少量H2O分子进入Cs4PbBr6晶格中,并且溶解了Cs4PbBr6中不稳定的CsBr,进而让Cs4PbBr6分解为CsPbBr3,镶嵌在Cs4PbBr6基体中(Cs4PbBr6+H2O→CsPbBr3),最终形成Cs4PbBr6/CsPbBr3的镶嵌结构(图2)。这种镶嵌结构中Cs4PbBr6作为包覆层很好地钝化作为发光源的CsPbBr3杂质,从而极大地改善其光学性能(图1(d)),这与CHEN等[18]的研究结果相一致。
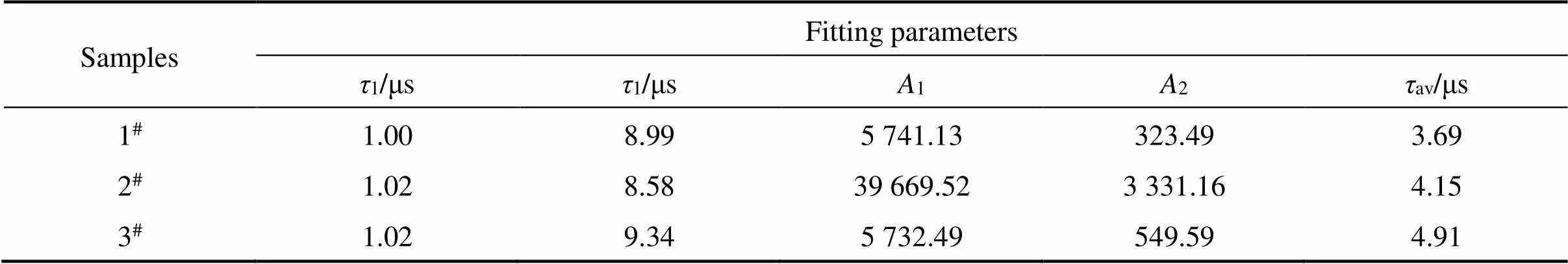
表2 1#、2#和3#样品的光致发光衰减谱拟合
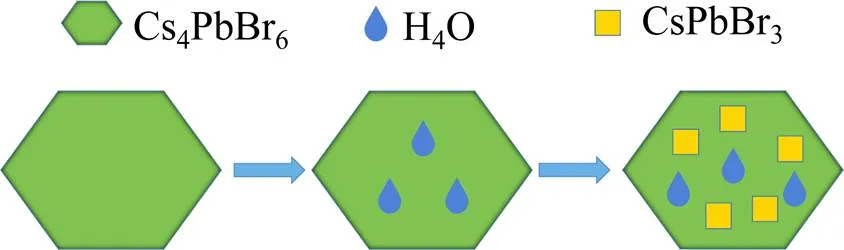
图5 Cs4PbBr6/CsPbBr3的镶嵌结构的形成示意图
3 结论
1) 在Cs4PbBr6纳米晶的合成中,水和二甲基亚砜可以完全占据铅离子的空位促进结晶,这使得溴离子更容易嵌入位点,从而结晶更好。
2) 水和二甲基亚砜协同作用能有效促进配体与Cs4PbBr6表面结合,从而优化钝化效果;同时,可以促使Cs4PbBr6纳米晶基体中产生Cs4PbBr6/CsPbBr3镶嵌结构,从而极大地改善Cs4PbBr6纳米晶的光学性能。
[1] CHEN D Q, WAN Z Y, CHEN X, et al. Large-scale room- temperature synthesis and optical properties of perovskite-related Cs4PbBr6fluorophores[J]. Journal of Materials Chemistry C, 2016, 4(45): 10646−10653.
[2] SAIDAMINOV M I, ALMUTLAQ J, SARMAH S, et al. Pure Cs4PbBr6: Highly luminescent zero dimensional perovskite solids[J]. ACS Energy Letters, 2016, 1(4): 840−845.
[3] AKKERMAN Q A, PARK S, RADICCHI E, et al. Nearly monodisperse insulator Cs4PbX6(X=Cl, Br, I) nanocrystals, their mixed halide compositions, and their transformation into CsPbX3nanocrystals[J]. Nano Letters, 2017, 17(3): 1924−1930.
[4] ZHANG Y H, SAIDAMINOV M I, DURSUN, et al. Zero -dimensional Cs4PbBr6perovskite nanocrystals[J]. Journal of Physical Chemistry Letters, 2017, 8(5): 961−965.
[5] ZHOU B, DING D, WANG Y, et al. A scalable H2O-DMF- DMSO solvent synthesis of highly luminescent inorganic perovskite-related cesium lead rromides[J]. Advanced Optical Materials, 2021, 9(3): 2001435.
[6] YUAN Y, LIU Z M, LIU Z Y, et al. Photoluminescence and self-assembly of cesium lead halide perovskite nanocrystals: Effects of chain length of organic amines and reaction temperature[J]. Applied Surface Science, 2017, 405: 280−288.
[7] CHA J H, HAN J H, YIN W P, et al. Photoresponse of CsPbBr3and Cs4PbBr6perovskite single crystals[J]. Journal of Physical Chemistry Letters, 2017, 8(3): 565−570.
[8] ZHOU H P, CHEN Q, LI G, et al. Interface engineering of highly efficient perovskite solar cells[J]. Science, 2014, 345(6196): 542−546.
[9] NIKL M, MIHOKOVA E, NITSCH K, et al. Photoluminescence of Cs4PbBr6crystals and thin films[J]. Chemical Physics Letters, 1999, 306(5/6): 280−284.
[10] LI X M, WU Y, ZHANG S L, et al. CsPbX3quantum dots for lighting and displays: Room-temperature synthesis, photoluminescence superiorities, underlying origins and white light-emitting diodes[J]. Advanced Functional Materials, 2016, 26(15): 2435−2445.
[11] LIU M, ZHAO J, LUO Z L, et al. Unveiling solvent-related effect on phase transformations in CsBr-PbBr2system: Coordination and ratio of precursors[J]. Chemistry of Materials, 2018, 30(17): 5846−8552.
[12] UDDIN M A, MOBLEY J K, MASUD A A, et al. Mechanistic exploration of dodecanethiol-treated colloidal CsPbBr3nanocrystals with photoluminescence quantum yields reaching near 100%[J]. Journal of Physical Chemistry C, 2019, 123(29): 18103−18112.
[13] WANG X, YU J, HU M Y, et al. The effects of hydroxyl by water addition on the photoluminescence of zero-dimensional perovskites Cs4PbBr6nanocrystals[J]. Journal of Luminescence, 2020, 221: 116986.
[14] LIU Y, GUO M R, DONG S, et al. Room temperature colloidal synthesis of CsPbBr3nanowires with tunable length, width and composition[J]. Journal of Materials Chemistry C, 2018, 6(29): 7797−7802.
[15] ZHENG X P, CHEN B, DAI J, et al. Defect passivation in hybrid perovskite solar cells using quaternary ammonium halide anions and cations[J]. Nature Energy, 2017,2(7): 17102.
[16] SUN S B, YUAN D, XU Y, et al. Ligand-mediated synthesis of shape-controlled cesium lead halide perovskite nanocrystals via reprecipitation process at room temperature[J]. ACS Nano, 2016, 10(3): 3648−3657.
[17] LIANG Z Q, ZHAO S L, XU Z, et al. Shape-controlled synthesis of all-inorganic CsPbBr3perovskite nanocrystals with bright blue emission[J]. ACS Applied Materials & Interfaces, 2016, 8(42): 28824−28830.
[18] CHEN Y M, ZHOU Y, ZHAO Q, et al. Cs4PbBr6/ CsPbBr3perovskite composites with near-unity luminescence quantum yield: large-scale synthesis, luminescence and formation mechanism, and white light-emitting diode application[J]. ACS Applied Materials & Interfaces, 2018, 10(18): 15905−15912.
Synergistic improvement of optical properties of Cs4PbBr6nanocrystals by water and dimethyl sulfoxide
SHI Zikuan, YANG Yu, LIN Liangwu
(National Key Laboratory of Science and Technology on High-strength Structural Materials, Central South University, Changsha 410083, China)
We developed a new ligand assisted reprecipitation method (LARP) for synthesis of highly luminescent and stable Cs4PbBr6nanocrystals, in which acetone, oleamine (OM) and oleic acid (OA) were used as precursor, water and dimethyl sulfoxide (DMSO) as adjuvant.The synergistic influence mechanism of water and DMSO on the optical properties of Cs4PbBr6was analyzed by transmission electron microscopy (TEM), X-ray diffraction (XRD), diffuse reflection absorption spectrum, fluorescence spectroscopy and fourier transform infrared spectroscopy (FTIR). The results showed that the addition of water and dimethyl sulfoxide can completely occupy the vacancy of lead ion and promote the crystallization, which makes bromine ion easier to embed into the site, and so that the crystallization is better. The synergistic effect of water and dimethyl sulfoxide can effectively promote the binding of the ligand to the surface of Cs4PbBr6, thus optimizing the passivation effect. At the same time, this synergistic effect can promote the formation of Cs4PbBr6/CsPbBr3mosaic structure in Cs4PbBr6nanocrystalline matrix, which greatly improves the optical properties of Cs4PbBr6nanocrystals.
Cs4PbBr6nanocrystals; Cs4PbBr6/CsPbBr3; water; DMSO; passivation effect
O649.1
A
1673-0224(2021)04-381-06
装备预研重点实验室基金资助项目(6142912xxxx);湖南省自然科学基金面上项目(2018JJ2509)
2021−03−18;
2021−04−19
林良武,博士。电话:18890393866;E-mail: linliangwu@csu.edu.cn
(编辑 谭彦妮)

