食用小麦后运动诱发过敏反应的研究进展
袁娟丽,吴双双,张冉冉,武 涌,陈红兵
(1.南昌大学 药学院,江西 南昌 330006;2.南昌大学 中德联合研究院,江西 南昌 330047;3.江西省微尺度交叉科学重点实验室,江西 南昌 330031)
食物依赖运动引起的过敏反应 (Food-Dependant Exercise-Induced AnaphyIaxis,FDEIA)是摄入食物后进行运动而导致的一种特殊类型的过敏反应。l983年Kidd等首先提出FDEIA概念[1]。而Kushimoto等于1985年首先报道了小麦相关的FDEIA。这种疾病被称为小麦依赖运动诱发的过敏反应(Wheat-Dependant Exercise-Induced Anaphylaxis,WDEIA)[2]。
小麦具有很高的营养价值和适口性,可以加工成许多食物,如面包、啤酒等。然而,小麦越来越被认为是引起免疫介导的食物过敏的主要诱因之一,包括IgE和非IgE介导的食物过敏。IgE介导的小麦过敏可分为呼吸过敏(面包师哮喘和鼻炎)、小麦食品过敏和WDEIA[3-4]。WDEIA患者仅能耐受小麦制品的摄入,但当同时存在其他辅助增强因素,如运动、感染等,会出现严重的I型过敏反应[5-8]。为科学地认识并有效防治WDEIA,作者主要介绍WDEIA的流行病学、发病机制、临床症状及其诊断和治疗方法。
1 流行病学研究
小麦是诱发FDEIA的最常见的食物。Silvade报告了斯里兰卡两个过敏反应诊所在2011—2015年共19例FDEIA患者的回顾性研究,19例患者均有小麦依赖性运动诱发的过敏反应[9]。2012年,在日本横滨地区的初中生中,FDEIA的发病率为0.018%,学生男女比例为1∶1,致病食物分别为甲壳动 物(n=5)、小麦(n=4)和未知(n=5),WDEIA占28.57%[10]。这与之前的研究没有显著性差异[11]。而横滨地区的小学生FDEIA的患病率为0.004 7%,明显低于初中生,其中WDEIA占50%[12]。有研究发现韩国首尔国立大学医院2000—2006年过敏病人发病率为0.014%,其中18例被诊断为FDEIA,致病食物 为 小麦(n=14)、苹果、虾(n=1)、未 知(n=2),WDEIA占77.78%[13]。随后在2013年有关韩国成人小麦过敏的报告中,6例小麦过敏中有3例是WDEIA,占50%[14]。
WDEIA可以在任何年龄表现出来,且多见于没有任何食物过敏史的青少年和成年人[15]。WDEIA在成人中的发生频率高于儿童,主要发生在18~30岁的年龄范围内[16-17]。有研究对2010—2014年在北京协和医院确诊为WDEIA的283名患者的性别、来源地及发病年龄进行统计分析,发现54%(153/283)的患者为男性;81.2%的患者来自以小麦为主食的中国北方,其中96名患者来自北京,占总人数的33.9%;32名患者来自湖北,占总人数11.3%;29名患者来自内蒙古,占总人数的10.2%;第一次发生过敏反应的平均年龄为(34.1±13.5)岁[18]。
2 发病机制
WDEIA在小麦过敏原和辅助因素共同作用下表现出过敏症状。运动、服用非甾体抗炎药以及感染等辅助因素可促进肥大细胞脱颗粒、释放组胺;增加肠道通透性,促进过敏原的吸收[19],而使患者出现过敏症状。
2.1 过敏原和致敏表位
小麦蛋白质占小麦籽粒质量的10%~15%,根据蛋白质在盐中的溶解度可分为两部分:1)水/盐溶性组分包括白蛋白和球蛋白,占总蛋白质质量的15%~20%;该组分包括淀粉酶/胰蛋白酶抑制剂(AAI)亚基以及其他蛋白质,如脂质转移蛋白(LTP)[20];2)水/盐不溶性组分(麸质蛋白)包括麦醇溶蛋白和麦谷蛋白,约占小麦蛋白质质量的80%,其中麦谷蛋白约占这一比例的一半[21-23]。麦醇溶蛋白根据电泳率的不同,又分为α/β、γ、ω型;而麦谷蛋白根据相对分子质量的大小,分为高相对分子质量麦谷蛋白亚基(HMW-GS)和低相对分子质量麦谷蛋白亚基(LMW-GS)[24]。
据报道,小麦麸质蛋白中的α/β-麦醇溶蛋白,γ-麦醇溶蛋白,ω5-麦醇溶蛋白,LMW-GS和HMW-GS是导致WDEIA的过敏原[25-27],其中ω5-麦醇溶蛋白和HMW-GS是主要过敏原,且部分过敏原的IgE结合表位序列已从日本和欧洲WDEIA患者中鉴定得到(见表1)。
2.2 辅助因素
2.2.1 运动诱发WDEIA最重要和最普遍的辅助因素是身体活动。诱发过敏所需的运动强度因患者而异。有研究表明[18],大多数反应发生在低强度运动(如散步等)之后。Wong等人[36]指出,相对较低的运动强度(步行15 min)即可在WDEIA患者中引起反应。运动可以通过以下几种不同的途径起作用:1)在运动过程中,转谷氨酰胺酶(TG2)可能被激活,这导致小麦肽段和TG2之间的缀合,随后与IgE结合[37],但是这种缀合物在循环中的存在仍未被证实;2)剧烈运动时产生乳酸等酸性代谢产物,导致血液pH值降低,可能增强肥大细胞活性;此外,运动还可增高体温,促进肥大细胞等炎性反应细胞释放炎性介质[16,38];3)运动和乙酰水杨酸能增加胃肠道通透性,并促进过敏原吸收到循环血液中[39];4)运动引起肠道局部渗透压增加,肥大细胞脱颗粒,从而增加肠道通透性[40-41];5)运动期间血流再分布可能携带过敏原至组织,其中含有对这些过敏原不耐受的肥大细胞,这可能是导致运动期间过敏反应的原因[42]。
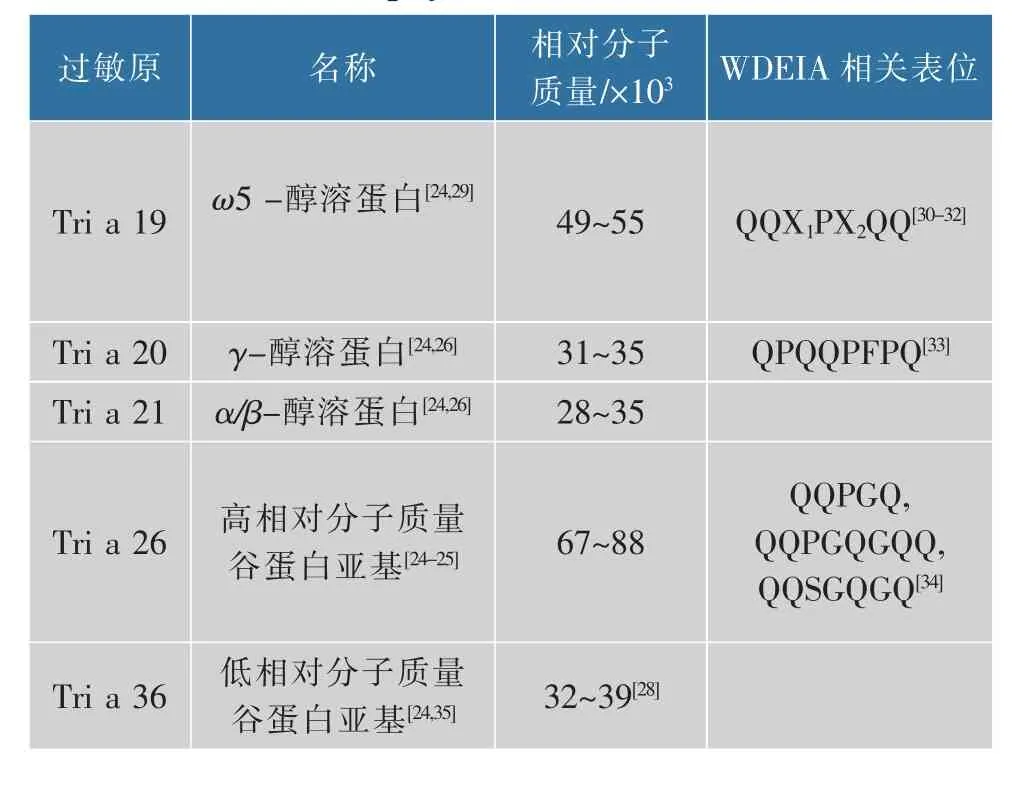
表1 导致小麦依赖运动诱发的过敏反应(WDEIA)的过敏原及其IgE结合表位Table 1 Allergen and IgE-binding epitopes identified as associated with wheat-dependent exerciseinduced anaphylaxis(WDEIA)
2.2.2 乙酰水杨酸和其他非甾体抗炎药(NSAIDs)在某些情况下,WDEIA不是由摄食小麦和运动相结合诱导的,而仅是因摄入小麦制品并服用了非甾体抗炎药乙酰水杨酸所诱发[43],且低剂量的乙酰水杨酸就足以诱发WDEIA[44]。研究表明,乙酰水杨酸是引起WDEIA患者严重过敏反应的重要辅助因素。研究人员报告了20例服用乙酰水杨酸后出现严重过敏反应的WDEIA病例[45]。除乙酰水杨酸外,吲哚美辛、布洛芬和双氯芬酸钠等非甾体抗炎药可能诱发WDEIA[46-48]。
非甾体抗炎药可与肠道黏液层和细胞表面磷脂双层相互作用,线粒体氧化磷酸化解偶联,导致肠细胞损伤和肠道通透性增加;抑制环氧合酶(COX),减少微血管的血流量,且在胃酸、胃蛋白酶、胆汁、肠道细菌等侵害性因子作用下,导致胃肠道损伤(炎症、糜烂和溃疡)[49];损伤胃肠道的细胞紧密连接,通透性增加,促进过敏原的吸收[39,50],辅助诱发WDEIA。此外,非甾体抗炎药可通过增加Syk激酶活化来加速组胺释放[48,51]。
2.2.3 乙醇和感染乙醇也可以作为诱发WDEIA的辅助因素[52],据报道它可以增加胃过敏原吸收并增加组胺释放[53]。乙醇还可能通过氧化应激引起肠道通透性增加[54]。此外,感染尤其是早期阶段或临床轻度形式,可作为辅助因素来增加过敏反应。与其他辅助因素相比,感染更加危险,因为无法避免或被预防[55]。
3 临床症状
WDEIA的症状通常在小麦摄入后短时间内由身体活动引起,但在极少数情况下可能会发生延迟发作[56]。相反,如果在运动后很快摄入食物,也可能出现症状[57]。WDEIA事件的发生频率因病人而异,从单一发作到多次发作[58],临床表现和严重程度也各不相同。WDEIA的典型症状是瘙痒、局部或全身性荨麻疹、血管性水肿,这些症状在运动后几分钟内就会出现,并可发展为呼吸困难、胃肠道症状、低血压以及过敏性休克[8,16,59]。
4 诊断
WDEIA的准确诊断对于避免进一步的严重反应是非常重要的。然而,由于疾病的罕见性,诊断时间滞后非常频繁[8]。事实上,WDEIA经常被误诊为其他更常见的疾病,如荨麻疹、运动性过敏反应或特发性过敏症[8]。诊断工具可分为体内试验,如皮肤点刺试验(SPT)和激发试验;体外试验,包括嗜碱性粒细胞活化试验(BAT)、组胺释放试验(HRT)和小麦蛋白特异性IgE试验。
对于疑似WDEIA的诊断,可能需要进行激发试验,即口服小麦制品后在跑步机上进行最大限度的运动,以确认诊断[8,55],这有助于了解病理机制,在诊断不明确的情况下尤为重要。然而,激发试验只能确认约70%的患者的诊断[60-61],并且因为不能很好地控制给予的食物量和诱导反应所需的运动强度,风险性高[8,62-63]。而且试验结果阴性也并不能完全排除WDEIA,因为在受控制的激发试验中并未考虑其他辅助因素的影响,如运动强度、花粉接触、非甾体类抗炎药物或乙醇的摄入。因此,当血清小麦蛋白特异性IgE抗体检测结果为阳性并且临床病史提示WDEIA时,诊断时并不需要常规进行激发试验。
血清中过敏原特异性IgE抗体的测定,较常使用ImmunoCAP,它是过敏原特异性IgE抗体体外检测的金标准,可通过荧光酶联免疫测定法(FEIA)测定小麦蛋白的血清IgE抗体[64]。有研究发现重组ω5-醇溶蛋白特异性CAP的灵敏度为80%,而小麦提取物和麸质蛋白CAP的灵敏度分别为48%和56%[65]。此外,由ImmunoCAP检测ω5-醇溶蛋白与小麦蛋白的血清特异性IgE,并计算两者对数值的比值,该比值具有100%的敏感性和特异性,可用于WDEIA患者的诊断[66]。此外,与任何过敏性发作一样,急性发作后WDEIA患者的血清类胰蛋白酶水平升高,如果在急性反应后6 h内测定类胰蛋白酶含量,也有助于确定诊断[15]。
WDEIA建议的临床诊断标如下:当患者出现以 下1、2、3、4或1、2、3、5症状时,极有可能是WDEIA[16,18]。
1.当运动前摄入小麦制品,运动期间出现过敏反应体征和症状。
2.患者在摄入小麦制品后6 h内进行运动时发作。
3.小麦提取物特异性IgE阳性,尤其是麸质和(或)ω5-醇溶蛋白,麸质和(或)醇溶蛋白的皮肤点刺试验呈阳性。
4.在避免食用小麦制品或在食用小麦相关食品后6 h内避免运动,未发生WDEIA。
5.未进行运动,但在其他辅助因素如服用非甾体抗炎药(NSAIDs)、摄入乙醇的参与下出现症状。
5 治疗
5.1 避免小麦摄入或其与辅助因素的结合
对在低阈值(如体育活动)激发情况下即可诱发症状的或出现严重反应的患者,以及从事高职业要求(飞行员、警察等)的患者,推荐无麸质饮食;而在不太严重的情况下,避免小麦摄取与辅助因素结合可能就足够了,如仅在剧烈运动后发作者,建议其空腹运动或者运动前4~6 h避免摄入小麦制品,并随身携带急救药品[16,67]。此外,由于小麦蛋白与来自黑麦、大麦和燕麦的相应蛋白质的交叉反应性,患者是否还需避免摄入其他含谷蛋白的谷物,目前尚不明确。
5.2 药物作用
某些药物可预防WDEIA的发作。有报告显示盐酸奥洛他定和酮替芬可抑制FDEIA的过敏反应,其中激发食物包含小麦[68]。Choi报告了一例WDEIA,患者在食用小麦前服用酮替芬,激发实验为阴性且没有出现呼吸困难等症状,成功预防了WDEIA[69]。口服色氨酸钠(SCG)对于预防WDEIA的发作也有效[70]。Inoue等的研究表明米索前列醇能够抑制阿司匹林引起的WDEIA患者血清醇溶蛋白的升高,抑制过敏原的吸收,从而抑制过敏反应[71]。韩国WDEIA病例使用了INF-γ口服免疫疗法治疗后,患者可自由食用含小麦的食物[72]。
5.3 紧急措施
WDEIA的紧急治疗措施包括在早期警告信号出现时立即停止体力活动,一旦发生严重过敏反应,症状较轻时可以口服或肌注抗组胺药物,当出现呼吸困难、血压降低等症状时,需立即使用肾上腺素进行抢救[16]。此外,应指导患者如何使用肾上腺素自动注射器。使用自动注射器装置给予肾上腺素是有效的急救措施,剂量为0.15 mg或0.30 mg,注入股外侧肌(大腿外侧)。根据美国国立卫生研究院的指南,0.15 mg肾上腺素自动注射器应用于体质量小于或等于25 kg的儿童,包括体质量小于10 kg的健康婴儿;如果需要,可以在至少间隔5 min后再给予相同剂量[73]。
6 展望
WDEIA是一种相对罕见但可能导致严重过敏反应的食物过敏形式,目前尚欠缺详细的数据,但报道的病例数越来越多,特别是在亚洲和欧洲地区。与小麦过敏不同,WDEIA可耐受小麦制品的摄入,只有在伴随有运动等辅助因素的共同作用下才会发作,然而因诱发所需运动强度的个人差异性,以及其他辅助因素的多样性,使其易被误诊或延迟诊断。因此全面了解WDEIA的相关知识,跟进研究新进展,提高对WDEIA的意识,将有助于尽早诊断和有效防治。

