二甲醚水蒸气重整反应器的工艺参数分析
王庆武,李 聪
(上海工程技术大学车辆工程系,上海 201620 )
二甲醚(DME)水蒸气重整制氢为两步连续反应[1-2]:首先,二甲醚在酸性催化剂的作用下水解成甲醇;然后,甲醇在金属基催化剂作用下重整生成富氢气体。二甲醚水解生成甲醇的反应受热力学平衡控制,若水解生成的甲醇马上进行水蒸气重整反应,则能减少生成物的体积分数,使反应向正向进行,加快二甲醚水解的速度,提高二甲醚的转化率。
二甲醚水蒸气重整反应的关键是催化剂的选择和使用,开发高效、高稳定性的重整催化剂是目前研究的重点[3]。方奕文等[4]研究了分子筛催化剂的类型、硅铝比和Cu、Pd改性与否对二甲醚低温水解活性的影响,发现酸性MCM-22和HZSM-5分子筛催化剂的二甲醚水解活性较高,且活性随着分子筛硅铝比的增加而降低。T.A.Semelsberger等[5]研究了多种固体酸,如Y型分子筛、ZSM-5[m(Si)/m(Al)=2.5]分子筛、ZSM-5[(m(Si)/m(Al)=15.0]分子筛、ZrO2、γ-Al2O3和非酸性固体Si等,在二甲醚水解过程中的催化活性。二甲醚水解甲醇的活性随硅铝比和催化剂类型的变化趋势为:ZSM-5[m(Si)/m(Al)=15.0],ZSM-5[m(Si)/m(Al)=25.0],ZSM-5[m(Si)/m(Al)=40.0]>ZSM-5[m(Si)/m(Al)=140.0],Y[m(Si)/m(Al)=15.0]>Y[m(Si)/m(Al)=2.5]>γ-Al2O3/ZrO2。
目前,国内针对二甲醚重整制氢的研究不多。为此,本文作者设计一种含瓦片式加热通道的二甲醚重整制氢反应器,对反应过程进行数值模拟和实验验证,研究分析不同条件下反应器的性能,为反应器的优化设计提供理论依据。
1 数学模型
1.1 反应器模型
设计的二甲醚重整反应器由催化床、绝缘套组成,二甲醚和水蒸气混合气体进入反应器,反应气体流过反应器的入口,在催化床中发生化学反应。反应器的直径为30 mm、长度为150 mm。
二甲醚空气重整反应器示意图如图1所示。
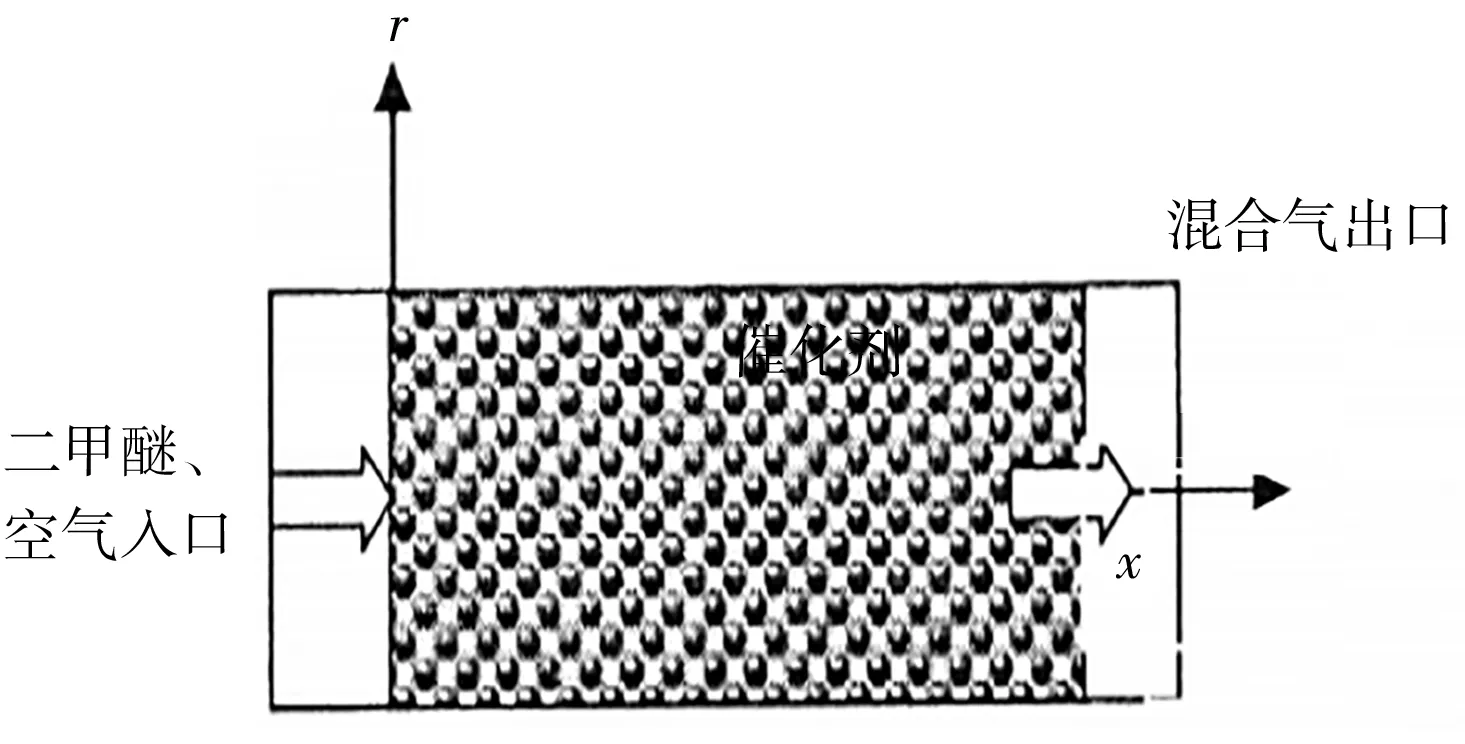
图1 二甲醚空气重整反应器示意图
1.2 模型假定
该模型的基本假设条件如下:①重整器为管状反应器,管内设有瓦片式加热通道,管内填充的催化剂假定为均匀的多孔介质;②在通道中,反应气体形成完全假设的层流,使得平均流场成比例地跨过反应器的压差;③反应速率是线性的;④气流仅在通道的方向上传输质量和能量;⑤反应气体是理想气体,不可压缩。
1.3 控制方程
在理想气体混合物的基础上,建立了包括质量守恒、动量守恒、能量守恒和化学物质守恒的控制方程。
气体在重整床中的流动采用达西定律[6]来描述:
(1)
式(1)中:ρ为气体密度;η为黏度;κ为多孔介质的渗透率;Psr为重整床的压强。
多孔床的平均温度分布和热容密度分别见式(2)、(3)。
(2)
(ρCp)T=ε(ρCp)f+(1-ε) (ρCp)s
(3)
式(2)、(3)中:f和s分别表示流体和固相;ε为流体的体积分数;Tsr为反应器温度;ksr为催化床的热弥散;Q为热源;v为流体速度;Cp为常压下的比热容;T为温度。
模型的质量平衡方程为稳态下的Maxwell-Stefan扩散和对流方程:
(4)

1.4 化学反应模型
二甲醚水蒸气重整的反应过程分为两步[7]:二甲醚水解生成甲醇[见式(5)]和甲醇水蒸气重整反应[见式(6)],同时,甲醇水蒸气重整反应又包含水气变换反应[见式(7)]。
CH3OCH3+H2O(g)⟺2CH3OHΔH=+23.6 kJ/mol
(5)
CH3OH+H2O⟺3H2+CO2ΔH=+49.5 kJ/mol
(6)
CO+H2O⟺CO2+H2ΔH=-41.17 kJ/mol
(7)
本文作者主要研究这3个反应的反应速率。对二甲醚水解反应、甲醇水蒸气重整和水气变换建立的化学反应动力学模型分别见式(8)-(10)。
(8)
(9)
(10)
式(8)-(10)中:r为反应速率;K为反应的化学平衡常数;k为反应速率常数;p为各组分的分压;下标H表示二甲醚水解成甲醇反应,MSR表示甲醇水蒸汽重整反应,WGS表示水汽转换反应,DME表示二甲醚,H2O表示水,M表示甲醇,CO表示一氧化碳,CO2表示二氧化碳,H2表示氢气。
DME水解反应的速率常数k可由Arrhenius方程计算:
(11)
式(11)中:A为指前因子;E为活化能;e为指数函数;R为摩尔气体常数。
由于实验温度设定在523~673 K,总体而言变化不大,对活化能的修正,最终归结到对指前因子A的修正。经过修正后的Arrhenius方程为:
(12)
式(12)中:kj是在温度T下的速率常数;EAj是在温度T下的活化能。
修正后的指前因子Asj的计算公式为:
(13)
式(13)中:Ksj为初始温度速率常数;Tsj为初始温度。
吸附平衡常数Kj以平均温度Tm(573 K)下的Kmj和吸附焓ΔHadsj作为拟合参数,表达式为:
(14)
1.5 边界条件
对重整催化床而言,入口和出口边界条件描述的是整个重整催化床的压力降。相对于该条件,所有其他边界没有压力降,则:
(15)
在反应器的出料口处,假设对流热传输占主导地位,则:
n·(-ksr▽Tsr)=0
(16)
同时,在出料口处,对流流量条件为:
(17)
在反应器出口处,假设对流热量传输占主导地位,则:
n·▽(-kg▽Tg)=0
(18)
式(18)中:g代表废气。
为了求解非线性方程组,基于有限体积法调用了一种计算流体动力学(CFD)程序。该程序使用压力和速度域耦合的简单算法。
重整器示意图如图2所示,模拟流化多孔区的长度为150 mm,直径为30 mm,外壳的厚度为3 mm。最大元素尺寸为150 mm,最小元素尺寸为2 mm。
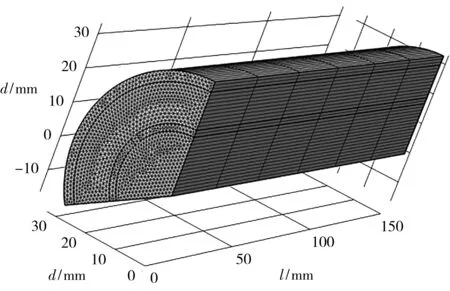
图2 重整器示意图
2 实验与模型验证
2.1 实验流程
为验证仿真模型的有效性,开展了二甲醚水蒸气重整实验,如图3所示。

图3 二甲醚重整制氢实验流程
流量计测得的蒸馏水在蒸发器内充分蒸发,空气、二甲醚(山东产,99%)和水蒸气被预热到723 K;然后,混合气体通过气体混合器进入反应器,反应器中充满CuO/ZnO/Al2O3+ ZSM-5分子筛催化剂(山东产)。反应后的产物进入连接到计算机的GC-900C气相色谱仪(上海产)上,进行组分的测量,或经皂膜流量计计量后排空。
二甲醚重整反应最重要的性能指标主要包括二甲醚转化率XDME和氢产率YH2,分别按式(19)、(20)计算。
(19)
(20)
式(19)、(20)中:FDME,in、FDME,out分别为二甲醚在反应器入口和出口处的流速;FH2,out为反应器出口处氢气的流速。
2.2 实验结果与分析
实验条件与仿真条件相同,水醚物质的量比(水醚比)为2、3、4,入口温度为750 K,流速为0.1 m/s,压力为1.013×105Pa。二甲醚转化率和氢产率的实验值与仿真值见表1。
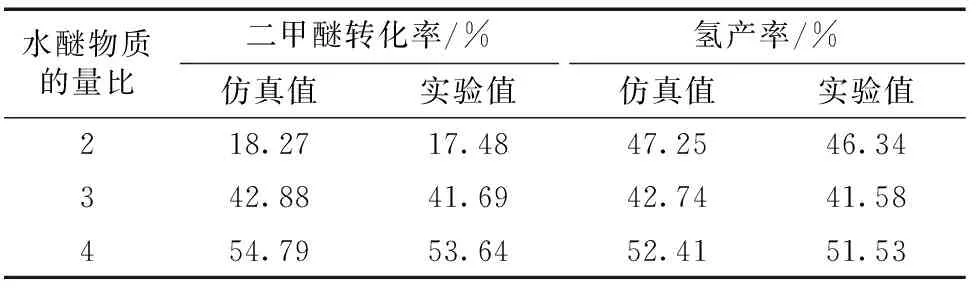
表1 二甲醚转化率和氢产率的实验值与仿真值
从表1可知,实验结果与仿真值较接近。实验氢产量下降的原因,可能是氢气溢出或氢气泄漏;实验值低于理论值,可能与不完全绝热和壁面散热有关。通过两项研究数据的对比,验证了该仿真模型可以详细描述重整反应。
2.2.1 温度的影响
在水醚物质的量比为4,热管入口流量为0.1 m/s,压力为1.013×105Pa,重整器入口温度分别为573 K、623 K和673 K的反应条件下进行模拟,二甲醚在不同的入口温度下转化率和氢气产率的变化见图4。
从图4可知,随着反应器入口温度的升高,二甲醚的转化率和氢气的产率提高。当水醚比为4、温度升至673 K时,二甲醚转化率与氢产率可达到最高值,分别为53.86%和53.22%。这是由于二甲醚水蒸气重整制氢的反应是吸热的,提高入口温度有利于提高反应的正向反应速率,并且反应朝着制氢的方向进行,从而提高了二甲醚的转化效率和氢气的产率。

图4 入口温度对二甲醚转化率和氢产率的影响
2.2.2 水醚物质的量比的影响
水醚比是影响二甲醚水蒸气重整制氢的一个主要操作参数。在热管入口流速为0.1 m/s、重整反应器入口温度为673 K、压力为1.013×105Pa的条件下,水醚比(2、3、4)对二甲醚转化率和氢产率的影响见图5。
+从图5可知,增加水醚比有利于提高重整器产氢率和二甲醚的转化率。当温度为623 K,水醚比增加到4时,重整制氢效率最大,此时二甲醚转化率和氢产率分别为52.30%和51.40%。从化学反应的原理来看,水醚比不能无限增大。反应为吸热反应,随着水蒸气含量的增加,反应器中的温度会降低,过量的水对正反应的反应速率有很大的影响,继而限制二甲醚的转化率和氢产率。
3 结论
设计了瓦片式重整制氢反应器,通过实验验证了反应器模型是可靠的,反应器的二甲醚转化率及产氢率表现良好。
温度和水醚比的增大,均可使二甲醚转化率和氢产率得到提高。过量的水会降低反应器温度,因此水醚比过高会影响二甲醚转化率和氢产率。
二甲醚水蒸气重整制氢反应器的数学物理模型可预测重整反应器的性能,建立的动力学模型可较为准确和具体地描述催化重整制氢系统反应的机制,给二甲醚水蒸气重整制氢微反应器的优化提供一定的参考。

