小儿止咳糖浆苯甲酸钠处方添加量及抑菌效力评估*
高 翔,佘 凡,马鹏飞△,刘 刚
(1. 陕西省食品药品监督检验研究院,陕西 西安 710065; 2. 陕西省杨凌示范区药品检验监测评价中心,陕西 杨凌 712100)
小儿止咳糖浆本身不具有充分的抗菌活性,且为多剂量包装,使用过程中需反复开启,存在被污染的风险,为保证产品的正常储存和使用,避免微生物生长与繁殖,根据制剂特性添加了抑菌剂苯甲酸钠[1-2]。小儿止咳糖浆曾收载于《中华人民共和国卫生部药品标准·中药成方制剂(第五册)》《国家中成药标准汇编中成药地方标准上升为国家标准部分口腔肿瘤儿科分册》,苯甲酸钠的处方添加量为0.5%。最近3 版《中国药典(一部)》均收载了该制剂的质量标准,其中2020 年版规定,苯甲酸钠的处方添加量为0.2%[3],并将2010 年版首次收载的抑菌剂效力检查法指导原则上升为抑菌剂效力检查法,要求更高,定位更准确[4]。但该制剂质量标准未制订苯甲酸钠具体的质量控制指标,作为药品的安全性评估,抑菌剂的添加量、抑菌效力是考察的重点,故本研究中对此进行了考察。现报道如下。
1 材料
1.1 仪器
2695 型高效液相色谱仪(美国Waters 公司);压力蒸汽灭菌器(上海华成医用核子仪器公司);HFsafe-760S 型生物安全柜(上海精宏实验设备有限公司);MJ-250-Ⅲ型霉菌培养箱(上海跃进医疗器械有限公司);LRH-250F 型生化培养箱(上海一恒科学仪器有限公司);PR224ZH 型电子天平(美国奥豪斯公司)。
1.2 试药
苯甲酸钠对照品(中国食品药品检定研究院,批号为100433-201702,供含量测定用);小儿止咳糖浆(样品A1-A3,华润三九<郴州>制药有限公司,国药准字Z43020385,批号分别为1804033N,1905016N,1905015N,规格为每瓶120 mL;样品B,广西维威制药有限公司,国药准字Z45021858,批号为180102,规格为每瓶120 mL;样品C,江西远东药业股份有限公司,国药准字Z36020251,批号为B180531,规格为每瓶120 mL;样品D,湖北诺得胜制药有限公司,国药准字Z42020245,批号为181001,规格为每瓶100 mL),包装均为口服液体药用聚乙烯瓶;甲醇、乙酸铵均为色谱纯;水为纯化水。
1.3 培养基
胰酪大豆胨琼脂培养基、胰酪大豆胨液体培养基、沙氏葡萄糖琼脂培养基、沙氏葡萄糖液体培养基,批号分别为1802052,190508,1801152,190702,均购于北京三药科技开发公司。培养基适用性检查符合2020 年版《中国药典》要求。
1.4 菌种
金黄色葡萄球菌[CMCC(B)26003],大肠埃希菌[CMCC(B)44102],铜绿假单胞菌[CMCC(B)10104],白色念珠菌[CMCC(F)98001],黑曲霉[CMCC(F)98003],鲁氏酵母菌[CICC1417];工作用菌株均为第3 代。鲁氏酵母菌来源于上海保藏生物技术中心,其他菌种来源于中国医学菌种保藏中心。
2 方法与结果
2.1 苯甲酸钠含量测定
2.1.1 色谱条件
色谱柱:WoburnStamsilC18柱(250mm×4.6mm,5μm);流动相:甲醇-0.05 mol/L 乙酸铵(5 ∶95,V/ V);流速:1 mL/min;检测波长:230 nm;柱温:30 ℃。
2.1.2 溶液制备
取苯甲酸钠对照品适量,精密称定,加水溶解,制成每1 mL 含苯甲酸钠0.1 mg 的对照品溶液;精密量取样品2 mL,置50 mL 容量瓶中,加水约40 mL,超声(功率为300 W,频率为40 kHz)处理20 min,取出,放冷,加水定容,摇匀,作为供试品溶液;取缺苯甲酸钠的阴性样品,同供试品溶液制备方法制成阴性对照品溶液。
2.1.3 方法学考察
专属性试验:取2.1.2 项下3 种溶液,按2.1.1 项下色谱条件进样测定。结果阴性对照品溶液色谱中,在与苯甲酸钠对照品溶液色谱相同保留时间处无干扰峰,表明专属性良好。详见图1。
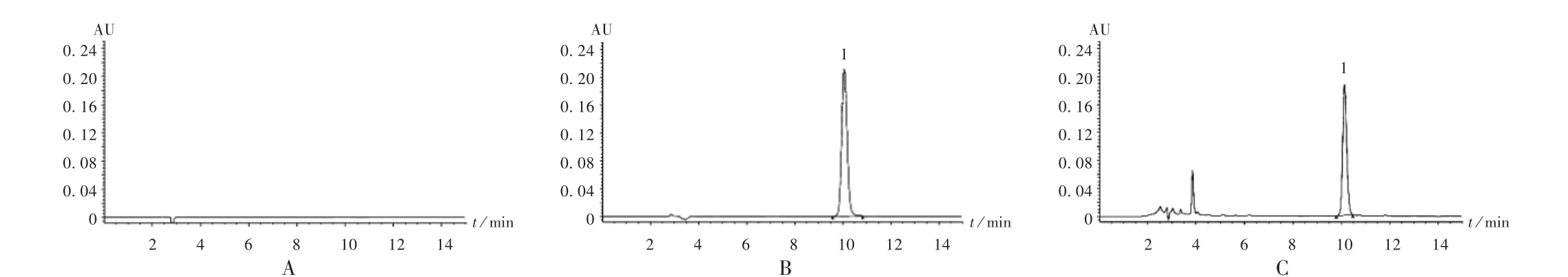
图1 高效液相色谱图Fig.1 HPLC chromatograms
线性关系考察:分别精密吸取苯甲酸钠对照品溶液(0.106 3 mg/mL)2,4,6,8,10,12 μL,按2.1.1 项下色谱条件进样,测定峰面积。以峰面积值(Y)为纵坐标、质量浓度(X,μg)为横坐标进行线性回归,得回归方程Y =3 228 068 X-75 910,r =0.999 9 (n =6)。结果表明,苯甲酸钠质量浓度在0.212 6 ~1.275 6 μg/mL 范围内与峰面积线性关系良好。
精密度试验:取2.1.2 项下对照品溶液,按2.1.1项下色谱条件重复进样6 次,测定峰面积。结果的RSD为0.46%(n =6),表明仪器精密度良好。
稳定性试验:取同一样品(批号为1804033N)供试 品溶液,在室温下分别于0,2,4,8,12,24 h 时按2.1.1 项下色谱条件进样,测定峰面积。结果的RSD 为0.19%(n =6),表明供试品溶液在室温下24 h 内稳定。
重复性试验:取同一批(含量为1804033N)样品,依法制备供试品溶液,平行制备6 份,按2.1.1 项下色谱条件进样测定。结果平均含量为2.054 mg/mL,RSD 为0.86%(n =6),表明方法重复性良好。
加样回收试验:精密量取已知含量的样品(批号为1804033N)1.0 mL,共9 份,置50 mL 容量瓶中,分别加入对照品溶液14,18,22 mL,平行加入3 份,依法制备供试品溶液,按2.1.1 项下色谱条件进样测定,记录峰面积并计算回收率,结果见表1。

表1 加样回收试验结果(n =9)Tab.1 Results of the recovery test(n =9)
2.1.4 样品含量测定
取不同批次样品适量,按2.1.2 项下方法制备供试品溶液,再按2.1.1 项下色谱条件进样测定,记录峰面积,并计算样品含量。结果样品A1,A2,A3,B,C,D 的含量分别为2.05,2.01,1.88,1.90,1.92,1.84 mg/mL,平均1.93 mg/mL。
2.2 抑菌效力测定
2.2.1 菌液制备
取金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌、白色念珠菌、鲁氏酵母菌的新鲜培养物,用无菌0.9%氯化钠溶液制成适宜浓度的菌悬液。取黑曲霉的新鲜培养物,加入适量含0.05%(V/ V)聚山梨酯80 的pH7.0 无菌氯化钠-蛋白胨缓冲液,洗脱孢子。然后,采用适宜方法吸出孢子悬液至无菌试管内,用无菌0.9%氯化钠溶液制成适宜浓度的孢子悬液。
2.2.2 方法适用性试验
进行抑菌效力检查前,需对供试品的计数方法进行验证,以确定该方法在抑菌剂效力检查时能有效检测出供试品中所有试验菌。按2020 年版《中国药典(四部)》存活菌数测定方法及方法适用性试验,对细菌数和真菌数采用1 ∶10 的平皿法(直径9 cm)进行计数。
2.2.3 抑菌效力测定方法
菌液组:无菌条件下,吸取20 mL 无菌0.9%氯化钠溶液加入无菌玻璃瓶中,平行制备6 份,将与样品组相同量的目标菌悬液加入其中,梯度稀释,采用平皿计数法计数,细菌于30 ~35 ℃培养3 ~5 d,真菌于20 ~25 ℃培养5 ~7 d 后,计算样品中试验菌菌数(即初始接种菌液浓度),并换算对数(lg)值。详见表2(表2、表3中“金葡”为金黄色葡萄球菌,“大肠”为大肠埃希菌,“铜绿”为铜绿假单胞菌,“白念”为白色念珠菌,“鲁氏”为鲁氏酵母菌,“黑曲”为黑曲霉)。
样品组:小儿止咳糖浆原包装瓶样品与菌液充分混匀。无菌条件下留取原包装瓶中样品20 mL,按目标菌的个数平行制备6 份,将2.2.1 项下制备的菌悬液各吸取0.2 mL 加入其中,使1 mL 供试品接菌量为105~106cfu,加菌量不超过容器中样品量的1%,于涡旋振荡仪振荡均匀。将制备好的供试液置23 ℃培养箱避光储存,分别在14 d 和28 d 对供试液中存活的微生物进行计数。
存活菌数测定:分别于第14,28 天将样品于涡旋振荡仪振荡均匀,无菌条件下,量取样品1 mL,用无菌0.9%氯化钠溶液梯度稀释制成1 ∶10,1 ∶102,1 ∶103的系列溶液,测定。培养物置规定温度、规定时间培养,逐日观察结果。根据菌落测定结果,计算1 mL 样品组各间隔时间的试验菌数量,并换算成lg 值。详见表2。

表2 小儿止咳糖浆接菌量、含菌量及lg 值Tab.2 Inoculated-pathogen quantity,germ-containing quantity and lg value of Xiaoer Zhike Syrup
口服制剂抑菌效力判断标准:按种14 d 时,金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌数量的lg 值减少不小于3,白色念珠菌、鲁氏酵母菌、黑曲霉数量的lg 值减少不小于1。试验菌增加数量的lg 值不超过0.5 为未增加。
结果判断:供试液中试验菌数量减少的lg 值为与前一测定时间点比较(14 d 比初始,28 d 比14 d)。接种试验菌14 d 时其数量的lg 值下降情况见表3。结果与14 d 时比较,28 d 时各样品中各类试验菌数量的lg 值均未增加。

表3 小儿止咳糖浆中第14 天时试验菌数量的lg 值降低情况Tab.3 The lg value of decrease of test bacteria in Xiaoer Zhike Syrup on the 14th day
3 讨论
本研究中参考文献[5-6],建立了小儿止咳糖浆中苯甲酸钠含量测定方法。该方法操作简便、结果准确、重复性好,可为小儿止咳糖浆中苯甲酸钠的含量测定提供参考。同时还对制剂中常用抑菌剂山梨酸钾、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯进行测定,均未检出。
4 个厂家、6 批次样品中的苯甲酸钠含量由高到低依次为A1>A2>C >B >A3>D,添加量范围为1.8 ~2.1 mg/mL,平均1.93 mg/mL,测定结果均在处方添加量的90% ~110%内。表明不同厂家、不同批次的样品抑菌剂种类、添加量、抑菌效力均符合药典标准。
糖浆剂系含有原料药物的浓蔗糖水溶液,蔗糖量应不低于45% (g/mL),小儿止咳糖浆蔗糖量为65% 。2020 年版《中国药典》规定含高浓度蔗糖的口服制剂抑菌剂效力测定时还应选用鲁氏酵母菌为试验菌株。鲁氏酵母菌耐高糖高盐高渗环境,可耐受60%蔗糖12%氯化钠,易致药物腐败,为糖浆剂常见的污染微生物。若小儿止咳糖浆加入鲁氏酵母菌进行抑菌效力试验,防腐体系的考察将更加科学、全面。
评估抑菌效力须先考察抑菌剂种类和添加量,防止企业因盲目追求抑菌效力,过量添加或联合添加的问题。企业应制订严格的内控质量标准,增加抑菌剂含量的质量控制方法。在确定抑菌剂种类和添加量的基础上,进一步考察抑菌体系控制微生物的能力,全面了解抑菌剂的使用情况,否则单纯评估抑菌效力意义不大[7-8]。
本试验中随着贮存时间的延长,细菌和真菌数量呈下降趋势;苯甲酸钠对细菌的抑制作用十分明显,但对真菌的抑制作用相对较弱,与相关文献报道一致[9-10]。
抑菌剂添加量“毒性-活性”的平衡,要求最低有效量,避免增加药品不良反应[11]。2010 年版以前的各版药典处方中抑菌剂的添加多依据使用经验和相关文献,缺乏试验数据支撑,添加量无验证依据。小儿止咳糖浆中苯甲酸钠的处方添加量由0.5%降至0.2%,14 d 时细菌、真菌下降的lg 值均符合规定。
抑菌剂具有一定的毒性,浓度过高会对婴幼儿产生潜在危害。人体每日的苯甲酸钠允许摄入量为0 ~5 mg/kg[12]。依据药品说明书,5 岁(体质量约17 kg)患儿口服小儿止咳糖浆1 次5 ~10 mL,1 d 3 ~4 次,即15 ~40 mL/d,含苯甲酸钠30 ~80 mg,已接近其允许最大摄入量(85 mg/d)。企业需进一步优化处方工艺,在保障抑菌效力的前提下,探讨更合理的添加量。
小儿止咳糖浆中含有大量的糖类物质,适合真菌生长。空气中的酵母菌、霉菌可致糖浆发酵、霉变、酸败及产生浑浊变质。建议企业开发单剂量包装,减少使用过程中的污染风险,进而减少抑菌剂的添加量,进一步提高药品的安全性。
处方中甘草流浸膏、桔梗流浸膏、橙皮酊均为乙醇浸出物,有辅助抑菌作用,故抑菌效力和抑菌剂添加量不完全呈正相关,样品A1并未显示比样品D 更好的抑菌效力。抑菌剂发挥抑菌效力,还需结合药物活性成分、pH、包装容器(如吸附作用)、辅料等因素进一步考察[13],但本研究中未做进一步探讨,有待后续试验开展研究。

