Pd/碳纳米管催化转移氢化大豆油工艺优化 及动力学分析
杜 晶,张晨晨,王 莹,高佳佳,朱秀清,,*,于殿宇,*,王立琦,罗淑年,,史永革
(1.东北农业大学文理学院,黑龙江 哈尔滨 150030;2.东北农业大学食品学院,黑龙江 哈尔滨 150030; 3.哈尔滨商业大学食品工程学院,黑龙江 哈尔滨 150028;4.九三粮油工业集团有限公司,黑龙江 哈尔滨 150090)
大豆油主要由含饱和脂肪酸和不饱和脂肪酸的甘油三酯组成。大豆油的氢化是油脂化学工业中的一个重要过程。经过氢化处理后的油脂中饱和脂肪含量增加,油脂的熔点和饱和度大幅升高,从而使其稳定性提高,同时油脂气味和色泽得到良好的改善,保存期得以延长[1-4]。 但油脂在氢化过程中会产生大量的反式脂肪酸(transfatty acids,TFAs)。摄入过多TFAs会对人体健康造成诸多负面影响,增加2型糖尿病、女性不孕、阿尔茨海默病及心血管等疾病的发生率[5-9]。因此,应尽可能在氢化过程中降低脂肪酸的不饱和度以及氢化后油脂中的 TFAs含量。
降低油脂氢化过程中TFAs的含量可以通过改变油脂氢化催化剂的组成实现。目前,油脂氢化催化剂多为雷尼镍,Ni的相对含量在90%以上,其比表面积较小,氢化过程中吸附氢的含量较少,造成氢化油脂中TFAs含量较高[10]。制备催化剂常用的载体有γ-Al2O3、Fe3O4、SBA-15及磁性材料等[11-14]。碳纳米管(carbon nanotube,CNTs)由于拥有纳米级管腔结构、较高的比表面积、类石墨的多层管壁等特点,在用作催化剂载体方面有着良好的应用前景[15]。Pd催化剂与Ni和Cu催化剂不同,其在油脂氢化过程中添加量低,但是依然能发挥较高的催化剂性能,是一种被广泛应用的油脂氢化催化剂,受到越来越多研究者的关注[16]。Plourde等将Pd分别负载于SBA15、MCM14载体上,研究了新型负载型Pd催化剂对向日葵油加氢过程中顺式单烯烃活性和选择性的影响[17]。 宋兰等采用浸渍方法制得Pd/C催化剂,通过比较大豆卵磷脂氢化过程中碘值的变化,从而探究制备条件对Pd/C活性的影响,并通过透射电子显微镜观察了催化剂的表观形态变化[18]。
为降低氢化过程中产生的TFAs含量,可以采用超临界流体氢化技术、电化学氢化技术及催化转移氢化技术等。超临界流体氢化大豆油的氢化时间较短,但反应是在高压条件下进行的,反应环境较为苛刻[19]。电化学氢化虽避免了高压,反应条件较为温和,但其氢化反应速率较慢[20]。催化转移氢化是一种氢气被氢供体取代的氢化大豆油技术[21],其可以避免高温高压,反应速率快。但对其研究多针对单金属催化剂催化转移氢化植物油。
本实验将Pd/CNTs催化剂应用在催化转移氢化体系下氢化一级大豆油,研究供体浓度、催化剂添加量和氢化温度对氢化过程的影响,并对其进行优化。根据氢化油脂过程中脂肪酸的变化趋势,研究油脂氢化反应过程的动力学反应速率常数、氢化选择性和反式异构性。 从动力学的角度分析催化转移氢化大豆油在氢化选择性和降低反式脂肪酸含量等方面的优势,为指导油脂氢化工艺提供一定的理论支撑。
1 材料与方法
1.1 材料与试剂
一级大豆油(碘值130 g/100 g) 九三粮油工业集团有限公司;Pd/CNTs催化剂为实验室自制;其他试剂均为国产分析纯。
1.2 仪器与设备
7890A气相色谱仪 美国安捷伦科技有限公司;DF-101S集热式恒温加热搅拦器 河南省予华仪器有限公司;DF205真空干燥箱 北京西城医疗器械二厂;DT100单盘精密电子天平 上海仪田精密仪器有限 公司;氢化反应釜为实验室自制。
1.3 方法
1.3.1 大豆油的催化转移氢化
150 mL的反应釜预热至一定温度(50、60、70、80 ℃),然后向反应釜中加入90 g一级大豆油、一定量的催化剂Pd/CNTs(0.10%、0.15%、0.20%、0.25%,添加量以体系质量计)和供体甲酸铵溶液(0.08、0.16、0.24、0.32、0.40 mol/50 mL)。在磁力搅拦下将反应釜置于水浴中。待温度恒定开始计时,反应一段时间后趁热将大豆油与催化剂离心分离,测定氢化大豆油的碘值及主要脂肪酸相对含量。
1.3.2 碘值的测定
参照GB/T 5532—2008《动植物油脂 碘值的测定》测定碘值。
1.3.3 主要脂肪酸含量的测定
样品甲酯化方法参照王立琦等的方法[22]。
气相色谱条件:CP-Sil-88强极性毛细管气相色谱柱(25 m×0.32 mm,0.20 μm);氢火焰离子检测器;载气N2,流速30 mL/min;燃气H2,流速30 mL/min;助燃气为空气,流速300 mL/min。
1.3.4 催化转移氢化大豆油的响应面优化试验设计
在单因素试验基础上,将Pd/CNTs催化剂应用于催化转移氢化大豆油,采用Box-Behnken软件进行响应面试验设计,以供体浓度(A)、催化剂添加量(B)和氢化温度(C)为自变量,氢化大豆油碘值(R)为响应值设计响应面试验,如表1所示。
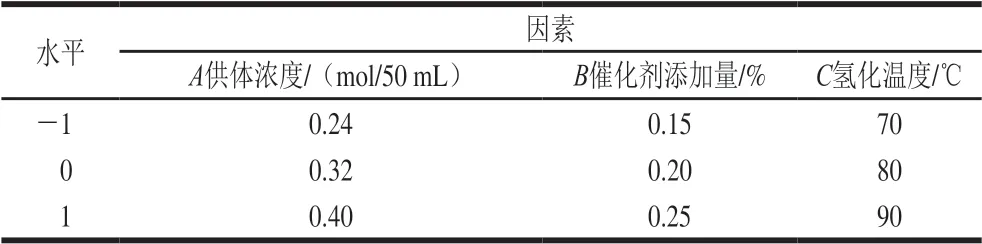
表1 响应面试验因素与水平Table 1 Codes and levels of independent variables used for response surface analysis
1.3.5 催化转移氢化大豆油的动力学分析
研究Pd/CNTs催化剂催化转移氢化大豆油的动力学,其路径采用Albright在Bailey模式的基础上提出的大豆油氢化反应路径[23]:
假设反应过程中氢气体积恒定,催化剂没有失去活性,有如式(1)~(3)的动力学方程。
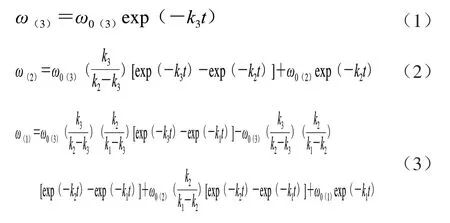
式中:ω(3)、ω(2)、ω(1)分别代表三烯酸、二烯酸、单烯酸在反应tmin时的质量分数/%;ω0(3)、ω0(2)、ω0(1)分别代表原料中三烯酸、二烯酸、单烯酸的质量分数/%;k3、k2、k1分别代表三烯酸、二烯酸、单烯酸的反应速率常数。利用非线性回归法解出 式(1)~(3)的微分方程,求出各反应路径的速率常数。
1.4 数据处理与分析
所有实验进行3 次平行,计算其平均值和标准偏差。使用Origin 8.5软件绘制图表。利用Design Expert 8.0.6软件进行方差分析。使用Matlab 2016a软件计算氢化反应的动力学参数。
2 结果与分析
2.1 大豆油催化转移氢化体系条件的确定
2.1.1 供体浓度
在温度80 ℃、添加催化剂Pd/CNTs占大豆油质量0.2%条件下氢化90 min,氢化过程中甲酸铵离子浓度对大豆油碘值的影响如图1所示。随着供体浓度从0.08 mol/50 mL增加到0.32 mol/50 mL时,大豆油中的碘值快速降低。这是因为反应溶液中氢供体多,使负载到催化剂上吸附态的氢增多,导致反应速率快。但供体浓度进一步增加至0.40 mol/50 mL时, 获得的最终碘值仅与0.32 mol/50 mL时有较小差异,这可能是因为供体浓度为0.40 mol/50 mL时,吸附到催化剂上的氢达到一定限度,反应速率减慢[24]。考虑到这一因素,认为0.32 mol/50 mL是进一步实验的最佳供体浓度。
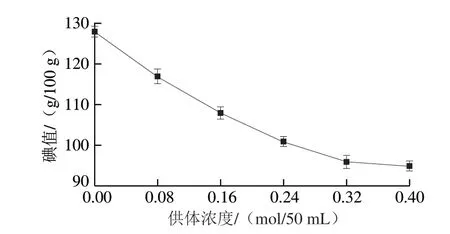
图1 供体浓度对氢化大豆油碘值的影响Fig.1 Effect of formate ion concentration on iodine value of hydrogenated soybean oil
2.1.2 催化剂添加量
在氢化温度80 ℃、供体浓度0.32 mol/50 mL条件下氢化大豆油90 min,氢化过程中催化剂添加量对大豆油碘值的影响如图2所示。随着催化剂添加量增加,碘值呈下降趋势。但碘值的下降速率并不均匀,这种现象可能是因为在催化剂添加量低于0.2%时,由于甲酸根离子、铵根离子和水分散作用,油不容易分散在水溶液中。甲酸根离子、铵根离子和水与催化剂接触,阻碍了氢化反应的发生[25]。当催化剂添加量高于0.2%时,油可以逐渐吸收到催化剂表面上,催化剂可以获得额外的活性位点,并降低催化剂表面上氢原子的解吸率,导致氢化水平提高[26]。但较高的催化剂添加量也可能导致催化反应速率降低,这是因为催化剂颗粒聚集减少了有效表面积。因此,氢化过程中催化剂添加量应控制在0.2%。

图2 催化剂添加量对氢化大豆油碘值的影响Fig.2 Effect of catalyst dosage on iodine value of hydrogenated soybean oil
2.1.3 氢化温度
90 g大豆油中供体甲酸铵浓度为0.32 mol/50 mL、催化剂添加量为0.2%、氢化90 min,改变氢化温度,其对氢化大豆油碘值的影响图3所示。随着氢化温度从50 ℃升高到80 ℃,大豆油中的碘值急剧降低,这可能是在氢化 过程中大豆油的C18:1和C18:0含量增加,C18:2和C18:3含量下降,导致大豆油的饱和度提高,碘值下降[25]。当温度高于80 ℃时,反应保持较高的速率,降低了氢化反应过程所需能耗,但高温条件下进行氢化反应也容易生成TFAs[27]。因此,要生产氢化率较高的低TFAs氢化大豆油,氢化温度选择控制在80 ℃。
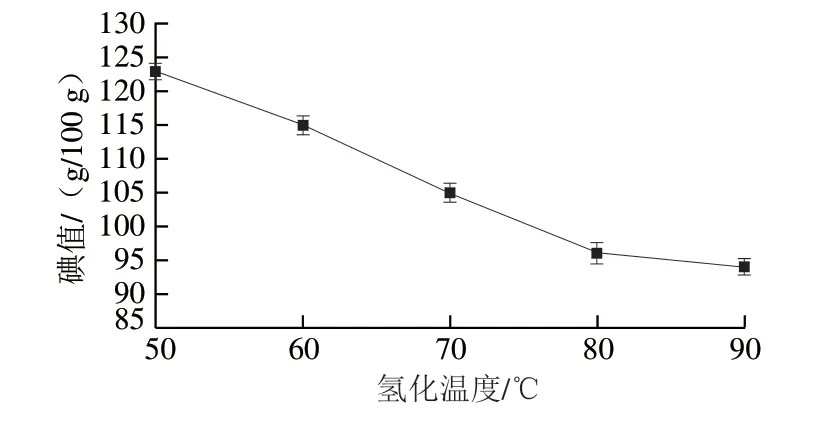
图3 氢化温度对氢化大豆油碘值的影响Fig.3 Effect of hydrogenation temperature on iodine value of hydrogenated soybean oil
2.1.4 大豆油催化转移氢化体系条件优化
在单因素试验的基础上,采用Box-Behnken方法,以供体浓度(A)、催化剂添加量(B)、氢化温度(C)为自变量,以碘值(R)为响应值设计三因素三水平响应面试验。试验设计方案如表2所示。

表2 响应面试验设计方案及结果Table 2 Experimental design and results for response surface analysis
将试验所得数据进行多元回归拟合,得到碘值(R)对供体浓度(A)、催化剂添加量(B)以及氢化温度(C)的回归方程:R=93.4-2.88A-1.50B-3.13C+6.75AB+2.50AC+0.75BC+7.05A2+6.30B2+3.55C2。
试验结果的方差分析采用Design Expert 8.0.6软件,结果如表3所示。方程因变量与自变量之间的线性关系明显,模型回归显著,失拟项不显著(P>0.05),并且 模型R2为0.991 9,为0.981 4,说明该模型与试验结果拟合度良好,供体浓度、催化剂添加量和氢化温度的交互作用对氢化大豆油中碘值的响应面分析结果如图4所示。

表3 方差分析结果Table 3 Analysis of variance
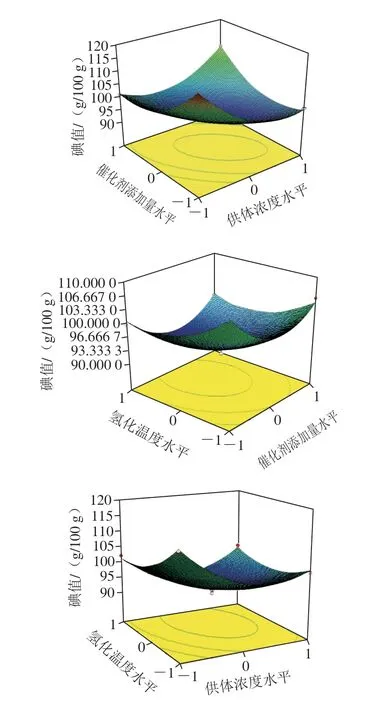
图4 两两交互作用对碘值影响的响应面图Fig.4 Response surface plots describing the effect of interaction among factors on iodine value
应用响应面优化分析方法对回归模型进行分析,确定最优响应结果,如表4所示。为检验响应面法所得结果的可靠性,按照上述优化值(供体浓度0.33 mol/50 mL、催化剂添加量0.2%、氢化温度84 ℃)进行验证实验,得到的氢化大豆油中碘值为95.3 g/100 g,TFAs相对含量为10.2%。预测值与实验值之间拟合良好,证实了模型的有效性。
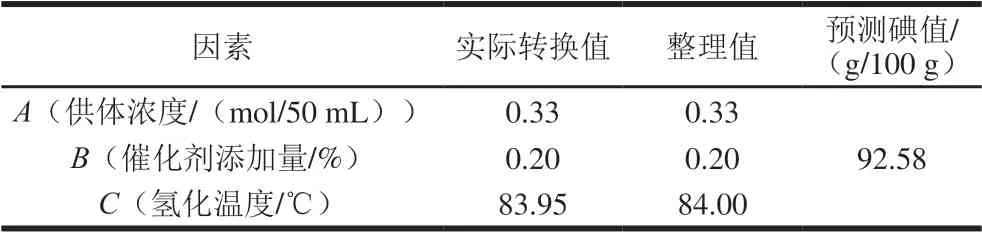
表4 响应面寻优结果Table 4 Results of response surface optimization
2.2 催化转移氢化大豆油的动力学分析结果
用Pd/CNTs作为催化剂催化转移氢化大豆油,所得氢化大豆油脂肪酸含量的预测值与实验值如图5所示。
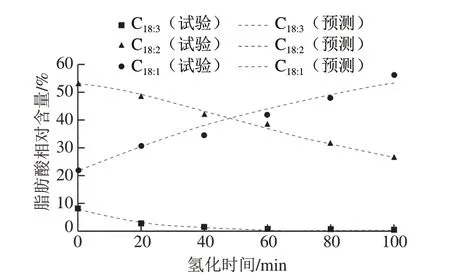
图5 氢化大豆油脂肪酸相对含量的预测值和实验值Fig.5 Good fitting between predicted and experimental fatty acid relative content of hydrogenated soybean oil
从图5中可以看出,三烯酸和二烯酸的相对含量会随着反应氢化时间的延长而下降,单烯酸相对含量随着反应时间的延长而增加。此外,氢化大豆油脂肪酸含量实验值与预测值的拟合程度较好。与动力学模型所描述基本吻合。
根据氢化大豆油脂肪酸含量的实验值计算出氢化大豆油的动力学反应速率常数及选择性,结果如表5所示,三烯酸、二烯酸和单烯酸反应速率常数分别为 4.9×10-2、8.7×10-3和8.31×10-4,氢化亚麻酸(三烯酸)和亚油酸(二烯酸)的选择性分别高达5.63和10.47。

表5 催化转移氢化条件下大豆油样品的动力学参数和脂肪酸含量Table 5 Kinetic parameters and fatty acid contents of soybean oil samples subjected to different durations of catalytic transfer hydrogenation
从表5中可以得出,大豆油氢化过程的反应速率常数为k3>k2>k1,说明氢化过程中三烯酸优先于二烯酸先被氢化,二烯酸优先于单烯酸先被氢化,这与Jovanović等的研究结果[28]趋势相一致,可能是因为三者的碳碳双键在氢化时都需要依靠催化剂降低反应的活化能,其中单不饱和脂肪酸氢化生成饱和脂肪酸所需活化能最大,而三烯酸生成二烯酸所需活化能最小,因此三稀酸的速率常数最大,而单烯酸的速率常数最小。此外,氢化亚麻酸的选择性为5.63,氢化亚油酸选择性为10.47。Zhao Yue等对大豆油进行氢化得到氢化亚麻酸选择性为1.2,氢化亚油酸选择性为5.8[29],本实验所得氢化亚麻酸和亚油酸选择性分别比其高出4.43和4.67。Zheng Huanyu等利用Pt/CNTs催化剂在固体聚合物电解质反应器中氢化大豆油,所得氢化亚麻酸和亚油酸的选择性仅分别为1.25和0.55[30],远低于本研究结果。本实验中反应速率常数远高于Tike等的研究结果(k3:1.2×10-3、k2:3.7×10-4、k1:2.9×10-5)[31]。本实验利用Pd/CNTs催化剂催化转移氢化大豆油,由于氢化反应的温度较低,并且由甲酸铵供体提供的H+传质速率要比提供氢气的氢化反应速率快,氢化后的大豆油中TFAs含量低,因此效果更好。
3 结 论
本实验在催化转移氢化体系中氢化大豆油,对氢化条件进行单因素试验,并进一步通过响应面试验优化工艺条件,其最佳工艺条件为供体浓度0.33 mol/50 mL、催化剂添加量0.2%、氢化温度84 ℃。催化转移氢化大豆油过程在不添加氢气条件下,氢供体提供H+的传质速率快,反应温度低。采用Matlab软件中的自编程序计算氢化反应速率常数,得出催化转移氢化大豆油的动力学常数和Pd/CNTs催化剂对亚麻酸及亚油酸的选择性均较高。综上,由甲酸铵溶液作为氢供体提供H+的传质速率快,氢化时间缩短,大豆油中TFAs含量低,避免了常规氢化使用氢气而引起的安全问题。

