分析化学经典内容是培养本科生创新能力的源泉
陈永雷,吕文娟,陈宏丽,陈兴国
兰州大学化学化工学院,兰州 730000
分析化学经典内容是分析化学的核心,是分析化学长期科学研究和高水平应用成果的结晶,蕴含了丰富的创新思维和创新途径,认真学习、熟练掌握和深刻理解这些内容对于培养本科生的创新思维和创新能力十分重要。分析化学的新理论、新方法、新技术和新应用对培养本科生的创新思维和创新能力同样有着重要的作用。因此,采取卓有成效的方式讲授分析化学经典内容、适时引导学生了解分析化学前沿领域和创新性研究成果,激发本科生创新思维、培养本科生创新能力,是分析化学课堂讲授必须解决的重要问题之一[1]。为了解决这一问题,我们在长期的教学过程中进行了不懈的探索和实践,结合分析化学经典内容的讲授,以学生易于接受并有利于培养他们创新能力的方式将分析化学的新理论、新方法、新技术和新应用及时引入课堂,并鼓励学生在学习中积极运用这些知识提高自身的创新能力,取得了良好效果。下面将通过实例进行介绍。
1 通过使极弱酸强化实现其准确滴定和Kjeldahl法测定蛋白质的讲授培养本科生的创新思维和创新能力
通过某些特定的化学反应可使极弱酸强化以实现用强碱对其进行准确滴定的目的,现行分析化学教材中常以在水溶液中滴定硼酸(H3BO3)为例介绍本部分内容。由于H3BO3的解离常数很小(pKa=9.24),无法用强碱(如NaOH)标准溶液在水溶液中直接滴定,但基于其可与某些多元醇如甘露醇络合而被强化,生成的甘露醇酸用酚酞作指示剂可通过NaOH标准溶液直接滴定。在讲授这部分内容时,我们从分子结构出发仔细剖析甘露醇能使H3BO3强化的原因,引导学生认识到其本质是由于硼原子与甘露醇分子中的邻二羟基络合形成了稳定的络离子所致(图1)。

图1 H3BO3与甘露醇的络合反应[2]
进而我们启发学生思考,能否将硼原子与甘露醇分子中的邻二羟基络合形成稳定络离子的性质用于分析化学其他领域如手性药物的分离,并要求通过查阅文献回答这一问题。通过文献调研,学生发现确实可以利用这一性质通过L-酒石酸二丁酯和硼酸缓冲液反应原位合成L-酒石酸二丁酯-硼酸络合物手性选择剂(图2),使用该手性选择剂建立的毛细管电泳方法可较好地实现普罗帕酮、布拉洛尔、普萘洛尔、阿普洛尔、丙萘洛尔、托利洛尔、吲哚洛尔、氧烯洛尔、比索洛尔、美托洛尔等十对手性药物对映体的分离[3]。

图2 L-酒石酸二丁酯和硼酸的反应[3]
类似地,L-酒石酸二异丁酯分子中也有两个相邻的羟基,也可以和硼酸发生反应生成络合物手性选择剂L-酒石酸二异丁酯-硼酸,以其为手性选择剂建立的毛细管电泳方法也可实现上述十对手性药物对映体的分离[4]。
蛋白质是食品的重要组分之一,准确测定其含量对于食品安全是十分重要的。现有分析化学教材中介绍的测定蛋白质含量的方法主要是Kjeldahl法。我们在讲授Kjeldahl法时,在介绍了其测定蛋白质含量的原理后,要求学生指出该方法存在的主要问题。学生经过思考和讨论后认为该方法的主要问题是仅能测定食品中氮的含量而无法确定氮的来源,有可能给食品安全问题留下隐患。在“三聚氰胺”事件曝光后,我们要求学生思考如何测定食品如乳制品中非法添加的三聚氰胺的含量以确保食品中源于奶类的蛋白质含量测定的准确性。学生通过查阅文献后发现,利用毛细管电泳技术不仅能在30 min内完成牛奶、酸奶、全脂奶等乳制品中三聚氰胺含量的测定,而且结果完全满足国家标准[5]。
2 通过金属离子指示剂的讲授培养本科生的创新思维和创新能力
金属离子指示剂(In)是络合滴定的主要内容之一,迄今为止使用的金属离子指示剂是基于In与被滴定金属离子(M)反应形成与In本身颜色不同的络合物(MIn)并使被滴定溶液呈现MIn的颜色。当滴入EDTA (Y)时,游离的M被逐步络合。在化学计量点附近,MIn中的In被Y取代使In游离出来,溶液呈现In的颜色,指示终点已到达。由此可知,In的结构、性质等对指示剂的性能有着决定性的影响。现有的金属离子指示剂虽然能满足络合滴定分析的要求,但仍存在封闭和僵化等现象。因此,在讲授金属离子指示剂时,我们要求学生在掌握其基本内容的基础上思考近年来出现的新材料,如纳米材料是否可以用作络合滴定的指示剂。学生通过查阅文献发现,离子选择性纳米球不仅可以用作络合滴定的指示剂,而且其指示终点的原理与金属离子指示剂在本质上是相同的,此外该指示剂放置一周后仍能很好地指示滴定终点(图3)[6]。应指出的是,与传统的络合滴定法相比,以离子选择性纳米球作指示剂的络合滴定法的选择性更高。

图3 用于钙离子滴定的纳米球指示剂及滴定过程中溶液颜色的变化[6]
3 通过晶型沉淀形成过程的讲授培养本科生的创新思维和创新能力
迄今为止,关于晶型沉淀的形成,一般认为在沉淀过程中构晶离子首先在过饱和溶液中形成晶核,然后进一步成长为按原定晶格排列的晶型沉淀。由此可知,通过合适的方式在溶液中形成数量适宜的晶核对于形成晶型沉淀是十分必要的。鉴于此,在讲授沉淀形成的过程时,我们积极引导学生深入思考新型纳米材料如金属有机框架材料的形成过程,以培养学生的创新能力。学生查阅文献后发现,通过在溶液中形成数量适宜的晶核不仅是制备金属有机框架材料的方法之一,而且还可以制备具有手性的金属有机框架材料[7–10]。进一步,我们鼓励学生尝试将这种方法用于制备手性涂层毛细管并考查它们在手性物质分离中的应用(图4)。学生通过实验,以ZnO纳米颗粒为成核试剂成功制备了手性MOF [Zn(s-nip)2]n涂层毛细管,并以此为分离通道建立了分离单胺类神经递质肾上腺素、异丙肾上腺素和脱氧肾上腺素对映体,麻黄碱和伪麻黄碱,硝基酚同分异构体,双酚A类似物的开管毛细管电色谱新方法[11]。
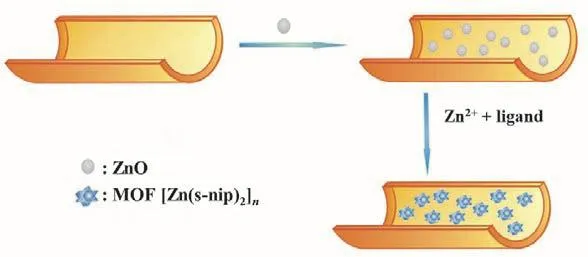
图4 以ZnO为成核试剂制备手性MOF [Zn(s-nip)2]n涂层毛细管的过程[11]
众所周知,通常都是在不断搅拌下把沉淀剂缓慢加入溶液获得沉淀,但这样操作难以避免在沉淀剂加入瞬间出现的局部过浓现象。为解决这一问题,人们发展了均匀沉淀法以获得完整的晶体沉淀。在讲授过程中,我们要求学生思考能否将这种方法用于制备纳米材料。学生通过查阅文献发现,以硝酸锌为原料、尿素为沉淀剂,基于反应温度超过70 °C时尿素不断发生水解产生的氨均匀分布于溶液中使得OH-浓度逐渐增大的现象,实现了在整个溶液中均匀生成氢氧化锌沉淀的目的,而后经过洗涤、干燥、煅烧,即可得到20–80 nm的氧化锌纳米粉体[12]。
4 通过显色剂的讲授培养本科生的创新思维和创新能力
吸光光度法是分析化学经典内容之一。事实上,吸光光度法的发展和应用主要取决于新型显色剂的发展。众所周知,近十多年来,纳米材料和纳米科技有了突飞猛进的发展,许多性质优异的纳米材料不断涌现,这些材料可否作为显色剂或显色反应的催化剂用于建立新的灵敏度高、选择性好的吸光光度法呢?基于此,我们在讲授显色反应和显色剂的基础上鼓励学生深入思考这一问题并大胆探索将纳米材料用作显色剂或显色反应的催化剂发展新的吸光光度法。学生经过查阅文献发现,Fe3O4磁性纳米颗粒具有类过氧化物酶的性质,可用于催化过氧化氢(H2O2)与2,2-连氮-双(3-乙基苯并噻-6-磺酸)磷酸氢二铵盐(2,2’-azino-bis (3-ethylbenzo-thiazoline-6-sulfonic acid) diammonium salt,ABTS)之间的氧化还原反应形成有色化合物[13]。利用Fe3O4磁性纳米颗粒这一性质和三聚氰胺(C3H6N6)与H2O2形成包合物C3H6N6·H2O2降低了体系中H2O2的含量,导致生成的氧化态ABTS浓度降低、溶液颜色变浅的现象(图5),建立了一种简单、快捷、准确、无需复杂设备的测定乳制品中微量三聚氰胺的Fe3O4磁性纳米颗粒吸光光度法[14]。
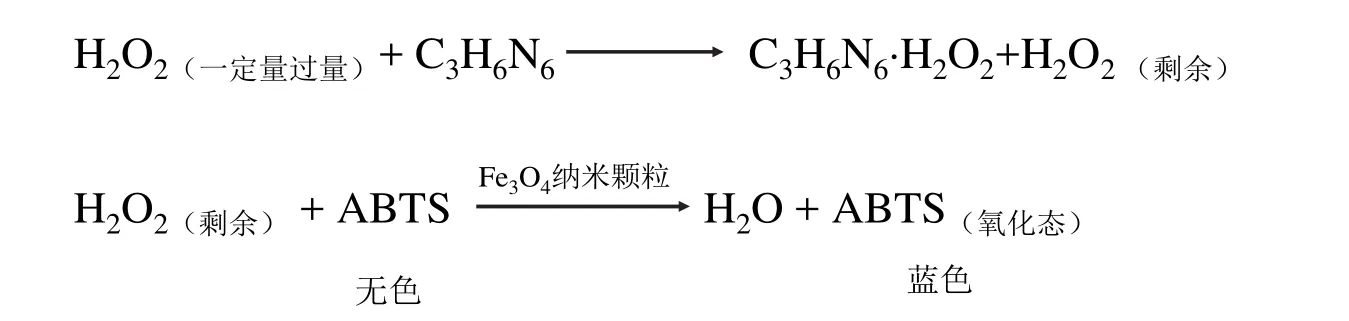
图5 以Fe3O4纳米颗粒为催化剂检测三聚氰胺的原理[14]
在此基础上,我们进一步启发学生思考除了Fe3O4磁性纳米颗粒外其他含有金属的纳米颗粒是否也可能具有类过氧化物酶的性质?学生思考后认为铁酸盐应该具有这种性质。而后通过实验制备了ZnFe2O4磁性纳米颗粒并发现其确实具有类过氧化物模拟酶性质。在此基础上,利用ZnFe2O4磁性纳米颗粒的这种性质建立了一种可视化检测葡萄糖的新方法并将其成功用于糖尿病患者尿液中葡萄糖的测定[15](图6)。进一步制备了MgFe2O4、NiFe2O4、CuFe2O4三种铁酸盐磁性纳米颗粒并研究了其过氧化物模拟酶的性质,并基于NiFe2O4磁性纳米颗粒的类过氧化物酶的性质建立了可视化测定尿液中葡萄糖的吸光光度新方法[16]。

图6 以ZnFe2O4纳米颗粒为催化剂检测葡萄糖的原理[15]
长期的教学实践表明,这种讲授方式深受学生欢迎,大家普遍反映这种讲授方式不仅能使他们深刻地掌握并理解分析化学的经典内容和内涵,而且能强烈地激发他们的创新欲望和创新思维,对培养他们的创新能力起到了显著的作用。学生还特别指出,这种讲授方式使他们了解并初步掌握了开展创新性科学研究特别是分析化学创新性研究的选题、方案制定和实施、论文撰写的方法和技能,为他们成功申请并高质量完成各类研究项目、取得具有一定创新性的研究结果奠定了坚实的基础。
5 结语
从上述实例可以看出,分析化学经典内容不仅是分析化学的核心内容,而且是激发本科生创新思维、培养本科生创新能力的源泉。因此,在讲授分析化学时,不能机械地、静态地介绍这些内容,而应引导学生认真思考、发现与它们相关的分析化学的新理论、新方法、新技术和新应用,积极探究它们所包含的科学内容和创新思想,以此激发学生的创新思维,培养他们的创新能力,为他们今后进行创新性科学研究奠定坚实的基础。

