体外受精-胚胎移植治疗过程中导致异常受精的相关因素分析
曾伟荣 蔡桂丰 熊永崂 阮永铭 赵琴
体外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET) 和卵胞浆内单精子注射(intracytoplasmic sperm injection,ICSI)的过程中,大多数生殖中心都是在授精18~20 h 内通过光学显微镜对胚胎的原核数目进行观察及评分,对明确观察到2 PN 作为正常受精的判断标准,从中选择优质的胚胎进行移植。0、1、3 PN 通常被视为异常受精胚胎,与发育停滞的2 PN 胚胎一同作为废弃胚胎被销毁,目前此方法被广大生殖中心所采用,其中一部分患者因受精异常等原因导致没有正常受精的胚胎而放弃移植。分析导致异常受精的相关因素,提高卵子的利用率,是目前胚胎学家和临床医师急需攻克的难题。
1 资料与方法
1.1 一般资料 选取2020 年1~12 月珠海市妇幼保健院生殖中心接受治疗的1426例IVF 周期不孕症患者作为IVF 组,449例ICSI 周期不孕症患者作为ICSI 组。纳入标准:IVF/ICSI 受精后0、1、2 和≥3 PN 来源胚胎病例。排除标准:①排除受精失败后进行卵母细胞补救的卵胞浆内单精子注射(LICSI)的胚胎;②排除部分卵胞浆内单精子显微注射(HALF-ICSI)的授精方式;③短时受精联合早期补救ICSI。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
表1 两组患者一般资料比较()

表1 两组患者一般资料比较()
注:两组比较,P>0.05;E2 :雌二醇;FSH:卵泡刺激素;LH:促黄体生成素;PRL:催乳素;T:睾酮;P:孕酮
1.2 方法
1.2.1 控制性超排卵方案 超排卵方案采用黄体期长方案,长效促性腺激素释放激素激动剂(GnRH-a)降调节,14~20 d 后给予FSH 进行超排卵治疗,卵泡最大直径≥18 mm 时注射人绒毛膜促性腺激素(HCG),36~38 h后在超声指导下取卵,授精后18~20 h 观察受精情况。
1.2.2 PN 观察 PN 的观察通常是在IVF-ET 和ICSI授精后18~20 h 进行,光学显微镜下观察PN 的形态和数量。正常受精卵可观察到2 PN 受精,只有1 个PN 的为1 PN 受精,没有 PN 且发现2 个极体的为0 PN,≥3 个 PN 的则为多 PN 受精。
1.3 观察指标 ①比较IVF 组和ICSI 组胚胎 PN 形成率。②比较IVF 和ICSI 周期中不同年龄段及Gn 用量胚胎 PN 形成率。③比较IVF 和ICSI 周期中不同获卵数胚胎 PN 形成率。计算方式 :IVF 的2 PN 形成率:2 PN 的总和/成熟与未成熟卵子总和;ICSI 的2 PN 形成率:2 PN 的总和/成熟卵子总和;相应授精方式下的0 PN、1 PN 及≥3 PN 胚胎的形成率均采用类似的计算方式。
1.4 统计学方法 采用SPSS22.0 统计学软件进行数据统计分析。计量资料以均数±标准差()表示,采用t 检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 IVF组和ICSI组胚胎 PN形成率比较 IVF组1 PN和≥3 PN 的形成率高于ICSI 组,0 PN 和2 PN 形成率低于于ICSI 组,差异均有统计学意义(P<0.05)。见表2。

表2 IVF 组和ICSI 组胚胎PN 形成率比较[个(%)]
2.2 IVF 和ICSI 周期中不同年龄段及Gn 用量胚胎PN 形成率比较 IVF 受精后,随着年龄的增加,Gn 用量随着加大,0 PN 形成率呈递增趋势,但各年龄段PN形成率比较差异均无统计学意义(P>0.05)。ICSI 受精后,30~35 岁的成熟卵(MII)卵子总数最多,≥3 PN 形成率最高,随着年龄的增加,Gn 用量随着加大,2 PN 形成率逐渐降低,但1 PN、2 PN 及≥3 PN 的形成率比较差异无统计学意义(P>0.05),而>35 岁的0 PN 形成率高于<30 岁和30~35 岁,差异有统计学意义(P<0.05)。见表3。
表3 IVF 和ICSI 周期中不同年龄段及Gn 用量胚胎PN 形成率比较[,个(%)]
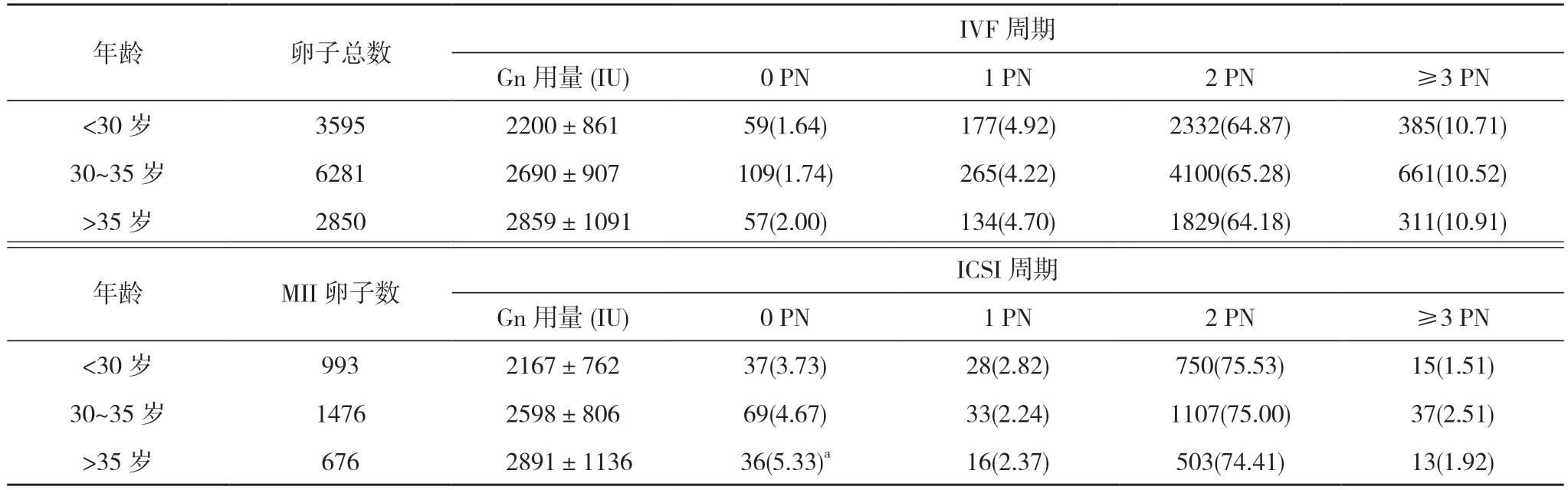
表3 IVF 和ICSI 周期中不同年龄段及Gn 用量胚胎PN 形成率比较[,个(%)]
注:与<30 岁和30~35 岁比较,aP<0.05
2.3 IVF 和ICSI 周期中不同获卵数胚胎PN 形成率比较 IVF 受精后,>15 个获卵数的各PN 形成率最高,其中1 PN 及2 PN 的形成率高于1~5 个和6~15 个获卵数,差异有统计学意义(P<0.05)。ICSI 受精后,1~5 个获卵数的0 PN 形成率高于6~15 个和>15 个获卵数,1 PN 形成率低于6~15 个和>15 个获卵数,差异均有统计学意义(P<0.05)。见表4。

表4 IVF 和ICSI 周期中不同获卵数胚胎PN 形成率比较[个(%)]
3 讨论
在人类辅助生殖技术(ART)进行IVF-ET 和ICSI的治疗过程中,受精 PN 需要在3~20 h 后才能观察到,大部分在受精后18~20 h 出现,观察到2 PN 则认为是正常受精,是移植或冷冻胚胎的首选,其中一部分患者因异常受精而没有正常受精的胚胎而放弃移植,对患者的经济和心理均造成巨大的影响[1]。研究异常受精形成的因素,提高卵子利用率,避免胚胎的浪费,是目前胚胎学家和临床医师急需攻克的难题[2]。
异常受精包括0 PN、1 PN 和多 PN[3]。在IVFET 过程中,0 PN、1 PN 胚胎[3-5]的产生机制主要有:孤雌激活、雌雄原核形成不同步、雌雄原核融合和成熟前原核核膜崩解、精子染色体解聚异常、受精提前或延迟而错过最佳观察时间、受精缺陷和第二极体未排出等[4,5]。多 PN 胚胎[6]的产生机制主要有:第二极体不能正常排出、错误观察、调控卵巢刺激时激素水平的异常、卵子募集过程中的透明带损伤、卵泡液的激素水平、纺锤体微管的缺陷等因素有关。
本文数据可看出,与正常的2 PN 胚胎相比,异常受精胚胎的形成与患者的年龄、选择的受精方式、Gn用量以及获卵数有关。与患者不孕年限、体质量指数和基础内分泌水平无关。在授精方式[7]方面,ICSI 周期的0 PN 形成率明显高于IVF 周期,这可能是ICSI 的注射时间和观察时间所导致的,国外学者发现,ICSI 注射后有16%胚胎的 PN 在18 h 后就已经消失了[8],也有些卵子的 PN 出现时间会推迟到29 h[9];IVF 周期的1 PN 及≥3 PN 形成率均显著高于ICSI 周期,由于促排过程中卵子的多次募集导致卵子的发育不同步,只有部分卵泡达到成熟卵泡的标准,而IVF 和ICSI 的受精的操作方式不同,导致IVF 的1 PN 和≥3 PN 增加。因此,对高龄、卵巢反应不良、获卵数较少的患者,可以考虑不同的受精方式,降低异常受精胚胎比例,避免卵子的浪费[10-12]。
在患者年龄方面,女方年龄增长0 PN 的形成率均呈递增趋势,可能是由于这部分患者大都为卵巢反应不良患者,随着女方的年龄增长,卵子质量开始下降,使得卵子非整倍体率[13,14]增加,从本文数据也可得知,随着年龄增长,卵巢储备随着低下,为获得较多的卵子,从而Gn 加大剂量[15,16],造成卵子透明带损伤、纺锤体微管的缺陷,卵子质量随之降低导致异常受精率的增加。在获卵数[17,18]方面,获卵数>15 个的1 PN和≥3 PN 形成率均高于1~5 个和6~15 个获卵数,可能是由于卵母细胞发育不同步的现象,获卵数的增加使得部分卵泡发育相对滞后或者过熟增加,而优势卵泡的百分率降低,导致异常受精率的增加。
综上所述,女方年龄、授精方式、Gn 用量及获卵数对异常受精的形成有一定的预测作用。在行辅助生殖技术过程中应综合考虑各种影响因素,及时调整临床用药方案,以降低异常受精胚胎的发生率,避免胚胎浪费,为患者提供更安全更合适的治疗方案。

