曲马多复合酒石酸布托啡诺用于二次剖宫产术后静脉自控镇痛的效果
张皓琳,卢 鹏,包晓航,彭 静,吴晓华,方 亮△,李 洪
(陆军军医大学第二附属医院:1.麻醉科;2.妇产科,重庆 400037)
随着我国新的二孩政策的实施,越来越多的产妇需要接受二次剖宫产,甚至多次剖宫产。据报道,接受二次剖宫产的产妇比例从2012年的9.8%增加到2016年的17.7%[1]。若第一次手术引起严重的粘连,不仅会增加二次手术的难度,延长手术时间,还可能会增加患者的疼痛敏感性,造成术后镇痛治疗欠佳[2]。尽管临床上已采取了多种措施控制剖宫产术后疼痛,术后镇痛不足的发生率仍高达20%~40%[3]。为二次剖宫产产妇提供满意的术后镇痛成为挑战。
曲马多是剖宫产术后静脉镇痛有效且耐受性良好的药物,与强效阿片类药物相比,不良反应较少[4]。研究表明,曲马多不仅可以减少二次剖宫产患者早期抑郁和焦虑感,同时可增强患者的动员能力并缩短住院时间[5];但曲马多可能存在镇痛不全,尤其对内脏痛的抑制不明显,且伴有较严重的胃肠道反应[6]。酒石酸布托啡诺是一种阿片受体激动拮抗剂,主要通过激活κ阿片受体参与脊髓镇痛和镇静作用。由于布托啡诺对κ受体的亲和力高于μ受体,使其具有较少强阿片受体激动剂的不良反应。研究已经证实,酒石酸布托啡诺用于产妇外周静脉给药是安全的,其镇痛作用持久,尤其对内脏痛抑制作用明显[6-8]。本研究旨在探讨曲马多联合酒石酸布托菲诺静脉自控镇痛(patient controlled intravenous analgesia,PCIA)对改善二次剖宫产术后早期疼痛的作用。
1 资料与方法
1.1 一般资料
选取本院妇产科2019年1—7月择期行二次剖宫产术的孕妇180例,平均年龄(31.8±3.8)岁,平均孕周(38.2±0.9)周。纳入标准:(1)单胎孕龄37~40周;(2)美国麻醉医师协会(ASA)麻醉分级Ⅰ~Ⅱ级;(3)第一次剖宫产为简单横切口;(4)产妇自愿要求术后PCIA。排除标准:(1)存在严重产科合并症者;(2)有疼痛史、慢性阿片类药物使用或药物滥用(依赖)者;(3)严重肝肾功能异常、心肺功能异常者;(4)存在椎管内麻醉绝对或相对禁忌证者;(5)患有精神病或无法沟通者;(6)拒绝参加者;(7)术中麻醉方式改变者。根据是否使用酒石酸布托啡诺及其剂量的不同将所有患者分为3组:B1组(n=60)、B2组(n=60)、T组(n=60)。本院医学伦理委员会审核并通过了本试验的研究方案(医院伦理编号:2017-研第026-01),本研究的所有受试者均签署书面知情同意书。
1.2 方法
患者入室后,常规心电监护,建立静脉通道,为防止患者术中及术后恶心呕吐,麻醉操作前均给予甲氧氯普胺10 mg和地塞米松10 mg。所有患者左侧卧位于第3~4腰椎(L3~4)间隙行蛛网膜下腔穿刺(0.5 mm×113 mm穿刺针,河南驼人医疗设备集团有限公司),回抽脑脊液通畅或脑脊液流出后缓慢注射1%盐酸罗哌卡因20 mg(批号:H20020250,瑞典阿斯利康),控制麻醉平面于T6以下,术中记录手术时间、术中失血量、生命体征。手术均由经验丰富的同一外科团队进行。手术结束后,患者在麻醉后监护病房观察6 h后转入产科病房,在产科病房中每天常规给予缩宫素20 U+500 mL生理盐水静脉滴注,由产科医生根据病情决定停止给药时间。手术结束后立即连接静脉自控镇痛泵(国械注准0153540995,北京科联升华医疗科技有限公司)。B1组镇痛配方:酒石酸布托啡诺1 mg+曲马多800 mg+生理盐水183 mL;B2组镇痛配方:酒石酸布托啡诺2 mg+曲马多800 mg+生理盐水182 mL;T组镇痛药物:曲马多800 mg+生理盐水184 mL。镇痛泵流速4 mL/h, 单次PCIA剂量1 mL,锁定时间15 min。补救措施:当患者术后疼痛视觉模拟评分法(VAS)评分大于4分,由不知分组的病房医生给予曲马多50 mg进行补救镇痛。
1.3 观察指标
观察术后即刻、术后6、12、24、48 h切口疼痛、宫缩痛、Ramasy镇静评分,以及平均动脉压(MAP)、心率(HR)、呼吸频率;24 h镇痛泵消耗量、患者术后镇痛治疗满意度、首次下床活动时间、患者感到疼痛的时间、住院时间及术后不良反应(恶心呕吐、镇痛不良、瘙痒、头痛、腰痛、过度镇静等)发生情况。
1.3.1疼痛评分标准
采用VAS量表:0分为无痛;1~3分为轻度疼痛;4~6分为中度疼痛;7~10分为重度疼痛。其中,切口疼痛是患者由平卧位起身时描述的疼痛;宫缩痛是由子宫收缩所引起的,表现为阵发性的内脏痛。VAS评分大于或等于4分判为镇痛不良。
1.3.2Ramasy镇静评分标准
1分:患者焦虑和(或)易激惹;2分:患者合作、有定向力、安静;3分:患者只对命令有反应;4分:患者对按压眉间及大声呼喊等刺激有快速而敏捷反应;5分:患者对按压眉间及大声呼喊等刺激反应迟钝;6分:患者对任何刺激都无反应。
1.3.3患者术后镇痛治疗满意度
患者对术后镇痛治疗满意度进行评价,包含不满意、一般满意、满意、非常满意。满意度=(满意+非常满意)/患者总例数×100%[9]。
1.4 统计学处理
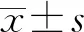
2 结 果
2.1 3组患者一般情况比较
3组患者年龄、身高、体重、体重指数(BMI)、孕周、术前MAP、术前HR、术前血氧饱和度(SPO2)、术前呼吸频率、手术时间、出血量比较,差异均无统计学意义(P>0.05),见表1。

表1 3组患者一般情况比较
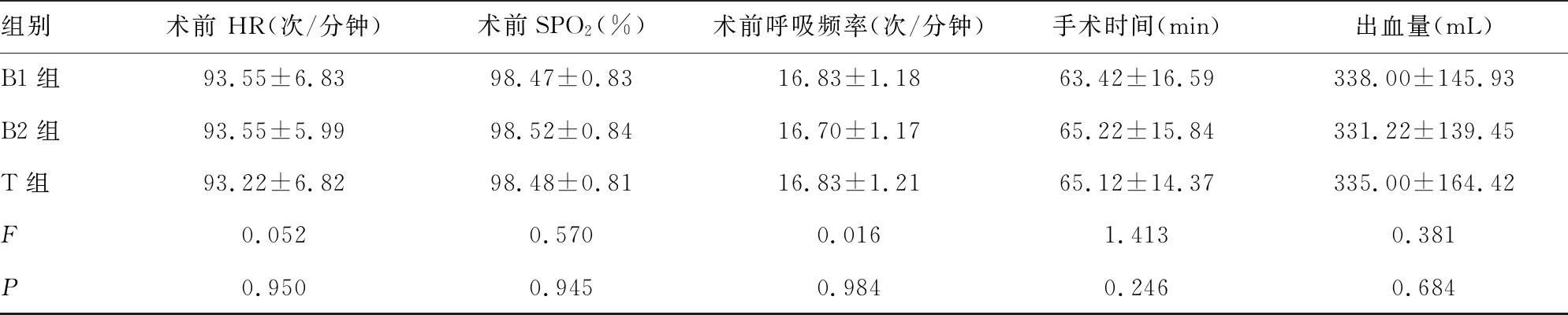
组别术前HR(次/分钟)术前SPO2(%)术前呼吸频率(次/分钟)手术时间(min)出血量(mL)B1组93.55±6.8398.47±0.8316.83±1.1863.42±16.59338.00±145.93B2组93.55±5.9998.52±0.8416.70±1.1765.22±15.84331.22±139.45T组93.22±6.8298.48±0.8116.83±1.2165.12±14.37335.00±164.42F0.0520.5700.0161.4130.381P0.9500.9450.9840.2460.684
2.2 3组患者镇痛效果比较
2.2.1静息切口疼痛
术后即刻、术后6、48 h,3组切口静息疼痛VAS评分比较,差异无统计学意义(P>0.05);术后12 h,B2组切口静息疼痛VAS评分明显低于B1组(P<0.001)和T组(P<0.001),且B1组明显低于T组(P=0.013);术后24 h,B2组切口静息疼痛VAS评分明显低于B1组(P<0.05)和T组(P<0.05),且B1组明显低于T组(P<0.05),见图1。
2.2.2运动切口疼痛
术后即刻,3组切口运动疼痛VAS评分比较,差异无统计学意义(P>0.05);术后6、12、24 h,B1组、B2组切口运动疼痛VAS评分均明显低于T组(P<0.05),且B2组明显低于B1组(P<0.05),见图1。
2.2.3宫缩痛
术后即刻,与T组相比,B1组、B2组宫缩痛VAS评分明显降低(P<0.01);但B1组与B2组比较,差异无统计学意义(P>0.05)。术后6、12 h,B1组、B2组宫缩痛VAS评分均明显低于T组(P<0.01),且B2组明显低于B1组(P<0.05)。术后24 h,B2组宫缩痛VAS评分明显低于T组(P<0.05),B2组宫缩痛VAS评分虽然低于B1组,但差异无统计学意义(P>0.05)。术后48 h,3组宫缩痛VAS评分比较,差异无统计学意义(P=0.138),见图1。
2.3 3组患者住院期间术后结局比较
B2组术后24 h PCIA消耗量明显少于B1组(P<0.001)和T组(P<0.001),且B1组明显少于T组(P<0.05);B2组患者术后镇痛治疗满意度明显高于B1组(P<0.001)和T组(P<0.001),B1组患者术后镇痛治疗满意度高于T组,但差异无统计学意义(P>0.05);3组住院时间比较,差异有统计学意义(P<0.05),与T组比较,B1、B2组住院时间均缩短,且B2组与T组比较,差异有统计学意义(P=0.002),B1组与B2组无明显差异(P>0.05);3组患者感到疼痛时间、额外镇痛需求、首次下床活动时间、术后恶心呕吐及麻醉相关并发症发生情况比较,差异均无统计学意义(P>0.05),见表2。3组患者均未出现过度镇静或躁动、呼吸抑制、瘙痒等术中及术后并发症。利用重复测量方差分析,3组患者不同时间Ramsay镇静评分评分比较,差异有统计学意义(F时间效应=90.97,P时间效应<0.001;F组间效应=5.82,P组间效应=0.004;F交叉效应=2.28,P交叉效应=0.036),Ramsay镇静评分随时间的变化具有明显差异;B2组Ramsay镇静评分在术后即刻、术后6、12 h均优于B1组和T组(P<0.05),B1组和T组无明显差异(P>0.05);3组患者不同时间MAP、HR、呼吸频率比较,差异无统计学意义(P>0.05),见图2。
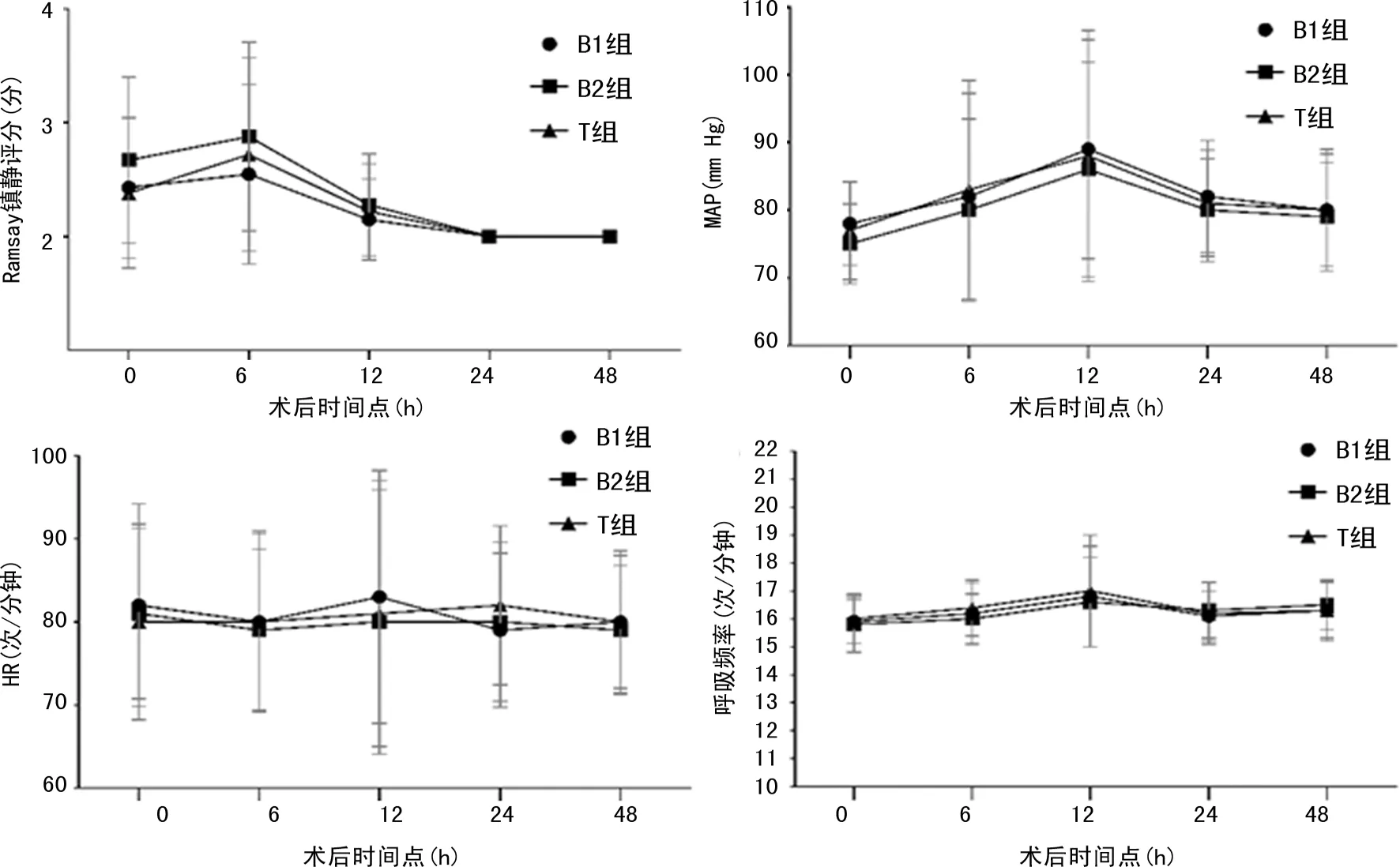
图2 3组患者术后生命体征随时间变化的趋势
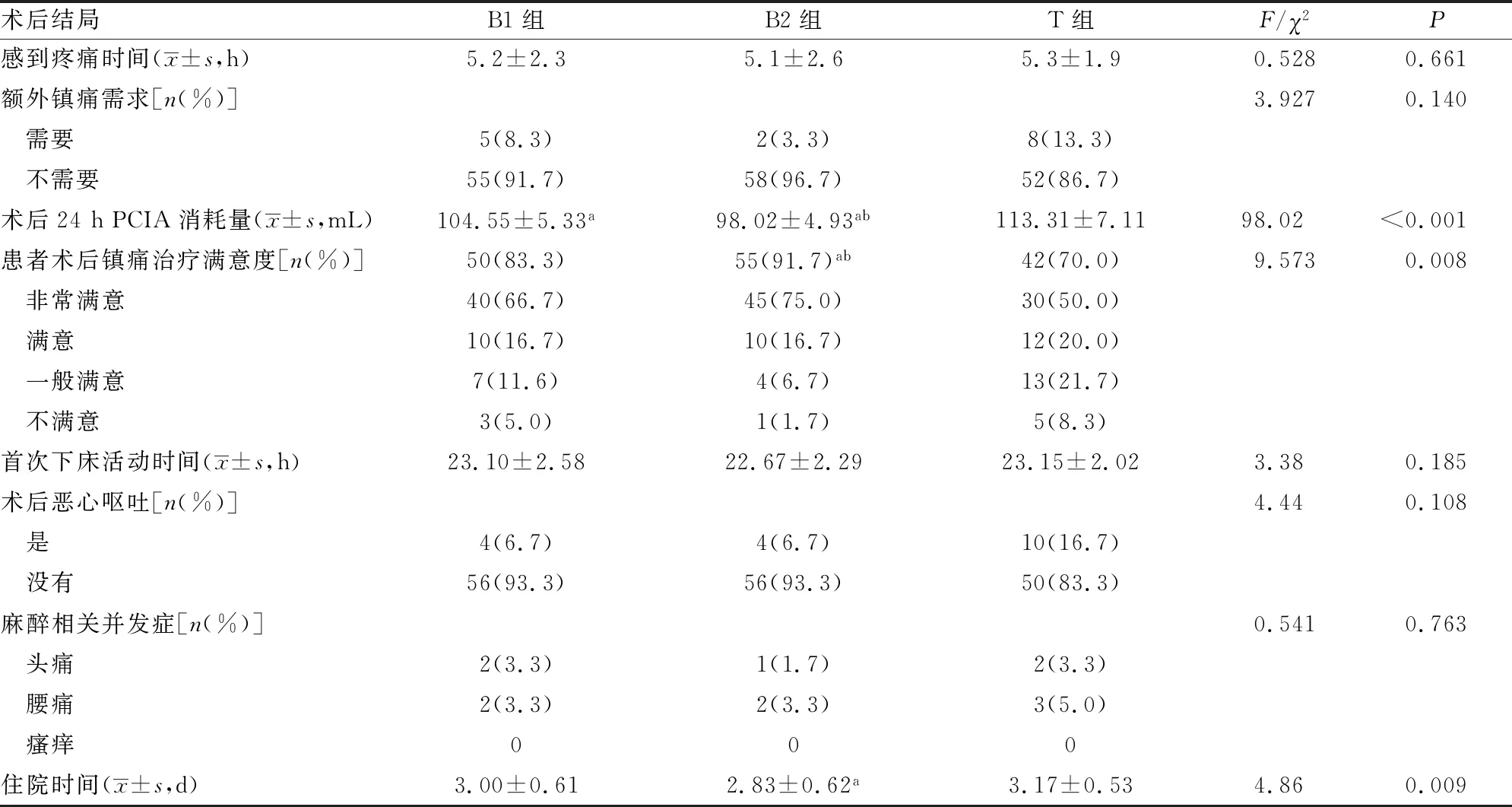
表2 3组患者住院期间术后结局比较(n=60)

a:P<0.05,与T组比较;b:P<0.05,与B1组比较。
3 讨 论
一项配对队列研究发现,与接受初次剖宫产的产妇相比,二次及以上剖宫产产妇镇痛不充分的发生率明显升高,且需要更多的额外镇痛[10]。其原因可能与下列因素有关:(1)手术史可能会增加患者的疼痛敏感性[11],且手术史已被证实为术后疼痛治疗不足的一个危险因素[12];(2)手术史引起的严重粘连通常不可避免,增加了手术难度[2];(3)二次及以上剖宫产产妇的手术时间及手术难度明显增加。YANG等[10]认为,接受二次及以上剖宫产的产妇比首次接受剖宫产产妇可能遭受更多的术后疼痛。另外,宫缩痛是一种位于机体深部,由子宫收缩引起的定位不准确的内脏痛,表现为阵发性的牵拉痛、绞痛等。胎儿娩出后给予缩宫素类药物可促进子宫的阵发性收缩,加强子宫复旧,减少产后出血,尤其术后椎管内麻醉作用消失后缩宫素类药物加剧子宫收缩,增加宫缩痛。KAINU等[13]认为,即使增加硬膜外局部麻醉药用量也达不到抑制宫缩痛的神经控制水平。另有研究证明,激活的外周κ阿片受体能有效缓解内脏痛[14],而κ受体是一种G蛋白耦联受体,可参与腺苷酸(cAMP)的信号转导通路和耦合N型电压依赖性钙通道(VDCC)[15]。酒石酸布托啡诺通过激活κ受体,下调脊髓背角cAMP依赖的蛋白激酶A(PKA)表达,抑制cAMP-PKA-环磷腺苷效应元件结合蛋白信号转导通路,从而缓解宫缩痛;同时,激活的κ受体阻断分布于脊髓背角神经元突触末梢上的N型VDCC开放,减少神经递质及疼痛通路中疼痛介质释放,从而产生强效镇痛作用[16]。
本研究发现,曲马多复合酒石酸布托啡诺PCIA可以有效改善二次剖宫产患者早期术后疼痛,尤其缓解了二次剖宫产患者术后宫缩痛,且宫缩痛缓解程度可能存在酒石酸布托菲诺的剂量依赖效应。酒石酸布托啡诺是阿片受体激动拮抗药,对κ、δ、μ受体的激动强度是25∶7∶1,主要作用于κ受体,部分作用于δ受体,对μ受体有激动拮抗双重作用。在体内无μ受体激动药时,主要表现为剂量依赖性和有封顶效应的κ受体镇痛作用。然而,曲马多为合成的弱阿片受体激动药,具有较弱的μ受体亲和力,因此本研究中酒石酸布托菲诺主要作用于κ表现为镇痛作用,尤其在缓解内脏痛方面表现出了一定的优势。另外,曲马多复合酒石酸布托啡诺的术后镇痛方式缩短了患者住院时间,提高了患者术后镇痛治疗的满意度,同时也促进患者术后早期恢复。作者认为,患者术后早期恢复不仅跟药物的选择有关,而且也与药物的剂量有关。曲马多PCIA用于产妇剖宫产术后镇痛的安全性已被证实,其对新生儿的影响较小[17],其镇痛作用随剂量的增加而增强,其不良反应也随剂量增加而增多。DEMIREL等[18]发现,曲马多PCIA组(840 mg/48 h)对于剖宫产术后疼痛的镇痛效果较好,1 500 mg/48 h的PCIA剂量可提高镇痛效果,但恶心及头晕发生比例很高。因此,本研究选用800 mg曲马多降低胃肠不良反应。
本研究发现,B1组、B2组、T组均能满足二次剖宫产产妇术后镇痛的需求。尽管3组患者术后感到疼痛的时间无明显差异,但单纯接受曲马多术后镇痛治疗的产妇在术后12 h内遭受了更严重的内脏痛,且T组需要额外镇痛治疗患者比例仍高于B1组和B2组,可能与曲马多缓解内脏痛作用不足相关[5]。B2组术后24 h PCIA消耗量明显低于B1组和T组,推测石酸布托菲诺和曲马多之间可能存在协同作用。与氢吗啡酮PCIA相比,曲马多PCIA可以缩短剖宫产患者术后下床活动时间。本研究中3组患者首次下床活动时间无明显差异,这可能与酒石酸布托啡诺的轻度镇静作用有关,虽然术后下床时间无明显差异,但酒石酸布托啡诺的镇静作用有利于术后早期康复[16]。布托啡诺即使椎管内给药仍具有一定的不良反应(眩晕、幻觉、精神错乱、恶心、呕吐等)[19],本研究中无患者出现眩晕、幻觉、精神错乱等不良反应。曲马多严重的胃肠不良反应(恶心、呕吐等)对产妇术后的疼痛管理和情绪影响较大,且曲马多不良反应的发生与使用剂量相关。本研究选用较合适剂量的曲马多(800 mg)并未引起患者发生严重的胃肠反应。分析原因:(1)多模式的镇痛方式减少了药物剂量,从而降低了其不良反应发生率;(2)术前给予甲氧氯普胺和地塞米松减少了恶心、呕吐的发生。
有效的术后镇痛可以改善患者的预后,促进患者早期恢复并缩短住院时间。本研究B2组住院时间短于B1组和T组。此外,曲马多不仅可以降低接受二次剖宫产产妇抑郁和焦虑的发生率,改善产妇的精神状态,还可以促进患者早期恢复并缩短住院时间,而且布托啡诺的轻度镇静可改善产妇术后早期康复。因此,作者认为布托啡诺复合曲马多PCIA二次剖宫产术后镇痛是安全有效的,同时也提高了产妇的就医体验及满意度。
综上所述,酒石酸布托啡诺复合曲马多可以有效改善二次剖宫产术后早期疼痛,尤其缓解了宫缩痛,同时也提高了产妇术后镇痛治疗的满意度,缩短了住院时间。

