白头翁汤通过抑制TLR4-ERK1/2信号通路缓解LPS诱导的微血管内皮细胞炎性反应
贺尚文,王月明,张 慧,侯思鲁,刘晓晔,董 虹*
(1.北京农学院 兽医学(中医药)北京市重点实验室,北京 102206;2. 北京大学,北京 100871)
白头翁汤是《伤寒论》清热解毒类方剂中的代表方剂,具有凉血止痢之效[1]。目前研究表明,白头翁汤具有较好的抗菌抗炎作用[2-3],可通过降低IL-8、ICAM-1水平调节肠道组织炎症以治疗大鼠大肠杆菌性腹泻,并与抗生素治疗相比可明显保护肠道菌群的种类及丰度,在治疗动物细菌性疾病方面具有较好的应用前景[4]。内毒素(LPS)是由革兰阴性菌产生的一种强致病性毒素,可引起机体强烈的炎症反应,导致内毒素血症[5],常被用作刺激因子调控IL-6、IL-1β等相关炎性因子的表达,构建炎症模型[6-7]。LPS-TLR4的信号通路转导途径是目前常见的LPS刺激途径,LPS主要通过Toll样受体4(Toll-like receptor 4, TLR4)识别宿主细胞并激活天然免疫系统[8]。LPS与TLR4结合后TLR4产生构象变化激活下游信号通路,使得下游的肿瘤坏死因子受体相关因子6(TNF receptor associated factor 6, TRAF6)活化,引起 ERK、JNK 和 p38 的 MAPK 信号转导而导致炎性因子的释放,引发病理变化[9]。实验室前期研究表明,白头翁汤具有良好的抗毒素药理作用,可通过抑制炎症反应,降低LPS诱导的大鼠肠黏膜微血管内皮细胞(rat microvascular endothelial cells, RIMVECs)损伤,保护微血管内皮细胞,从而激活跨内皮中性粒细胞(PMNs)溶菌酶,增强PMNs杀菌能力,发挥抗菌作用[10-13]。但其中具体作用机制尚不明确,因此本研究以RIMVECs细胞为模式细胞,利用RT-PCR、Western blot等方法检测白头翁汤对LPS诱导的RIMVECs 的TLR4、TRAF6、P-ERK基因及蛋白表达的影响;以ERK1/2信号通路特异性阻断剂PD98059作用后探究对下游炎性因子的影响,从而研究白头翁汤的抗炎机制,为抗炎中药的开发奠定试验基础,为抗炎策略提供参考。
1 材料与方法
1.1 主要试剂
白头翁(批号:801001104)、黄连(批号:18121402)、黄柏(批号:18052601)、秦皮(批号:180713001)购自北京同仁堂药店,DMEM高糖培养基、D-Hank’s干粉、胎牛血清、双抗、胰蛋白酶均购自GiBco公司,L-谷氨酰胺、二甲基亚砜、LPS、Ⅱ型胶原酶购自Sigma公司,超纯RNA提取试剂盒、cDNA第一链合成试剂盒、UltraSYBR Mixture (WithROX)、DNase1、5×RNA Loading Buffer购自北京康为世纪生物科技有限公司,TRAF-6、TLR4、Erk1+Erk2抗体购自Abcam公司,羊抗兔IgG二抗、BCA蛋白浓度测定试剂盒购自碧云天生物技术公司,大鼠IL-6、IL-8、IL-β、TNF-α ELISA试剂盒购自上海酶联生物科技有限公司,PD98059购自MCE公司。
1.2 主要仪器
奥林巴斯倒置荧光显微镜(日本Olympus公司,型号:IX71),CO2培养箱(日本Sanyo公司,型号:MCO-17AC)PCR仪(美国ABI公司,型号:2720),实时荧光定量PCR系统(德国Roche公司,型号:LightCycler®480II),垂直电泳转印系统(美国Bio-rad | Biorad,型号:PROTEAN Tetra+ Trans-Blot),凝胶成像仪(上海天能,型号:Tanon-5200),多功能酶标仪(美国Bio tek,型号:SYNERGY4)。
1.3 试验材料
原代培养的1~3日龄SD大鼠肠黏膜微血管内皮细胞,经纯化、鉴定、可稳定传代后用于本试验。称取黄连15 g、黄柏10 g、秦皮20 g、白头翁20 g按兽药典[14]中方法制备白头翁汤水煎液,然后浓缩生药浓度至1 g·mL-1,0.22 μm滤膜过滤后置于4 ℃冰箱保存备用[13]。
1.4 细胞的分组与处理
将RIMVECs细胞分为空白对照组、LPS组和白头翁汤组。待细胞长至80%~90%汇合状态时,各组进行如下处理:对照组,加入维持培养基(2% DMEM)作用细胞28 h;LPS组,加入10 μg·mL-1的LPS作用于细胞4 h后使用2% DMEM作用24 h; 白头翁汤组,LPS作用4 h后使用20 μg·mL-1白头翁汤作用细胞24 h。涉及PD98059(ERK1/2抑制剂)处理的细胞分组中,PD98059组使用20 μmol·L-1PD98059预处理细胞2 h后加入10 μg·mL-1的LPS 作用细胞4 h,使用2% DMEM作用细胞24 h,其余各组在上述分组处理基础上使用2% DMEM预处理细胞2 h。
1.5 RT-PCR检测基因转录
使用总RNA提取试剂盒提取RIMVECs细胞总RNA,并反转录为cDNA,反应体系共20 μL,加入1.2 μL Primer mix及总RNA 3 μg(6~7 μL),70 ℃孵育5 min,立即冰浴5 min,随后短暂离心将管壁上的溶液离心至管底。继续向以上反应管中加入以下试剂:4 μL 5×RT Buffer,2 μL 0.1 mol·L-1DTT,0.75 μL 10 mmol·L-1dNTP Each,0.2 μL HiFi-MMLV Enzyme Mix,加H2O 至20 μL。轻轻混匀,42 ℃孵育45 min,85 ℃保温5 min。用荧光定量PCR仪,采用2-△△Ct法进行数据的相对定量分析。取Roche 384孔板,分别编号,按如下反应体系进行: 2×UltraSYBR Mixture 12.5 μL,PCR Forward Primer(10 μmol·L-1)0.5 μL,PCR Reverse Primer(10 μmol·L-1) 0.5 μL,DNA模板 2 μL,加入灭菌蒸馏水至25 μL,程序为95 ℃预变性3 min,40个循环(95 ℃ 12 s,62 ℃ 40 s)。其中根据GenBank中TLR4、TRAF6基因序列,采用Primer Premier 5.0设计1对特异引物(表1),由北京基谱生物科技有限公司合成。根据GenBank中MAPK3基因序列,采用Primer Premier 5.0设计1对 特异引物(表1),由苏州吉玛基因有限公司合成。

表1 GAPDH、TLR4、TRAF6、ERK基因引物
1.6 Western blot
使用RIPA裂解缓冲液提取细胞的总蛋白并按照碧云天BCA蛋白浓度测定试剂盒测定蛋白浓度。根据BCA的结果将每组样品使用裂解液统一至相同浓度后按4∶1的比例加入5×SDS-PAGE上样缓冲液,充分混合均匀后,于100 ℃条件下煮沸8 min, 使蛋白充分变性。按电泳时的上样量合理分装,-80 ℃ 保存。8% SDS-PAGE检测TLR4、TRAF6、P-ERK,使用GAPDH校正,所有蛋白条带灰度值均使用Image J软件进行分析。
1.7 ELISA检测细胞炎性因子
收集各组细胞培养上清液,根据试剂盒说明书要求使用ELISA试剂盒检测IL-6、IL-8、IL-1β、TNF-α含量。
1.8 数据处理与分析

2 结 果
2.1 白头翁汤对LPS作用的RIMVECs中TLR4、TRAF6及ERK基因表达的影响
为了探究白头翁汤是否通过TLR4-ERK1/2信号通路的级联作用产生抗炎效应,检测TLR4、TRAF6及ERKmRNA的转录情况,结果显示,与空白组相比,LPS组TLR4、TRAF6的基因相对表达量显著升高(P<0.01,P<0.001),ERK的基因相对表达量有升高趋势但无显著变化(P>0.05)。与LPS刺激组相比,白头翁汤组TLR4、TRAF6、ERK的基因相对表达量降低,差异显著(P<0.001,P<0.001,P<0.01),结果见图1。

图1 白头翁汤对 LPS 作用的RIMVECs TLR4、TRAF6 及 ERK mRNA表达的影响Fig.1 Effect of Pulsatilla decoction on the relative expression of RIMVECs TLR4, TRAF6 and ERK genes induced by LPS
2.2 白头翁汤对LPS作用的RIMVECs TLR4、TRAF6及P-ERK蛋白表达的影响
白头翁汤能从基因的转录水平较好地抑制RIMVECsTLR4 及TRAF6、ERK的表达,为了进一步探究白头翁汤能否抑制到蛋白表达,采用 Western blot 法从蛋白水平研究白头翁汤的抗炎作用机制。图2、3结果表明,LPS组和空白对照组相比TLR4、TRAF6、P-ERK的相对表达量升高,差异显著(P<0.01,P<0.05,P<0.001),白头翁汤组和LPS组相比,TLR4、TRAF6、P-ERK的相对表达量降低,差异显著(P<0.05,P<0.05,P<0.01)。
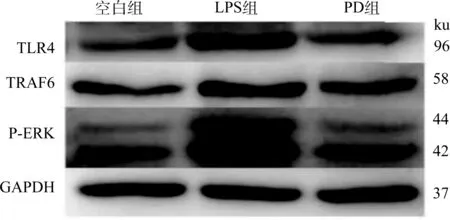
图2 白头翁汤对 LPS 作用的RIMVECs TLR4、TRAF6、P-ERK 蛋白表达的影响Fig.2 Effect of Pulsatilla decoction on the expression of TLR4, TRAF6 and P-ERK protein in RIMVECs stimulated by LPS

A. TLR4 灰度值分析;B. TRAF6 灰度值分析;C. P-ERK 灰度值分析A. Gray value analysis of TLR4; B. Gray value analysis of TRAF6; C. Gray value analysis of P-ERK图3 TLR4、TRAF6、P-ERK 相对表达量灰度值分析Fig.3 Gray value analysis of relative expression of TLR4, TRAF6 and P-ERK
2.3 白头翁汤对LPS诱导的RIMVECs P-ERK表达的影响
由图4、5可知,与空白对照组相比,LPS组P-ERK 水平显著增高(P<0.01),白头翁汤组显著降低了LPS所诱导的RIMVECs P-ERK水平(P<0.05),与上述结果一致。抑制剂组与LPS组相比,P-ERK的蛋白表达量显著降低(P<0.05),并且白头翁汤组与抑制剂组相比作用效果无显著差异。

图4 P-ERK 蛋白表达情况Fig.4 Expression of P-ERK

图5 P-ERK 相对表达量灰度值分析Fig.5 Gray value analysis of relative expression of P-ERK
2.4 白头翁汤对LPS处理的RIMVECs IL-6、IL-8、IL-1β、TNF-α表达的影响
由图6可知,与空白对照组相比,LPS作用后,RIMVECs 的IL-6、IL-8、IL-1β、TNF-α表达显著升高(P<0.01,P<0.01,P<0.05,P<0.01),而与LPS组相比,白头翁汤组IL-6、IL-8、IL-1β、TNF-α表达显著降低(P<0.05,P<0.001,P<0.05,P<0.05)。同时抑制剂组与LPS组相比其下游炎性因子IL-6、IL-8、IL-1β、TNF-α的分泌显著降低(P<0.05,P<0.001,P<0.05,P<0.01)。白头翁汤组与抑制剂组相比其下游炎性因子IL-6、IL-8、IL-1β、TNF-α的分泌无显著性差异。
3 讨 论
微血管内皮细胞(MVECs)是机体重要的保护屏障,其在维持机体内环境稳态、抗炎等方面都具有重要作用[15]。MVECs在细菌病的发生过程中有着十分重要的作用,是多种细菌毒素的靶标[16-17]。致病因子会首先识别MVECs膜上的特异性受体并与之结合来破坏MVECs的屏障作用[18],进而引发炎症反应[19]。其中,LPS是细菌所产生的重要毒力因子,在细菌性疾病发生过程中起重要作用,研究表明,其主要通过损伤MVECs发挥致病作用[20]。尤青海等[21]研究发现LPS可通过PI3K/Akt信号通路诱导RACK1及rac1表达造成大鼠肺微血管内皮细胞损伤导致弥漫性肺间质及肺泡水肿。在研究Apelin-13对LPS诱导大鼠肺微血管内皮细胞炎性因子表达的影响时发现,LPS还可通过干预 ROS-NF-κB 信号通路诱导炎性因子的表达并最终损害内皮细胞功能[22]。在脑微血管内皮细胞中,秦劭晨等[23]发现,LPS处理可升高脑微血管内皮细胞 TNF-α、CCL20、IL-8 mRNA表达量,诱导炎性因子分泌增加最终导致脑小血管疾病。由此可见保护微血管内皮细胞对于治疗LPS所致的机体损伤具有重要意义。而研究发现中药对 MVECs 具有多种调节作用,包括改变血管的通透性、促进细胞的增殖、减少炎症的分泌等[24-25]。白头翁汤主要成分为皂苷类:白头翁皂苷A、B、B4;生物碱类:小檗碱及药根碱;柠檬苦素类:黄柏内酯;香豆素类:秦皮甲素、秦皮乙素及葡萄糖苷[4]。前期研究表明,其在抑制LPS所致的大鼠肺微血管内皮细胞损伤、治疗肠道炎症方面具有良好的效果。节阳华等[26]研究发现,白头翁汤可通过阻断JAK2/STAT3通路的转导,改善结直肠癌中炎性微环境从而达到抗肿瘤的效果。在溃疡性结肠炎治疗中,白头翁汤可通过调节肠道免疫系统如维持Th17/Treg的平衡、增加miR-19a的表达等,调节NF-κB mRNA的水平、黏附分子水平及影响TGF-β1/Smad3信号通路等途径发挥显著抗炎作用[27]。
因此,本试验以RIMVECs细胞为材料,探究白头翁汤是否通过抑制TLR4-ERK1/2信号通路而发挥抗炎作用。炎症Toll样受体(TLR)4属于TLR受体家族,可诱导对入侵病原体的炎症反应,是参与介导LPS诱导跨膜信号转导和细胞激活的受体,广泛分布于内皮细胞等多种免疫细胞中,在机体免疫过程中具有重要作用[28]。TLR4激活后会引起一系列的下游蛋白的反应,包括引起TRAF6活化、ERK1/2的磷酸化等。ERK1/2是MAPK成员之一,许多文献都表明 ERK1/2 在控制炎症方面发挥重要作用,其持续的激活可引起炎症细胞因子不断产生,和其上游的 MAPKK 及 MAPKKK 共同作用,导致级联“瀑布”效应。严宁等[29]研究发现,抑制ERK1/2信号通路后可缓解心肌缺血再灌注大鼠所出现的炎症损伤。在幽门螺杆菌所致的大鼠肠黏膜炎性反应中,田华等[30]研究发现抑制ERK通路可减轻胃炎大鼠胃黏膜的炎性反应。在非酒精性脂肪肝病中,廖媛等[31]研究发现下调TLR4、ERK1/2基因及蛋白表达,可抑制炎症反应,减轻肝脏炎症。

图6 PD98059 作用后白头翁汤对 LPS 作用的RIMVECs IL-6、IL-8、IL-1β、TNF-α 表达的影响Fig.6 Effects of Pulsatilla decoction on the expression of IL-6, IL-8, IL-1β and TNF-α in RIMVECs induced by LPS after PD98059 treatment
前期实验室研究表明20 μg·mL-1的白头翁汤对细胞无毒性[13]。笔者发现20 μg·mL-1的白头翁汤处理可以显著降低LPS诱导的TLR4、TRAF6、ERK1/2基因及蛋白的表达。随后使用ERK1/2信号通路上的特异性抑制剂PD98059,观察白头翁汤与抑制剂在抑制P-ERK蛋白表达及LPS所诱导的RIMVECs炎性因子IL-6、IL-8、IL-1β、TNF-α分泌情况的作用效果差异。PD98059可通过特异性抑制其上游蛋白激酶MEK从而阻断ERK1/2信号通路的激活[32],其被广泛应用于癌症的研究中[33-34]。抑制剂PD98059抑制了LPS所引起的ERK1/2磷酸化及其下游炎性因子的分泌。表明ERK信号通路是LPS诱导炎性因子分泌,损伤RIMVECs细胞的主要靶点之一。白头翁汤在抑制ERK1/2磷酸化水平上与抑制剂组相当,并可显著降低LPS所诱导的炎性因子IL-6、IL-8、IL-1β、TNF-α含量的高表达,且白头翁汤下调炎性因子表达的效果与ERK1/2抑制剂相似,无统计学差异。这提示EKR1/2可能是白头翁汤抑制炎症反应保护RIMVECs的主要靶点之一。本试验从细胞水平证实了白头翁汤可抑制 LPS 刺激 RIMVECs 所引起的IL-6、IL-8、IL-1β、TNF-α的高表达,并通过 PD98059 阻断试验,初步认为其机制可能与白头翁汤抑制ERK1/2信号通路有关,ERK1/2信号通路可能是白头翁汤作用的主要靶位之一。以上说明,白头翁汤可通过抑制TLR4-ERK1/2 信号通路,降低 LPS所引起的细胞炎性反应,从而达到保护机体的目的。此外由于LPS激活胞内信号转导,可引起多条信号通路间的级联反应,且白头翁汤多成分、多靶点,除了抑制LPS激活ERK1/2通路外,是否还作用于其他胞内通路,都需进一步的试验进行研究探讨。
4 结 论
白头翁汤通过抑制TLR4-ERK1/2 信号通路上TLR4、TRAF6、ERK基因及蛋白的表达抑制LPS所诱导的RIMVECs炎性反应,发挥抗炎作用。

