羊红膻二氯甲烷部位的化学成分研究
郝晶晶,张府君,甄会贤,冯 贞
(1.山西药科职业学院,山西 太原030031;2.山西省食品药品检验所,山西 太原030006)
羊红膻是双子叶植物药伞形科茴芹属植物缺刻叶茴芹的根或全草,为多年生草本植物。别名羊洪膻、六月寒[1]。产地分布在东北、陕西、内蒙古、河北、山西、台湾、广东、山东等地。夏秋季采集,洗净,切段,晒干备用或鲜用。药理研究表明其具有降压、降低心肌耗氧量,增加心、脑、肾血流量,预防外源性甘油三酯升高的作用,并且有显著增强体力的功效[2]。临床观察中也发现羊红膻对治疗慢性气管炎及克山病有良好疗效,并且在心电图上也有一定的改善[3]。本文对羊红膻二氯甲烷部分进行化学成分研究。
1 试剂与器材
1.1 试剂
二氯甲烷(色谱纯,天津市科密欧化学试剂有限公司);硫酸、甲醇、二氯甲烷、石油醚(60-90)、乙酸乙酯、甲酸、冰乙酸、盐酸及氢氧化钠均为AR。
1.2 药材
羊红膻药材的药用部位为全草或根,本实验对羊红膻全草进行研究,采购于陕西省黄安县,经由山西药科职业学院杨红教授鉴定为羊红膻药材。
1.3 材料
AB-8大孔吸附树脂(批号:HG 2-885-76,天津市光复精细化工研究所),80~100目硅胶(青岛海洋化工厂分厂),200~300目硅胶(青岛邦凯高新技术材料有限公司),硅胶G板(30×100 mm,50×100 mm,100×100 mm,青岛海洋化工厂分厂),Sephadex LH-20凝胶(GE Healthcare)。
1.4 仪器设备
分析天平(上海舜宇恒平科学仪器有限公司),旋转蒸发仪(SY-5000,上海亚荣生化仪器厂),循环水式真空泵(SHZ-D(Ⅲ),巩义市予华仪器有限责任公司),层析柱(24 mm×670 mm,10 mm×200 mm,20 mm×350 mm),超声波清洗机(SB-5200 DTDN,宁波新芝生物科技股份有限公司),点样毛细管(0.3 mm,长城科学仪器商店经销)。
2 方法
2.1 馏分的制备
羊红膻药材阴干,粉碎成粗粉,称取药材5 kg,加60%乙醇,浸泡12小时,加热回流提取,浓缩得浸膏1 401 g。分别用石油醚、二氯甲烷、水饱和正丁醇对混悬液依次进行萃取,萃取至无色,回收有机溶剂,得到二氯甲烷部位A 43 g,石油醚部位B 32 g,正丁醇部位C 65 g。A部位用少量二氯甲烷溶解,进行硅胶柱层析,用二氯甲烷、二氯甲烷:甲醇(100∶1、80∶1、50∶1、20∶1、10∶1、5∶1、1∶1)依次梯度洗脱。每500 mL(柱体积1 800 mL)收集一份馏分,流速3~5 mL/min,浓缩之后装到10 mL西林瓶内。
2.2 大孔树脂吸附法100∶1馏分除色素
将50 mm×500 mm层析柱洗净、干燥,垂直固定在铁架台上;AB-8大孔树脂用无水乙醇浸泡约24 h后装柱,用80%乙醇冲至树脂表面平整后,使洗脱剂液面降低至高于树脂表面1~2 cm处;用80%乙醇溶解样品,用滴管缓慢加入,附在柱壁上的使用80%乙醇沿壁缓慢冲洗;待样品吸附2~3 h后,用80%乙醇洗脱,待所接溶液泛绿时停止操作,回收乙醇。
2.3 化合物的分离与精制
用薄层色谱进行跟踪检测,显色剂为10%硫酸-乙醇,显色后根据馏分的斑点情况,合并相近馏分。本实验选择合并馏分100∶1中11~17进行进一步纯化分离。取层析柱(24 mm×670 mm),将硅胶湿法装柱,样品拌样,上样,以二氯甲烷:乙酸乙酯为洗脱剂进行梯度洗脱。通过反复硅胶柱层析、凝胶柱层析分离得到化合物Ⅰ和化合物Ⅱ。
2.4 化合物Ⅰ和化合物Ⅱ的流程图(图1):

图1 羊红膻二氯甲烷部分提取分离纯化流程图
3 结果
3.1 化合物Ⅰ的检识及鉴定
3.1.1 化合物Ⅰ的薄层鉴别 三种展开剂系统下(二氯甲烷∶乙酸乙酯 =1∶1;石油醚∶乙酸乙酯 =1∶1;二氯甲烷∶甲醇=80∶1;显色剂:10%硫酸-乙醇)化合物均为一个黄色斑点。
3.1.2 化合物Ⅰ的鉴定 化合物Ⅰ:无色液体,极易溶于二氯甲烷,微溶于甲醇,10%硫酸-乙醇(95%)显色后呈黄色斑点。1H NMR(600 MHz,CD2Cl2):δ7.16(d,J=8.4 Hz,2H,C2,6-H),6.79(d,J=8.4 Hz,2H,C3,5-H),4.11(d,J=4.9 Hz,1H,C1′-H),3.91(m,1H,C2′-H),3.39(dd,J=9.4,7.1 Hz,2H,C1″-H),1.17(t,J=7.0 Hz,3H,C2″-H),1.08(d,J=6.4 Hz,3H,C3′-H),7.288(宽短峰,Ar-OH),13 C NMR(151 MHz,CD2Cl2)δ156.28(C1),129.48(C2,6),115.58(C3,5),130.96(C4),85.58(C1′),71.28(C2′),64.84(C1″),18.44(C3′),15.52(C2″)经碳谱和氢谱综合分析,并参考文献确定化合物为4-(1′-乙氧基-2′-羟基丙基)苯酚(结构式见图2)[2]。
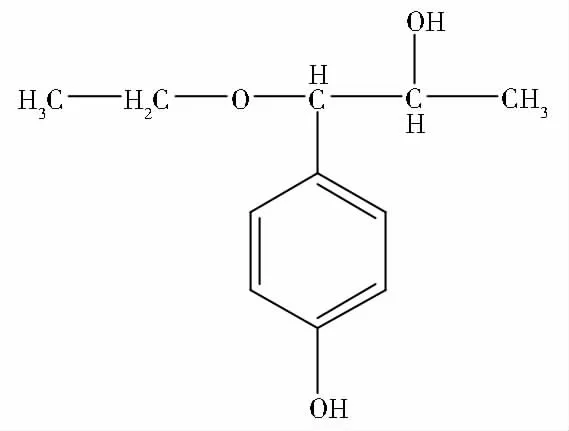
图2 化合物Ⅰ的结构式
3.2 化合物Ⅱ的检识及鉴定
3.2.1 化合物Ⅱ的薄层鉴别 三种不同展开系统下(二氯甲烷∶甲醇 =30∶1;二氯甲烷∶乙酸乙酯 =1∶1;石油醚∶乙酸乙酯=1∶1。显色剂为10%硫酸-乙醇。)化合物均为一个橘黄斑点。
3.2.2 化合物Ⅱ的鉴定 化合物Ⅱ:无色液体,易溶于二氯甲烷,微溶于甲醇,10%硫酸-乙醇(95%乙醇)显色后为橘黄色。1H NMR(600 MHz,CD2Cl2):δ7.37(m,3H),7.05(dd,J=8.6,3.4 Hz,3H),4.63(d,J=4.3 Hz,1H),3.95(dd,J=6.4,4.4 Hz,1H),2.43(d,J=7.1 Hz,1H),1.81(d,J=13.7 Hz,1H),1.62(s,1H),1.27(d,J=7.0 Hz,4H),1.07-0.99(m,11H),13C NMR(151 MHz,CD2Cl2):δ175.66(C1″),150.90(C1),138.78(C2),128.20(C3,5),121.85(C6),77.46(C1′),71.66(C2′),41.58(C2″),26.31(C3″),22.58(Ar-CH3),17.61(C3′),16.74(C4″),11.79(C5″),53.84(CD2CL2)。经过碳谱和氢谱综合分析,并参考文献确定化合物为2-甲基丁酸-4-甲基-2-(1′,2′-二羟基丙基)苯酚酯(化合物结构式见图3)[3]。

图3 化合物Ⅱ的结构式
4 讨论
4.1 葡聚糖凝胶装柱
本实验中化合物溶于二氯甲烷中,凝胶装柱时使用洗脱剂为二氯甲烷,凝胶较二氯甲烷轻,浮于上层,凝胶装柱时若保留洗脱剂高于凝胶面6~7 cm时,总有一部分凝胶浮于上层,需加较厚的一层棉花将其压下,保证凝胶沉降完成。
4.2 薄层鉴别
本次实验中当用展开系统为二氯甲烷∶甲醇=60∶1时,两种化合物斑点颜色及Rf均相同,但换展开系统为二氯甲烷∶乙酸乙酯=1∶1时,两种化合物虽斑点颜色相近,但比移值却相差甚远。
4.3 化合物分子量的测定
在本次实验中,曾使用ESI-HRMS测定两种化合物的精确分子量,但在实验条件下,两种化合物均无响应,说明化合物的极性较小。因此如需测定这两种化合物的分子量需采用APCI-MS进行。

