富马酸贝达喹啉片治疗耐多药肺结核的临床疗效分析
凌慧琪,陈伟杰,何显科
(广西钦州市第二人民医院,钦州 535000)
肺结核为由结核分枝杆菌(mycobacterium tu-berculosis,MTB)感染引起的以干酪样坏死及肉芽组织增生为特征的慢性感染性疾病。我国结核病人数居世界第二[1],由于长期不合理用药、抗生素广泛应用等导致耐药MTB的产生,尤其是耐多药肺结核(multidrug resistance pulmonary tuberculosis,MDRTB)与广泛耐药结核病(extensively drug-resistant tuberculosis,XDR-TB)、广泛耐药结核病前期(pre-XDR-TB),有较强传染性,目前由于抗结核新药的匮乏,MDR-TB/XDR-TB 的治疗时间长、费用高、不良反应多,治疗预后多不理想,增加了肺结核治疗难度[2]。贝达喹啉(bedaquiline)为近50 年来第1 个上市的抗结核新药,其作用机制独特且抗MTB活性强、无交叉耐药性,对敏感菌株与多药耐药菌株有较高抗菌活性[3]。本研究旨在探讨富马酸贝达喹啉片治疗MDR-TB的临床疗效,现将结果报道如下。
1 对象与方法
1.1 研究对象 选取2018 年9 月至2020 年1 月广西钦州市第二人民医院收治的64 例MDR-TB 患者为研究对象。病例纳入标准:(1)符合MDR-TB 诊断标准[4],胸片提示肺结核病变,经MTB培养阳性,药敏试验提示至少同时对异烟肼和利福平耐药;(2)文化程度在小学及以上,且意识清晰、有沟通交流能力。排除标准:(1)对研究药物或其中任何成分有过敏史或无法有效完成治疗方案;(2)入组时合并有严重呼吸衰竭、心功能不全或肝肾功能障碍者;(3)临床上有明显心电图异常(男性QTC间期>430 ms,女性QTC 间期>450 ms);(4)妊娠或哺乳期妇女;(5)临床研究前3个月有参加过其他任何临床试验或艾滋病病毒抗体检测阳性者。将研究对象随机分为观察组和对照组,每组32 例,两组一般资料比较,差异无统计学意义(P>0.05),具有可比性,见表1。本研究获得医院医学伦理委员会批准,所有患者均签署知情同意书。
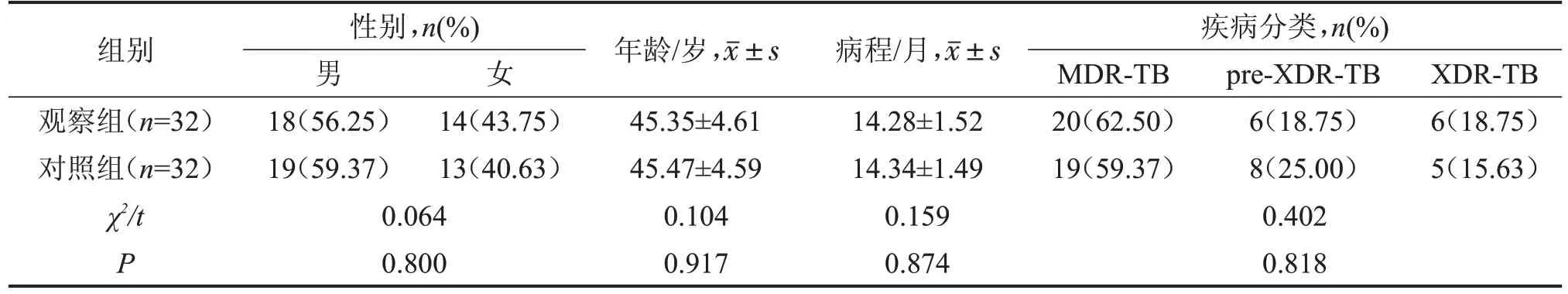
表1 两组一般资料比较
1.2 方法 对照组采用常规MDR-TB 治疗方案:(1)MDR-TB标准化疗方案:吡嗪酰胺片、阿米卡星(卡那霉素、卷曲霉素)、左氧氟沙星(莫西沙星)、对氨基水杨酸(环丝氨酸、乙胺丁醇)、丙硫异烟胺强化治疗24周。(2)pre-XDR-TB/XDR-TB标准化疗方案:吡嗪酰胺、卷曲霉素、莫西沙星、对氨基水杨酸、环丝氨酸(丙硫异烟胺)、克拉霉素、阿莫西林克拉维酸钾强化治疗24周。观察组在对照组基础上,依据抗结核新药贝达喹啉临床应用专家共识[5],严格按照适应证及标准予以富马酸贝达喹啉片治疗方案,第1~2周400 mg/次,1次/d,与食物同服,第3周200 mg/次,3 次/周,与食物同服,2 次用药间隔至少48 h,每周总剂量为600 mg;若在治疗第1~2 周内漏服1 次本品则无需补足漏服药物,应继续正常给药,第3 周若漏服200 mg 剂量,应尽快服用漏服剂量,后继续每周3次的用药方案,连续治疗24周。
1.3 观察指标(1)比较两组治疗24 周累积痰菌阴转率,记录痰菌阴转时间。(2)比较两组治疗6周、12周、24周病灶吸收率、空洞闭合率,依据影像学判定病灶吸收及空洞闭合[6],病灶吸收判定:显吸:病灶吸收≥原病灶50%;吸收:病灶有所吸收,但不足原病灶50%;不变:病灶未见明显吸收变化;恶化:病灶扩大或播散。空洞判断标准:闭合:空洞闭合或消失;缩小:空洞缩小≥原空洞直径50%;不变:空洞缩小,但不足原空洞直径的50%或空洞增大不足原空洞直径的50%;增大:空洞增大至原空洞直径的50%及以上。(3)于两组治疗前、治疗6 周、12 周、24 周取2 mL EDTA 抗凝外周静脉血,经抗体标记后,以FACSCalibur 流式细胞仪测定T 淋巴细胞亚群(CD3+、CD4+、CD8+)变化,并计算CD4+/CD8+。(4)观察两组不良反应。
1.4 统计学方法 采用SPSS 23.0软件进行数据分析,计数资料以百分率(%)表示,组间比较采用χ2检验、连续校正χ2检验或Fisher精确概率法;计量资料以均数±标准差()表示,采用重复测量数据的方差分析,组间比较采用LSD-t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组痰菌阴转情况比较 观察组治疗12 周、24 周痰菌阴转率显著高于对照组(P<0.05);观察组平均痰菌阴转时间明显短于对照组(P<0.05),见表2。
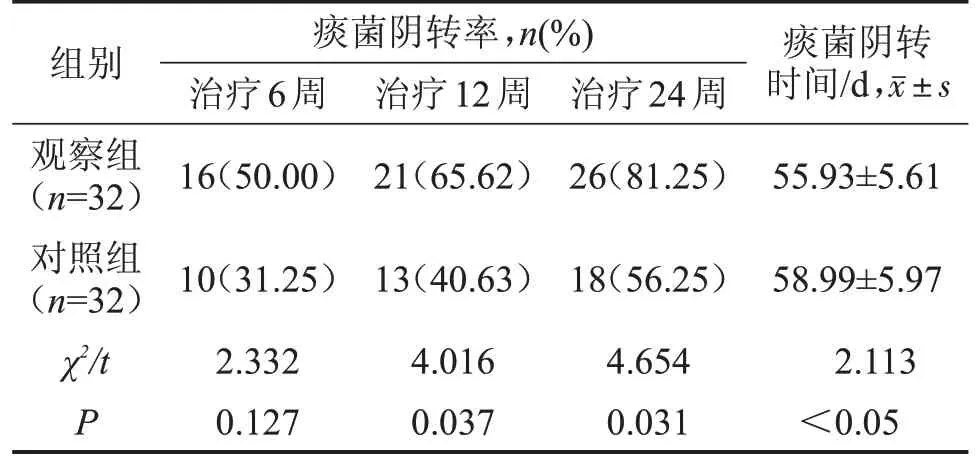
表2 两组痰菌阴转率及阴转时间比较
2.2 两组病灶吸收及空洞闭合情况比较 两组治疗6周、12周病灶显吸率、空洞闭合率比较,差异无统计学意义(P>0.05),而观察组治疗24 周病灶显吸率、空洞闭合率显著高于对照组(P<0.05),见表3。
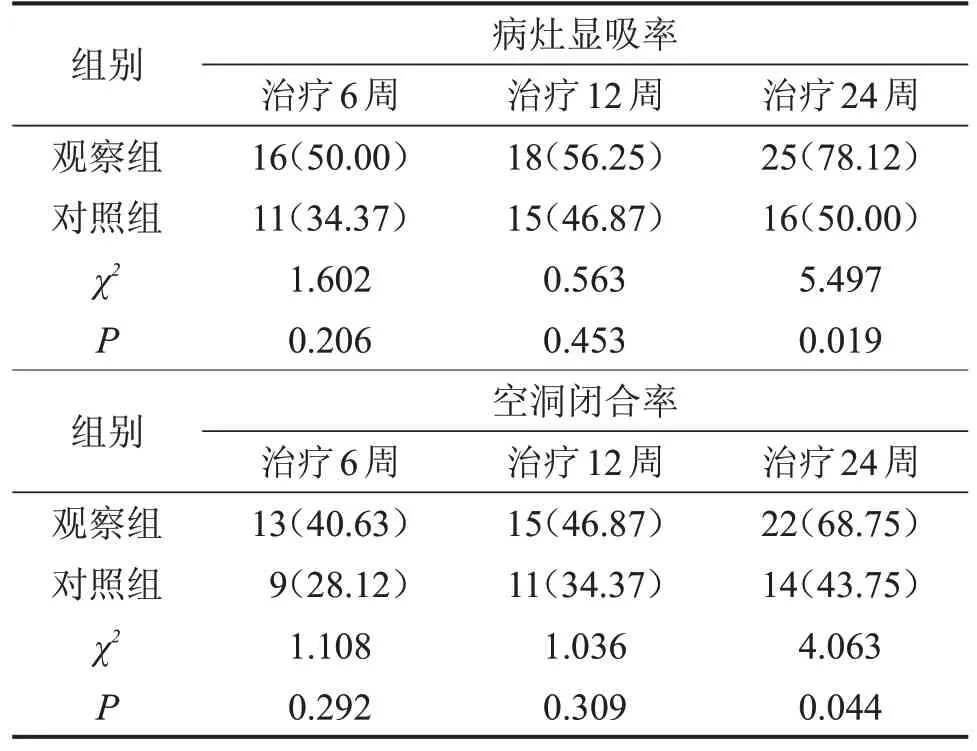
表3 两组病灶吸收及空洞闭合情况比较n(%),n=32
2.3 两组T淋巴细胞亚群变化比较 治疗后两组T淋巴细胞亚群均发生改变,表现为CD3+、CD8+增加,而CD4+、CD4+/CD8+下降,且观察组治疗12 周、24 周CD3+、CD8+明显高于对照组,而CD4+、CD4+/CD8+明显低于对照组(P<0.05),见表4。
表4 两组T淋巴细胞亚群变化比较 ,n=32
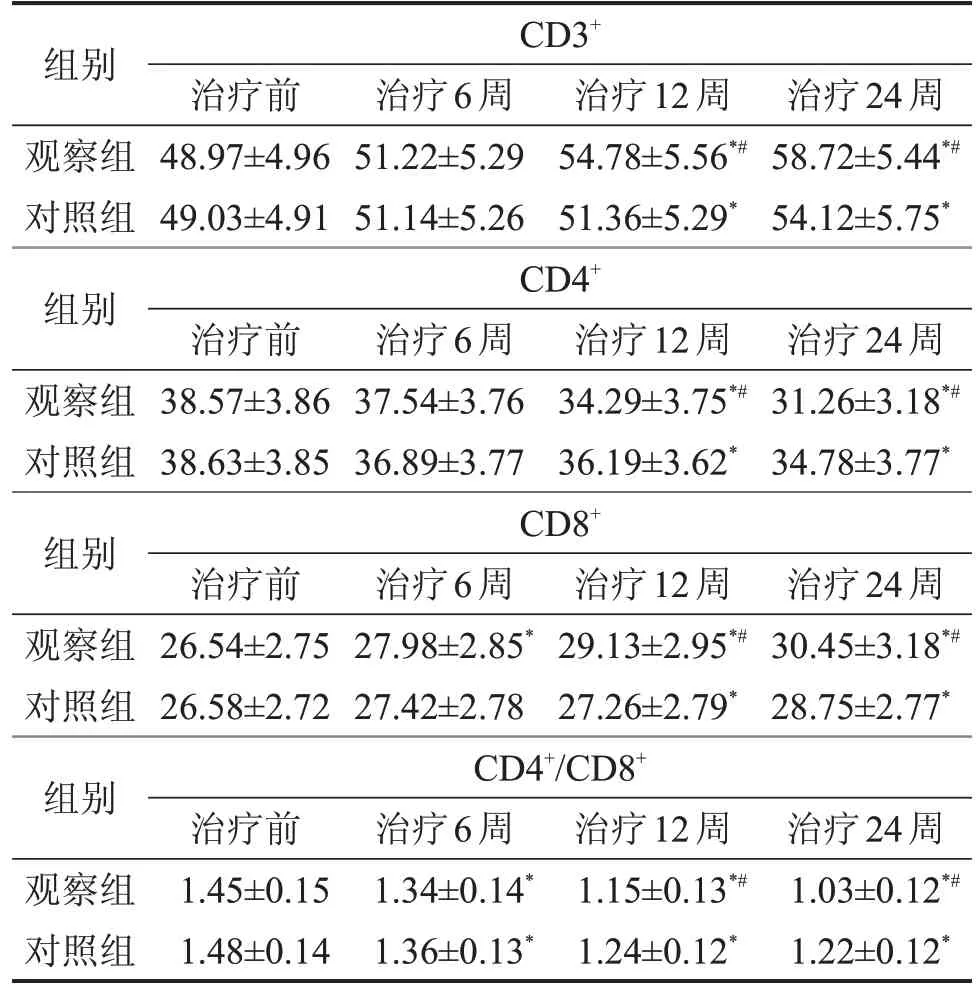
表4 两组T淋巴细胞亚群变化比较 ,n=32
与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
2.4 两组不良反应发生率比较 观察组治疗期间不良反应有QTC 间期延长、肝功能损伤、白细胞减少、咯血、心律失常、恶心呕吐等,不良反应可耐受,仅3 例因QTC 持续延长而停止使用贝达喹啉。观察组QTC 间期延长发生率明显高于对照组(P<0.05),两组其他不良反应发生率比较,差异无统计学意义(P>0.05),见表5。
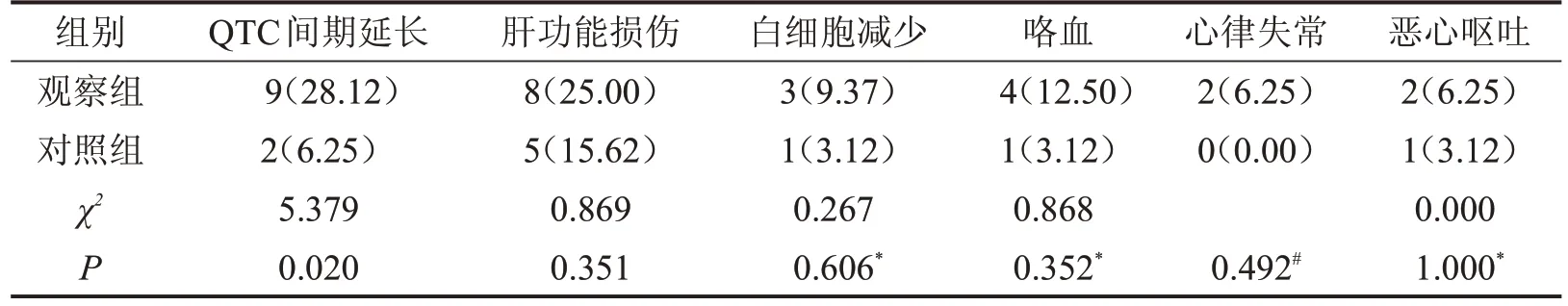
表5 两组不良反应发生率比较n(%),n=32
3 讨论
目前结核病在世界范围内仍是高致死性疾病,约1/3 世界人口存在结核杆菌感染,而其中发病者只占少部分,多数为隐性感染状态[7]。MDR-TB 为肺结核患者感染的MTB至少同时对异烟肼、利福平耐药,MDR-TB 及XDR-TB 的出现,使抗结核治疗难度上升,长期实践表明,MDR-TB 治疗成功率不足50%,而XDR-TB治疗成功率更低。因此,MDRTB/XDR-TB 仍是目前威胁人类健康与致死性极强的公共卫生问题,随着贝达喹啉、德拉马尼或普瑞马尼等新药相继问世,以贝达喹啉加标准化疗方案治疗MDR-TB/XDR-TB取得了惊人治疗成功率,近期日本一项关于贝达喹啉治疗MDR-TB 患者中的安全性、有效性和药代动力学研究表明,贝达喹啉治疗24 周是一种适合日本成人MDR-TB 患者的治疗方法[8]。因此,贝达喹啉在MDR-TB 中有一定应用前景,但关于其疗效与安全性仍需要进一步证实。
早期Pym等[9]的研究发现,贝达喹啉治疗MDRTB 24周痰菌阴转率为79.5%,平均痰菌阴转时间为57 d,治疗结束(120 周)痰菌阴转率为72.2%,其中MDR-TB、pre-XDR-TB、XDR-TB 痰菌阴转率分别为73.1%、70.5%、62.2%。本研究观察组治疗12周、24周痰菌阴转率均明显高于对照组,观察组平均痰菌阴转时间明显短于对照组(P<0.05),与上述研究结果基本相符,表明在常规抗结核药物的基础上加用贝达喹啉治疗24 周,有利于促进痰菌阴转,并缩短痰菌阴转时间。
贝达喹啉为二芳基喹啉类代表药,其可经抑制MTB的三磷酸腺苷(adenosine triphosphate,ATP)合成酶而发挥抗MTB作用,可与ATP合成酶低聚物亚基C相结合,影响ATP合成酶质子泵活性,导致ATP合成受阻,继而阻止MTB 中的ATP 能量供应,发挥抑菌与杀菌作用[10-11]。因此,对于MDR-TB 有较好抗结核效果。牛瑞青等[12]的系统评价也发现,观察组经贝达喹啉用药24 周后,痰菌阴转率高于对照组,基于现有随机对照试验结果发现贝达喹啉联合常规治疗可有效治疗MDR-TB,其效果优于常规治疗。吴桂辉等[13]发现,25例完成24周贝达喹啉治疗的MDR-TB患者在疗程结束后,病灶范围显吸率为40%,吸收率为56%。因此,认为贝达喹啉联合其他二线药物治疗MDR-TB可达到较好病灶吸收率,本研究观察组治疗24 周后病灶显吸率达78.12%,空洞闭合率为68.75%,较上述报道结果略高,可能与患者依从性好、所选病例中MDR-TB 为主、pre-XDR-TB 与XDR-TB 占比不足50%、治疗难度稍小等有关。
机体在感染MTB后,天然免疫应答与特异性免疫应答功能发生改变,而外周血T 淋巴细胞为反映机体细胞免疫状态较好的指标,其中CD3+、CD4+与CD8+T淋巴细胞在人体免疫调节中起着非常重要作用,CD4+/CD8+比值为导致人体免疫功能改变的主要因素,两者比值一定时才可保证相对平衡[14]。宋华峰等[15]的研究发现,与非耐药初治肺结核(DSTB)相比,MDR-TB 患者CD3+、CD8+T 淋巴细胞下降,这给结核病的治疗提供了依据。本研究发现,治疗后两组细胞免疫功能发生一定变化,而观察组改善效果更明显。贝达喹啉可通过抑制MTB 的ATP合酶活性抑制活跃复制及非复制的MTB,低浓度贝达喹啉也能抑制潜伏结核感染的休眠菌,有强大杀菌及灭菌活性,紧密结合在血浆,组织穿透能力强,尤其对MTB 感染的器官穿透力更强,能与血浆及组织长时间结合,半衰期可达5.5个月[16-17]。体外研究也表明,贝达喹啉对MDR-TB临床株有较高抗菌活性,且MDR-TB菌株非北京基因型与贝达喹啉耐药相关[18]。但关于贝达喹啉对MDR-TB患者T淋巴细胞亚群的改善作用具体机制仍需进一步探索。
贝达喹啉连续应用18周为安全及有效的,尚可惠及儿童、青少年、孕妇、艾滋病病毒感染等特殊人群,但不可避免出现原发与获得性耐药、交叉耐药、结核复发、患者QTC间期延长[19]。本研究观察组治疗期间不良反应有QTC 间期延长、肝功能损伤、白细胞减少、咯血、心律失常、恶心呕吐等,与金武[20]报道的湖北地区贝达喹啉治疗MDR-TB 后不良反应观察结果相似,表明贝达喹啉治疗MDR-TB疗效确切且临床安全性较高,可有效提高治愈率,为MDRTB的治疗提供了新思路。观察组QTC间期延长发生率高于对照组(P<0.05),两组其他不良反应发生率比较,差异无统计学意义(P>0.05),与胡春梅等[21]的研究相近,表明贝达喹啉的不良反应发生率与常规治疗相当,但仍需Ⅲ期临床试验进一步验证。
综上所述,使用24周的贝达喹啉联合其他药物治疗MDR-TB 可明显提高痰MTB 培养阴转率,缩短阴转时间,其机制可能与调节T 淋巴细胞亚群水平有关,虽然QTC 间期延长较普遍,但患者总体耐受性良好,有临床推广意义。
- 广西医科大学学报的其它文章
- CTRP3 alleviates OGD/R-induced myocardial cell injury by activating the SIRT1/FoxO3a pathway
- 舒尼替尼通过调控lncRNA ROR/miR-670-3p/MARCH5轴对胃癌细胞增殖和凋亡的影响*
- LncRNA SNHG7靶向调节miR-146a-5p对胃癌细胞增殖、迁移、侵袭和细胞凋亡的影响*
- 高糖通过上调E2F1的表达促进肝癌细胞的侵袭和转移*
- lncRNA GABPB1-IT1靶向下调miR-501抑制宫颈癌细胞增殖、侵袭和迁移的机制*
- 姜黄素通过调控miR-152对甲状腺癌细胞TPC-1增殖、凋亡、迁移和侵袭的影响*

