多杀性巴氏杆菌主要毒力因子研究进展
尹媛媛,何 芳,赵光夫,李 攀,李能章,彭远义*
(1.西南大学 动物医学院,重庆 400715;2.四川大学 生命科学学院,四川 成都 610065)
多杀性巴氏杆菌(Pasteurellamultocida,Pm)是一种革兰阴性短杆菌,分别根据其荚膜抗原或脂多糖的多样性,可分为A、B、D、E、F共5种血清群或1~16共16个血清型。临床上,该病原主要导致动物呼吸系统疾病、局灶性感染及出血性败血症,如牛肺炎、禽霍乱、有蹄动物的出血性败血症、猪进行性萎缩性鼻炎、兔鼻瘘、牛羊猪等的船运热,以及人的皮肤脓肿、脑膜炎、蜂窝织炎、腹膜炎等[1]。Pm属于条件性致病菌,正常情况下常存于动物口腔、消化道和呼吸道,极少致病。当天气骤变、饲养环境差(如通风不良、潮湿、拥挤、饲料霉变)、营养缺乏、疲劳等,会导致动物免疫力降低,该菌易突破机体的防御屏障,经淋巴液侵入黏膜并大量增殖,逃避宿主的固有免疫系统造成内源性感染[2]。Pm引发的下呼吸道感染有极强的传染性,可直接通过空气传播和直接接触传播。
近年来畜禽的频繁调运导致的运输应激使Pm感染呈逐年上升趋势,MOORE等[3]分析了2010—2012年自澳大利亚运往中东、俄罗斯和中国的20次活牛长途运输中215头牛死亡的病因,发现59.4%死于呼吸道疾病,其中72.0%发生包括Pm、溶血性曼氏杆菌和支原体在内的病原微生物感染。Pm对人类健康同样构成了严重威胁,人可被携带了Pm的猫、犬等宠物抓伤而感染[4]。GREEN等[5]对1989—1999年多杀性巴氏杆菌脑膜炎病例报告进行了统计,发现17例患者中有5例(17%)患者出现了神经系统并发症。SAMKAR等[6]统计了截止2016年多杀性巴氏杆菌脑膜炎成年患者(88例)的典型症状,发现100%患者伴随发热现象,88%出现颈部僵硬,63%出现头疼,13%出现一定程度的后遗症,最终有20%患者不幸去世。
Pm对宿主的感染是一个多步骤的过程,只有成功逃避宿主的免疫系统并获得自身存活所需要的营养条件,才能在宿主体内繁殖定居。毒力因子是Pm在宿主体内存活、繁殖、致病的关键,对其致病性、在宿主体内的存活和繁殖能力都有重要作用[7]。Pm具有多种毒力相关因子,主要包括LPS、荚膜、OMPs、三聚体自转运蛋白、IROMPs、PlpE、PMT、PlpB、PtfA、FhaB和蛋白酶等[8]。现就近10年来国内外对Pm一些经典的和新发现的毒力因子的研究进展进行综述,以期为该菌的致病机制及新型疫苗研究提供参考。
1 脂多糖(LPS)
脂多糖(lipopolysaccharide,LPS)是革兰阴性菌细胞壁外膜较厚的脂多糖类物质,是细菌重要的毒力因子之一,参与细菌-宿主间相互作用(如识别、定殖和黏附中性粒细胞等)、膜屏障作用、发挥毒力作用和刺激宿主免疫反应等。完整的LPS由高度保守的内脂A(Lipid A)、疏水性的核心多糖和亲水性的O-抗原共同构成(图1),其中Lipid A包含脂肪酸链、磷酸基团和内核心寡糖,该结构与致病性密切相关。Pm的LPS包括Lipid A和核心多糖,不含O-抗原,且其核心多糖由内核心寡糖和外核心寡糖2部分组成。Pm有16种LPS血清型,其LPS合成基因分散于基因组中,不同血清型LPS的内核组装所需基因位于基因组的不同区域,而外核组装所需基因的区域较为稳定,成簇存在于保守基因priA和fpg之间的单个位点上,且不同血清型LPS可能具有相同的外核寡糖基因簇[9]。
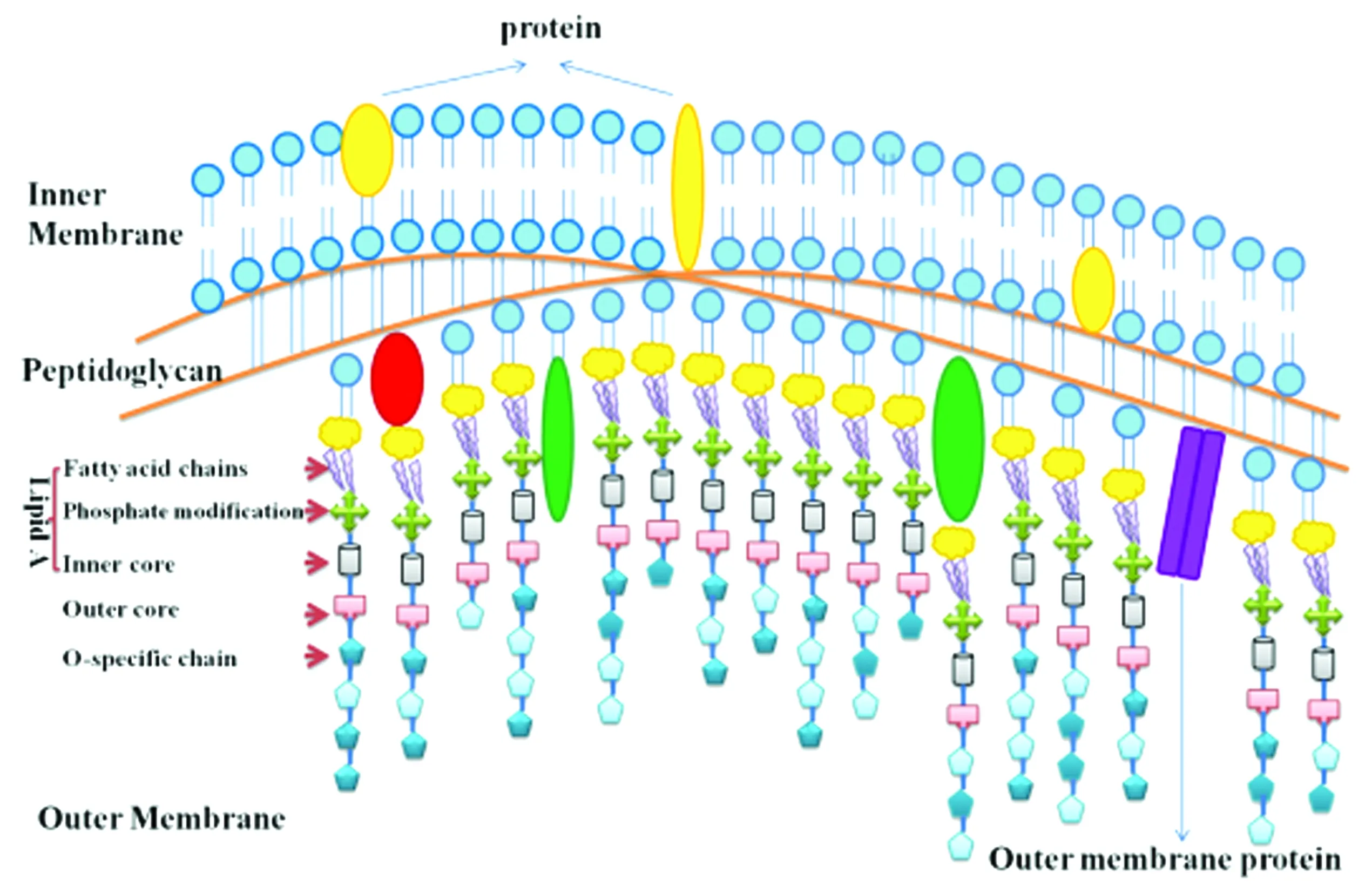
图1 LPS的完整结构图[10]
LPS的构象与其致病力的强弱密切相关,研究表明,糖基转移酶基因的突变、最外层磷酸胆碱残基和内核庚糖侧链的缺失都会改变LPS的主要构象,导致Lipid A暴露,从而增加Pm对抗菌肽的敏感性,降低其对天然免疫系统的抵抗力[11-12]。Pm的LPS和宿主糖蛋白结构相似,故LPS在发挥致病性过程中可以模拟宿主分子,提高Pm在宿主生态位的生存能力[13]。
LPS可通过Toll样受体4(TLR4)作用于免疫活性细胞,介导多种炎性因子的分泌[14]。胞外LPS与胞膜上TLR4相互作用后,激活MyD88-NF-κB信号通路,增强含半胱氨酸的天冬氨酸蛋白水解酶11(Caspase-11)的前体物质Pro-casp-11的转录和表达。Pm通过自身形成含有高浓度LPS的外膜囊泡,经巨噬细胞介导内吞形成吞噬体后,进入胞质,再由鸟苷酸结合蛋白2(guanylate binding proteins 2,Gbp2)破坏囊泡,将LPS暴露在胞浆内,与Pro-casp-11识别、聚合,并形成活化的Caspase-11。研究发现,Caspase-11是导致内毒素休克的关键因子。活化的Caspase-11可通过剪切成孔蛋白GSDMD形成GSDMD-NT,多个GSDMD-NT在胞膜上聚合形成孔道,诱导细胞发生焦亡,产生典型的内毒素性休克症状。同时活化的Caspase-11还能激活NLRP3/ASC-Caspase-1通路,介导IL-1β、IL-18等多种炎性因子的分泌与表达。当Caspase-11过度活化,致使大量胞内促炎介质释放到胞外,引起炎症反应(图2)。尽管LPS可诱导机体产生特异性免疫反应,但研究表明Pm的LPS的交叉保护性极弱。同时,不同血清型Pm的LPS免疫不同动物,产生的抗体水平和免疫保护效果也不同[15]。
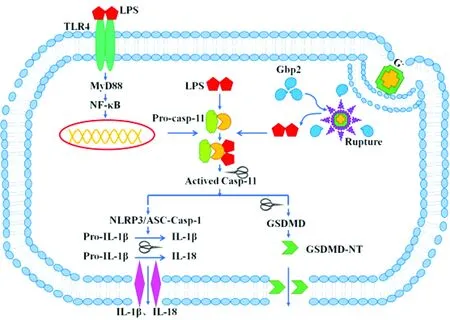
图2 LPS通过Toll 4介导炎性因子的分泌[16-17]
2 荚膜(capsula)
荚膜是分泌至菌体外的一类以多糖或多肽为主的物质,在细菌-宿主致病过程中起重要作用,如黏附、细菌扩散、抵抗宿主先天性和特异性免疫系统、细菌胞内生存和调节宿主细胞的细胞因子等,不同Pm荚膜血清型中荚膜的主要成分和作用不同(表1)。荚膜能够促进Pm的细胞黏附能力。BORRATHYBAY等[18]发现Pm荚膜中一种39 kDa的特异性蛋白能显著增强Pm对鸡成纤维细胞的黏附能力。另外,荚膜的有无决定了Pm的致病能力,有荚膜菌株对吞噬细胞的抵抗能力远高于无荚膜菌株,荚膜缺失突变株的毒力也低于野生株。研究表明,Pm荚膜是躲避中性粒细胞和单核吞噬细胞吞噬作用的重要免疫逃避因子[19]。Pm荚膜的缺失会降低Pm对抗补体介导的吞噬杀伤作用,导致致病力显著性降低[20]。CHUNG等[21]将四环素抗性基因插入A:1型Pm X-73菌株的hexA基因后,X-73株不能产生荚膜,对鸡的致病力明显减弱。

表1 不同荚膜血清型中荚膜的主要成分和作用
本实验室研究发现,Pm荚膜合成相关基因hyaC的点突变、Pm0442基因的缺失、群体感应基因qseC和luxS的缺失,以及编码假定三聚体自转运黏附素蛋白(TAA)的chr_orf01597基因的缺失,都会显著影响荚膜产量,降低Pm致病能力(未发表数据)。研究还发现,牛源A型多杀性巴氏杆菌(PmCQ2)感染巨噬细胞后能通过激活NLRP3炎性小体(NLRP3 inflammasome)和天冬氨酸蛋白水解酶1(Caspase-1),促进IL-1β的成熟及分泌[24]。进一步地,相较于PmCQ2,弱毒株PmCQ6荚膜含量少,更易被吞噬,对NLPR3炎性小体的激活程度也更高,进而诱导更高水平IL-1β的分泌[25]。
3 外膜蛋白(OMPs)
外膜蛋白(outer membrane proteins,OMPs)是主要的毒力因子之一,包括结构蛋白(OmpA、Omp28、Oma87)、外膜通道蛋白(OmpH、OmpW)、脂蛋白(PlpB、PlpE和Omp0979)、铁调节外膜蛋白(IROMPs)、转运蛋白、结合蛋白、黏附素、蛋白质组装器、孔蛋白和三聚体自转运蛋白等,多数OMPs具有抗吞噬作用。研究发现给牛皮下接种B:2型Pm的OMPs提取物,可引起出血性败血症,并对牛致死[26]。
Pm的OMPs跨膜区域为β-折叠,由偶数个β-分子反向折叠成β-桶状结构,将OMPs锚定在外膜上,部分β-桶状结构可作为离子通道,是一类作用于营养摄取、物质运输、感染宿主和激发免疫应答等过程的高免疫原性蛋白,具有良好的抗原性和免疫原性,常作为重要的疫苗候选抗原[27]。以OMPs制备的疫苗对小鼠、鸡和兔都有明显的保护力[28]。不同OMPs在不同血清型菌株中的种类、结构、功能和免疫学特性存在差异(表2)。

表2 OMPs的种类、结构、功能和免疫学特性

续表2
4 多杀性巴氏杆菌毒素(PMT)
多杀性巴氏杆菌毒素(Pasteurellamultocidatoxin,PMT)是一种由D型和少数A型产毒素多杀性巴氏杆菌(toxigenicPasteurellamultocida,T+Pm)产生的皮肤坏死毒素,能引起猪进行性萎缩性鼻炎,本质是一种高活性的有丝分裂原。PMT可与破骨细胞、成骨细胞、T细胞、T辅助细胞和纤维母细胞上的受体结合,影响其生长分化。PMT可阻断成骨细胞的进行性变性,使鼻甲骨的生长、合成与吸收失衡[50-53]。当PMT达到一定浓度时,促进纤维原细胞和造骨细胞的DNA合成,诱导破骨细胞和成骨细胞的前体大量生长,提高骨的吸收能力,使细胞骨架重排,如引发猪的进行性萎缩性鼻炎。PMT可制备成类毒素保护小鼠及其后代抵抗PMT。通过基因修饰置换掉PMT的2个关键氨基酸,新翻译的无毒性蛋白可保护野生型毒株对猪的感染。口服PMT和硫醇盐丙烯酸树脂微粒(TEMS)混合制备成的W/O/W乳剂,前者能在后者的包裹下缓慢释放,促进巨噬细胞分泌TNF-α和NO,增强疫苗的免疫作用[54]。
PMT通过激活Galphaq/11家族的异源三聚体G蛋白,与鸟嘌呤核苷酸交换因子(p63 RhoGEF)发生特异性反应,激活RhoA蛋白,活化的RhoA在Rho激酶的帮助下,可以刺激有丝分裂原激活蛋白(MAP),引起一系列级联反应。该过程涉及到原癌基因(Ras)、MAPK/ERK激酶1(MEK-1)和细胞外信号相关激酶1/2(ERK1/2),改变相关基因的表达,从而抑制骨细胞的分化(图3A)。
除了由RhoA蛋白介导的PMT致病通路外,还存在由G蛋白q家族的α亚基(Gαq)这个高度专一的直接靶点介导的致病通路。具体通路是:PMT先通过脱酰胺基和磷酸化作用激活α亚基,三聚体G蛋白复合物随之解开,再通过JAK-STAT通路激活磷酸肌醇特异性磷脂酶C-β1(PLCβ1)和颗粒酶A,颗粒酶A切割IL-1β前体形成成熟的IL-1β。活化的C-β1通过水解磷脂酰肌醇4,5二磷酸(PIP2)形成1,4,5-三磷酸肌醇(IP3)及二酰基甘油(DAG),IP3和DAG可结合细胞内游离的Ca2+和蛋白酶C(PKC),从而抑制成骨细胞的诱导分化作用(图3B)。
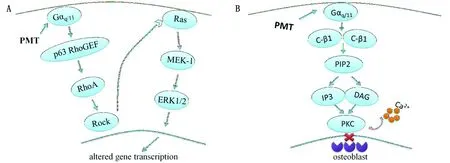
A.RhoA蛋白介导;B.C-β1介导图
5 黏附相关因子
对细胞的黏附作用是Pm定殖和感染宿主的前体条件,其中起主导作用的是荚膜、菌毛和一些黏附相关基因。研究发现PlpB蛋白与Pm对鸡成纤维细胞的黏附力密切相关,该蛋白影响Pm的毒力、致病性和对细胞的附着能力,发挥黏附因子作用,可以调节IL-1、IL-3、IL-4、TNF-α和TNF-β等炎性因子的分泌[18]。除鸡成纤维细胞外,PlpB也有助于增强Pm对白细胞和内皮细胞的黏附作用[58]。PRUIMBOOM等[59]在研究Pm对火鸡巨噬细胞的附着机制发现,向巨噬细胞中添加透明质酸可抑制Pm黏附,用透明质酸酶解聚Pm荚膜可增加巨噬细胞的吞噬能力,同时降低Pm的黏附能力、抗吞噬能力和致病性。证明荚膜的有效成份透明质酸在Pm黏附过程发挥重要作用。
Ⅳ型菌毛(PtfA)广泛存在于A、B、D型Pm中,与宿主嗜性和致病性密切相关,被认为是潜在毒力因子之一[60]。Pm70基因序列中也包含多种能编码类似菌毛功能的黏附相关基因,如HadA、fimA、flp1、flp2、Hsf-1、Hsf-2等。由他们编码的相关蛋白如:黏附素A(HadA)、自转运黏附素1(Hsf-1)、自转运黏附素2(Hsf-2)都能影响Pm的定殖和感染[61]。
6 丝状血球凝集素蛋白(PfhB)
血球凝集素家族的PfhB存在于多种细菌和病毒表面,参与细胞的识别和附着,能够专一且可逆地结合到特异性单(多)糖上。Pm具有PfhB1和PfhB2(或称为FhaB1和FhaB2)2种丝状血凝素,与生物被膜形成、Pm定殖和毒力有关。PfhB1和PfhB2功能的缺失,可以显著降低Pm的毒力作用[62]。主要由于pfhb1和pfhb编码的肽酶C58结构域具有细胞毒性,而致病因子PfhB1和PfhB2上都包含肽酶C58结构域、血凝素活性结构域和血凝素重复结构域[63]。
pfhb1和pfhb2在Pm最初的入侵和定殖中发挥重要作用。敲除pfhb1会导致禽源菌株C48-102毒力下降,并降低Pm对补体的抵抗作用。诱变pfhb1并对火鸡鼻内接种,发现pfhb1的失活可显著降低禽源菌株P-1059的致病力;改为肌肉接种,其毒力同样适度减弱。诱变禽源A:3型Pm菌株的pfhb2后感染火鸡,不管是鼻内接种还是静脉注射,pfhb2的失活均显著降低了Pm的致病力,且鼻内接种的降低程度更显著。敲除pfhb2亦会降低禽源菌株P-1059的毒力,但不影响对补体的抵抗作用[64]。突变P-1059菌株的pfhb2后感染小鼠,发现菌株完全减毒[65],以Pm的FHAB2多肽重组体免疫火鸡,可以对不同血清型的Pm产生免疫保护性,除PfhB1和PfhB2外,PfhB6同样能对单一血清型提供保护,且在多种血清型中保守性较高[66]。
7 蛋白酶及其他
Pm可通过抑制抗体活性逃避宿主的免疫机制,促进定殖和感染[67]。其中发挥主要作用的是Pm分泌的蛋白酶,它作用的底物是免疫球蛋白IgG和IgA,能够降低这些抗体的活性和水平。目前研究的其他毒力因子还包括神经氨酸酶(NanB、NanH)、超氧化物歧化酶(sodA、sodC)、紧密黏附蛋白(TadD)、透明质酸酶(Pm HAS)、菌毛亚单位蛋白(FimA)、皮肤坏死毒素(ToxA)等[68]。
本实验室前期建立的牛源A型PmCQ2感染小鼠肺炎模型发现,相较于其他毒力基因,Pm0442基因和qseC基因可在PmCQ2感染小鼠的肺脏中大量表达。同野生型菌株比,PmCQ2-Δ0442的荚膜含量、黏附、入侵以及毒力均下降。PmCQ2-ΔqseC的荚膜含量、毒力和在小鼠肺部的定殖量同样极显著降低。推测Pm0442基因和qseC基因是PmCQ2的毒力相关基因(未发表数据)。
8 总结与展望
目前,Pm仍是威胁畜禽养殖业和人类公共卫生安全的重要病原菌之一,其致病性可能是多种毒力因子协同作用的结果。不同血清型的Pm抗原性、宿主特异性和致病机理不同,感染后临床症状也不相同,毒力因子的具体作用机制也有待深入研究。很多毒力因子被证实与Pm的结合、转运、黏附、定殖、入侵等过程有关。多种菌体蛋白被认为是疫苗开发中的潜在靶抗原,如OmpA、OmpH、PlpB和PlpE都具有良好的免疫保护作用,可作为预防和治疗多杀性巴氏杆菌病的新型疫苗候选靶标。基于这些毒力因子的研究,有助于阐明Pm的致病机理,促进疫苗的研制,减少畜禽养殖中因多杀性巴氏杆菌病引起的经济损失。

