巩膜扣带术治疗合并视网膜下增生的孔源性视网膜脱离的疗效观察
杨 琼,魏文斌
0引言
孔源性视网膜脱离(rhegmatogenous retinal detachment, RRD)是严重威胁视力的眼底病之一,发生率6.3/10000~17.9/10000[1]。巩膜扣带术(scleral buckling,SB)和玻璃体手术(pars plana vitrectomy, PPV)是治疗RRD两种主要术式,前者适用于不复杂的RRD,而对于复杂的RRD目前主要采用PPV术治疗。增殖性玻璃体视网膜病变(proliferative vitreoretinopathy, PVR)是视网膜脱离后的自我创伤修复也是视网膜脱离手术失败的主要原因,继发的细胞迁徙和胶原纤维增殖引起视网膜内外表面的增殖膜形成,继而收缩牵引形成视网膜皱褶甚至视网膜脱离[2-3]。因此对于PVR C级以上的病例,通常需要玻璃体手术剥除前膜解除牵拉增殖才能恢复视网膜的柔软度。但临床上还有一部分以视网膜下增生为主的视网膜脱离病例,虽然也是PVR的一种亚型,但部分病例是可以选择SB治疗,本文总结了一组相关病例,并分析其临床特征及SB治疗的有效性。
1对象和方法
1.1对象回顾性临床分析研究,收集2016-10/2020-01就诊于北京同仁医院眼科的合并视网膜下增生的RRD患者54例54眼。所有患者治疗前均签署知情同意书,该研究方案得到北京同仁医院伦理委员会的批准。纳入标准:合并视网膜下增生且裂孔位于赤道前的孔源性视网膜脱离患者。排除标准:PVR C级以上且合并明显视网膜表面增生的患者;屈光间质明显混浊影响间接检眼镜使用者如明显白内障、玻璃体积血等;裂孔位于赤道后;其他原因不适合扣带术的患者。
1.2方法所有患者均行全身麻醉下SB复位视网膜,间接检眼镜下冷冻定位裂孔,根据个体情况选择适当外加压物,再结合冷冻、放液等操作复位视网膜。外加压材料在本组患者均为硅胶带,宽度分别为4.5mm(型号219)和2.5mm(型号240),其中型号219用于外加压封闭裂孔,型号240用于环扎。5-0不可吸收线缝合外加压带,放液采用尖刀片行全层巩膜切开后,用刀片尖或1mL无菌针头刺穿脉络膜放液。术中选择单纯外加压8眼(15%),外加压联合环扎46眼(85%)。术中放液34眼(63%),未放液20眼(37%)。对于术中未找到明确孔的3眼(6%),将周边可疑位置缝合外加压并联合环扎。随访时间5~39(平均19.17±11.15)mo。收集患者人口学资料、视网膜脱离范围、裂孔位置数量、视网膜下增生位置及范围、手术前后最佳矫正视力(BCVA)、眼压、视网膜复位情况及并发症等。BCVA检查采用国际标准视力表进行,统计时换算为最小分辨角对数(LogMAR)视力;数指、手动、光感分别对应1.7、2.0、2.3LogMAR单位。眼底检查裂孔完全贴服于加压嵴且无肉眼可见的视网膜下液为视网膜完全复位。视力较术前提升≥2行定义为视力提高。
统计学分析:采用SPSS 23.0统计软件,用百分比描述分类数据,手术前后BCVA比较采用配对样本t检验,以P<0.05为差异有统计学意义。
2结果
纳入患者54例54眼中男36例,女18例,年龄7~60(平均24.92±11.99)岁,所有患者一般资料见表1。

表1 纳入患者一般资料及视网膜脱离情况
术后视网膜完全复位52眼(96%)(图1),其中术后1d完全复位31眼(57%),末次随访时术后视网膜下液逐渐吸收至完全复位21眼(39%);视网膜未复位2眼(4%),1眼失败原因是PVR(视网膜表面增生),1眼为遗漏裂孔(SB术中未查到明确孔,PPV术中发现鼻侧锯齿缘附近小孔),均行玻璃体手术后复位。
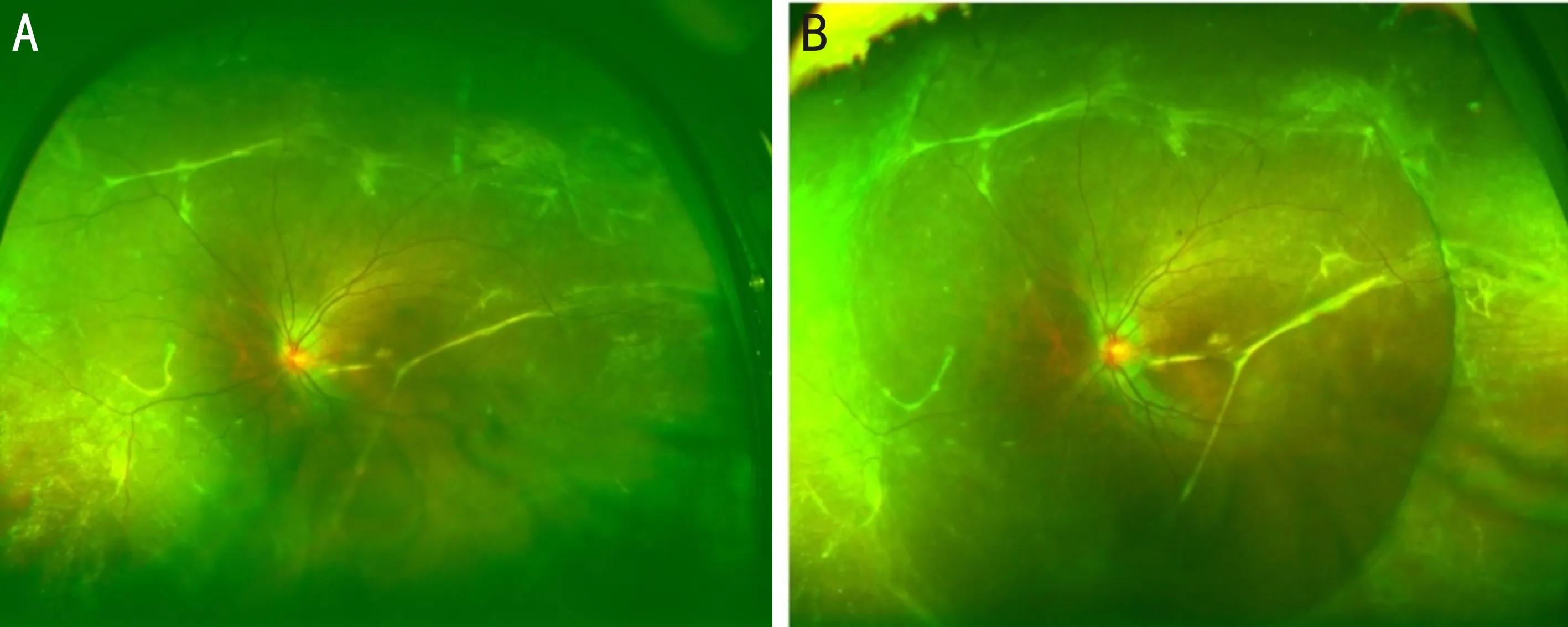
图1 14岁男性视网膜复位前后对比图 A:左眼陈旧RRD,视网膜下增生超过3个象限且同时累及赤道前和后,颞侧周边萎缩孔;B:SB术后1wk,视网膜基本复位,鼻侧残留部分视网膜下液,可见加压嵴,孔在嵴上。
术前平均BCVA(LogMAR)为1.21±0.77,术后为0.61±0.40 ,手术前后BCVA比较差异有统计学意义(P<0.01)。术后47眼(87%)视力提高。
术中发生并发症3眼(6%),其中放液点出血至视网膜下2眼(4%),放液点穿孔1眼(2%),将放液点冷冻后放置于加压嵴上,术中并发症均未影响视网膜复位。术后发生并发症1眼(2%),为硅胶带感染暴露,该例患者在术后14mo拆除硅胶带,未影响复位。
3讨论
文献报道视网膜下增生在所有RRD相关的PVR中占47%[4-5],而在不复杂的RRD中占3%~15.5%[6]。PVR作为评估视网膜脱离手术选择的重要指标,有关PVR的分型也在发生变化,1983年视网膜学术委员会主要根据玻璃体及视网膜表面增生将其分为A、B、C、D四级,也是目前使用最广泛的分级方法,但这种分型的局限是无法体现增生发生的具体位置形态等。在1991年又制定了新的PVR分型,将其分为A、B、C三级,其中将C级又分为前部及后部,并将增殖的位置和形态做了更详细的描述,在这种分级中就包含了视网膜下增生并将其纳入PVR C级中[7-8]。视网膜下增生和玻璃体视网膜表面的增生有所不同,通常是发生在较年轻的患者,玻璃体黏稠且没有后脱离,较视网膜前膜更不容易形成收缩牵拉;视网膜下增殖也预示病程较长,是陈旧视网膜脱离的表现之一,通常裂孔都是以周边萎缩孔为主。因为视网膜下增生并不都造成视网膜收缩皱褶,因此视网膜下增殖膜并不都需要手术剥除,文献报道玻璃体切除术中仅有28%的视网膜下膜需要被剥除[4],其余并不影响视网膜复位。鉴于以上原因,单纯合并视网膜下增生而不伴有明显视网膜表面增生的RRD多数是适合SB的,当外加压将裂孔封闭后视网膜下液吸收,残留的视网膜下增生不影响视网膜复位。
SB治疗简单的RRD的复位率在80%~90%[9-13],合并视网膜下增生的RRD采用SB的报道不多,Ghasemi等[2]报道43例合并视网膜下增生的视网膜脱离行扣带术成功率为88.7%;Zhou等[14]报道159例SB联合眼内充气治疗复杂视网膜脱离成功率达91.82%,Wallyn等[15]报道SB治疗20例合并孤立的视网膜下增生的视网膜脱离复位率95%。本组病例的52眼一次复位,复位率96%,分析原因可能包括:(1)本组病例平均年龄24.92±11.99岁,年轻患者为主,玻璃体较黏稠无明显液化,裂孔以变性区内的萎缩孔为主多位于周边部视网膜,虽然有15眼(28%)的多发裂孔甚至3眼(6%)未查到明确裂孔,但是裂孔的数量并不是影响SB成功的重要因素,裂孔位置是更重要的参考条件,裂孔过于靠后或者多发裂孔位于不同纬度难以通过一处加压材料将所有裂孔完全封闭更容易导致SB手术失败。(2)虽然所有患者均合并不同程度的视网膜下增生,但是并未形成明显的视网膜收缩皱褶,裂孔封闭后,视网膜神经可以贴服于视网膜色素上皮;(3)46眼(85%)采取外加压联合环扎的术式,在本组病例里占主导术式,环扎的优势是可以浓缩玻璃体部分缓解周边部玻璃体视网膜的牵拉,减轻裂孔周围的牵引力,比较适用于陈旧RRD。另外,本组34眼(63%)选择了放液,剩余未放液病例均为液过浅或液靠后极放液困难的病例,对于视网膜脱离时间较长的病例,由于视网膜活动度略差且视网膜下液较黏稠不易吸收,建议尽量放液。本组病例术中及术后均未出现严重并发症,手术安全性较好,在视网膜复位后,47眼(87%)视力得到改善。
总之,对于年轻患者合并视网膜下增生但不伴有视网膜表面增生的RRD,如果选择PPV,术中可能需要取出视网膜下膜,这将增加手术操作难度及视网膜损伤,增加视网膜脉络膜出血风险[16],年轻患者玻璃体黏稠且无后脱离不容易清除干净,填充物如硅油容易引起晶状体混浊等并发症,因此这部分病例可能SB不失为更优选择。但是本组纳入病例数不多,且是回顾性分析无对照组,选择的病例有一定的共性可能导致分析结果的偏移,临床上还是要结合患者病情及医生手术经验选择最合适的术式。

