孕期B族链球菌感染对胎膜早破和新生儿影响及药敏分析
黄晓林 严静静
江苏省南京市江宁医院 (211100)
B族溶血性链球菌(GBS)是引发妇科疾病的常见需氧致病菌,也被称为无乳链球菌[1],主要在人体消化道与泌尿生殖道定植,尤其是育龄期女性容易携带,成为导致孕产妇生殖道感染的关键因素,增加早产、产褥期感染、胎膜早破等发生风险[2]。由于GBS对于绒毛膜有较强穿透、吸附能力,能够在母体组织吸附,继而侵入绒毛膜促使胎膜早破的发生[3]。有研究报道显示,我国GBS感染率达3.5%~32.4%,南京市感染率为4.1%,母婴垂直传播是GBS传染的主要途径[4]。现在研究多停留在分析孕期GBS感染对妊娠结局的影响,但较少报道降低或改善GBS感染的不良妊娠结局,系统地采用大样本分析如何给予有效护理干预孕期GBS感染的报道更少。本研究将本院妇产科接受GBS筛查的1266例孕妇为观察对象,分析GBS感染待分娩孕妇给予抗感染治疗并建立针对性护理计划对降低胎膜早破及改善妊娠结局的效果。
1 资料与方法
1.1 研究设计
研究采用回顾性、开放、对照临床研究方法设计,以本院妇产科2018年1-8月收治的接受GBS筛查的1266例孕妇为观察对象,其中220例为胎膜早破孕妇为观察组,余1046例为对照组。所有入选对象与家属均知情并签署知情同意书。本研究经院伦理委员会审批。
1.2 纳入及排除标准
纳入标准:①经B超检测结果为单胎头位;②经妇科检查、GBS检测结合临床表现确诊为生殖道GBS感染;③1个月内未行其他抗生素治疗。排除标准:①胎儿发育延迟,即首次胎动16~20w,孕24w母体外测量宫高连续3次无增长[5];②既往有习惯性流产史;③合并心、肝、肾等严重功能障碍;④凝血功能障碍;⑤伴随妊娠高血压、糖尿病或泌尿系统感染。
1.3 试剂与仪器
全自动细菌鉴定分析仪(梅里埃VITEK 2 Compact),主要试剂为GBS核酸检验试剂(泰普生物科学公司)。
1.4 检测方法
孕妇均行GBS检测。①标本采集:常规清洗消毒处理,窥阴器扩张阴道,应用无菌棉拭子在阴道下1/3部位采集分泌物;同时用另一无菌棉拭子在肛门括约肌上方2~3cm部位旋转1周,采集直肠分泌物;将两份棉拭子制作为标本后送检。②细菌培养:将标本接种至含有多粘菌素、甲紫、萘啶酮酸的培养基中,35℃孵育24h;置于哥伦比亚血培养基,35℃培养24h,对阳性格兰感染者行触酶或环磷酸腺苷试验,再次确认后以全自动细菌鉴定分析仪检测,依照GBS核酸检测试剂说明进行。③药敏检测:应用制片扩散法,取孕妇GBS菌落制备浓度0.5MCF溶液,涂抹在M-H平板,再加入其中抗感染药物药敏制片,置35℃培养箱孵育18h,判定药敏检测结果。
1.5 治疗及干预
对感染孕妇抗感染治疗,若孕妇对青霉素无过敏反应给予青霉素(山东鲁抗医药股份有限公司),首次500万U与0.9%氯化钠注射液250ml混合后行静脉滴注,随后每4h给予250~300万U至孕妇分娩。若孕妇对青霉素过敏给予克林霉素(重庆莱美药业股份有限公司)900mg,与0.9%氯化钠注射液250ml混合后静脉滴注,每8h给予900mg至孕妇分娩。足月胎膜早破,GBS(+),应立即应用预防性抗生素并尽快引产;未足月>34周,GBS(+),积极终止妊娠并促胎肺成熟,<34周者给予抗生素治疗同时应用宫缩抑制剂保胎。密切监测产妇与宫内胎儿各项生命体征变化。对GBS阳性孕妇进行有效干预措施:根据孕妇特点建立针对性护理计划。采用健康宣教方式耐心讲解疾病感染机制、治疗情况及预后;定制高营养、高蛋白食物,保证睡眠,提高治疗效果。
1.6 疗效指标
比较两组孕妇临床基础资料,包括年龄、孕周、孕产史等。统计组间剖宫产、孕妇胎膜早破、产褥感染、宫内感染、产后出血等发生率;新生儿不良结局,包括新生儿感染、胎儿窘迫、新生儿窒息、新生儿肺炎。对两组新生儿娩出后1min、5min采用阿氏评分(Apgar),0~10分,<7分为存在轻度窒息,分值越高则新生儿越健康[6]。感染组孕妇为药敏试验后结果。问卷调查孕妇对产前护理、分娩情况、产后指导等满意度,满分为100分,>80分为满意。
1.7 统计学方法

2 结果
2.1 孕妇临床资料
GBS检测结果显示,观察组GBS阳性27例,阳性率12.3%;对照组GBS阳性58例,阳性率5.5%。GBS阳性者共计85例纳入感染组,GBS阴性者1181例纳入非感染组,两组孕妇临床基础资料比较无差异(P>0.05)。见表1。
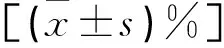
表1 两组孕妇临床资料比较
2.2 妊娠结局
两组孕妇剖宫产率无差异(P>0.05),感染组胎膜早破、产褥感染、宫内感染、产后出血等妊娠不良事件发生率高于非感染组 (P<0.05)。见表2。

表2 两组孕妇妊娠结局比较[例(%)]
2.3 新生儿结局
新生儿不良结局总发生率感染组高于非感染组(P<0.05)。见表3。感染组新生儿娩出后1min(7.0±0.8分)、5min(8.4±1.7分)Apgar评分均低于非感染组(8.2±1.3分、9.0±2.0分)(t=8.395、2.696,P=0.000、0.008)。
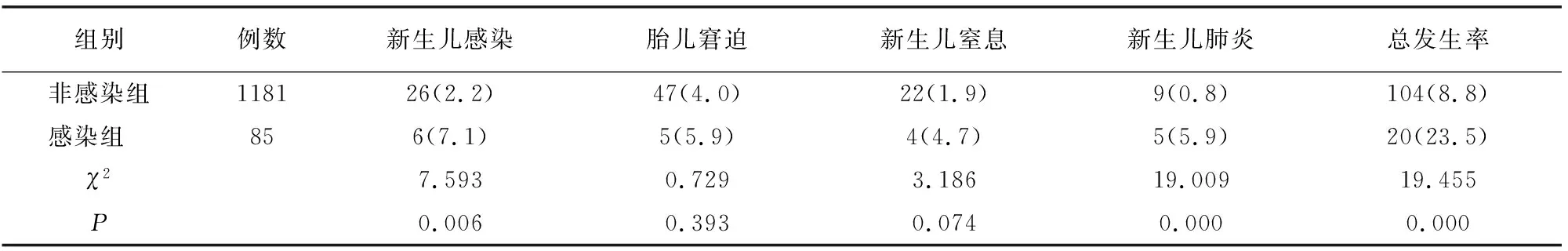
表3 两组新生儿不良结局比较[例(%)]
2.4 GBS感染药敏试验
感染组孕妇经药敏试验结果显示,青霉素与头孢菌素敏感性更高,克林霉素、阿米卡星敏感性较低。见表4。

表4 GBS感染的药敏试验结果(n=85)[例(%)]
2.5 感染组患者诊疗满意率
85例感染组孕妇均接受护理干预,满意度为100%(85/85)。
3 讨论
生殖道感染是由多种致病微生物所引发的妇科感染性病症,GBS作为人体直肠与阴道正常寄居菌群,随着机体抵抗力降低,其寄生环境发生变化,微生态平衡被破坏,继而侵入机体并形成感染[7-8]。而孕妇在妊娠过程中处于特殊阶段,比较未妊娠女性其生殖道病原菌微生物感染几率增高。有研究调查数据显示,在不同种族、不同区域的孕妇中,GBS感染率为3.5%~32.4%%,妊娠晚期孕妇发生GBS感染后新生儿病死率更高[9-10]。而导致其发生主要与孕妇妊娠中内分泌波动幅度大,提高了雌激素与孕激素释放,从而降低机体局部细胞抵抗力;同时孕妇阴道中糖原水平增高,为病菌感染提供了良好的繁殖环境,使得GBS感染风险提高[11]。当孕妇发生GBS感染后,往往会诱发泌尿系统感染、败血症、绒毛膜羊膜炎、早产等,而胎膜早破、新生儿围生期感染则是其中尤为严重的不良反应[12];分析原因可知,孕妇在GBS感染后会经分娩、乳汁、母体子宫等途径传播给新生儿;同时GBS对于绒毛膜具有较强吸附力与穿透力,能够诱发炎症反应,促使维持细胞骨架的角蛋白表达水平下调,导致胎膜早破[13-14]。另外,孕妇多因胎儿头盆不对称、多胎导致宫内压增高,导致胎膜早破,增加难产率,且胎膜早破后,羊水减少,子宫收缩加大,胎儿承受压力增加,易出现胎儿窘迫、窒息等不良新生儿结局。
胎膜完整能够有效防止阴道发生逆行性感染。在正常情况下,阴道常驻菌群与机会致病菌能够维持阴道微生态平衡状态,而阴道正常解剖结构与上皮分泌功能则维持着阴道酸性环境,抑制致病菌增殖[15-16];但孕妇在妊娠中,体内激素水平与宫腔内环境发生变化,致使阴道壁黏膜水肿、充血,降低阴道自身屏障作用,使优势菌群发生变化,外来菌群繁殖,引发感染[17]。张紫娟[18]等通过分析GBS感染与阴道微生态失调对于胎膜早破和妊娠结局的影响,发生胎膜早破孕妇阴道pH值>4.5占比与GBS感染率、微生态失调率均较未发生胎膜早破者增高,分别为58.75%、17.5%、85.00%;而GBS感染阳性者发生产褥感染、绒毛膜羊膜炎、胎儿窘迫及新生儿肺炎等分别为35.71%、35.71%、42.86%、28.57%。本次研究中,接受GBS筛查的1266例孕妇中220例为胎膜早破孕妇;GBS感染组孕妇妊娠不良事件及新生儿不良结局非感染孕妇,提示GBS感染可增加母婴妊娠风险。在张莹[19]等研究,针对孕妇GBS感染致使胎膜早破者行抗感染治疗,与未发生GBS感染孕妇组产褥感染、宫内感染、新生儿胎儿窘迫及早产发生率无明显差异,且胎膜早破、新生儿肺炎、新生儿窒息发生率降低。证实对GBS感染孕妇实施抗感染治疗,可有效降低母婴新生儿不良结局。本次研究中,对85例GBS感染孕妇药敏试验结果显示,青霉素与头孢菌素敏感性更高,均达到90%以上,而克林霉素、阿米卡星敏感性较低。因此在行临床治疗中可选择青霉素与头孢菌素药物治疗,控制GBS感染,帮助孕妇顺利度过分娩期,有效降低胎膜早破及新生儿不良事件发生风险,改善母婴结局[20-21]。新生儿感染GBS早期症状不太明显,应每4h检测患儿体温、脉搏、呼吸、吃奶情况,将感染患儿与非感染患儿进行隔离,避免交叉感染。同时保持并放干净,避免患儿被惊吓、打扰等中断睡眠。本研究中感染组孕妇护理干预后满意度为100%,表明护理干预作用较好。
综上所述,孕期GBS感染会提高新生儿围生期不良事件及胎膜早破发生风险,因而当待分娩孕妇确诊感染后需即可行药敏实验,并选择针对性抗生素及护理干预,使胎膜早破发生率降低,改善母婴不良结局。

