乳制品样品前处理与分析检测技术研究进展
陈雅莉,扈洪志,肖小华,李攻科
(中山大学 化学学院,广东 广州 510275)
乳制品是以牛奶、羊奶、驼奶等动物乳为原料的各种食品,主要包括液体乳类、乳粉类、炼乳类、乳脂肪类、干酪类、乳冰淇淋类和其他乳制品类七大类[1]。牛奶中含脂肪、蛋白质、人体所需的20种氨基酸以及较丰富的矿物质,是膳食中蛋白质、钙、磷、维生素A、维生素D和维生素B2的重要来源之一[2]。近年来,我国特色奶畜种饲养量逐年增加且分布广泛,其中羊奶是发展较好的特色奶品种[3]。羊奶分为山羊奶和绵羊奶,是世界上公认最接近人奶的乳品,以其营养丰富、易于吸收等优点被称为“奶中之王”。驼乳为驼科动物双峰驼的乳汁,富含维生素C、不饱和脂肪酸、铁和维生素B,被视为一种不可替代的营养品。随着各类乳制品成为家庭日常摄入的营养物质,其质量安全问题也成为大家关注的重点。
乳制品中的有害物质主要包括农兽药残留、毒素、重金属、微生物、有害添加剂以及在包装或运输过程中引入的其他有害物质。一般来说,农药、霉菌毒素以及重金属残留主要来源于被污染的动物饲料或食料,其中黄曲霉毒素B1(Aflatoxin B1,AFB1)是天然产生的强致癌物之一[4]。β-内酰胺类、磺胺类、大环内酯类、四环素类抗生素[5]被广泛用来预防或治疗动物细菌性感染疾病,一些抗生素还被用作添加剂以延长牛奶保质期。
乳制品保存不当可产生大肠杆菌等多种微生物[6],如沙门氏菌可导致感染者腹泻、腹痛、呕吐和发烧[7];李斯特菌是新生儿脑膜炎的常见病因之一[8]。乳制品中的有害添加剂包括三聚氰胺、过氧化氢[9]、甲醛等防腐剂,色素类添加剂以及从食品包装材料中迁移到乳制品中的塑化剂、多氯联苯[10]等,具有干扰内分泌、致癌等危害。
乳制品种类多、基质复杂,有害物质结构和性质差异大、含量水平低,亟需发展快速高效的样品前处理技术和准确灵敏的分析检测方法。本文综述了近十年来乳制品样品前处理方法的研究进展,包括固相(微)萃取法、液相(微)萃取法、免疫亲和色谱法等;介绍了各类有害物质的分析检测方法,如色谱法、原子光谱法、电化学分析法、生物免疫法、分子光谱法等的研究进展,重点比较了实验室分析方法与现场快速检测方法的优势与不足。
1 乳制品的前处理方法研究进展
乳制品通常是高粘度或固态样品,且基质复杂、干扰严重,易给后续分析结果带来不利影响,需要快速高效的样品前处理技术。在标准方法中,乳制品一般先通过乙腈萃取或皂化除去脂肪和蛋白质,再利用正己烷[11]、乙酸乙酯[12]等溶剂萃取;萃取液进一步经固相萃取柱[13]、阴/阳离子交换柱[14]等净化,或将微生物通过增菌培养[15]后,采用色谱等进行分析。
乳制品中大部分有害物质可以使用基于相分配或相吸附原理的样品前处理方法,这两种方法各有优势且应用广泛(见表1),下面对这两类方法分别进行介绍。
1.1 基于相分配原理的样品前处理方法
1.1.1 液-液萃取 液-液萃取法(Liquid-liquid extraction,LLE)是经典的样品前处理方法,通过适当有机溶剂从乳制品中萃取目标分析物,如黄曲霉毒素[16]、农药、植物激素、兽药[17]等。三聚氰胺一般选择乙腈-水[18]混合物、甲醇-水[19]混合物、酸性溶液[20]等作为萃取溶剂。低温纯化技术能沉淀蛋白质和脂肪,可以作为LLE的辅助纯化方法[21]。
盐析辅助液-液萃取技术通过向样品溶液与萃取溶剂混合物中加入无机盐实现目标物的相分离,使用与水混溶的有机溶剂为萃取剂,可提高极性分析物的萃取效率,萃取溶剂与样品溶液互溶,两相接触面积大,富集程度更高。Moreno-González等[22]建立了婴儿牛奶和酸奶中15种β-内酰胺的盐析辅助液-液萃取/超高效液相色谱-串联质谱(UPLC-MS/MS)分析方法,检出限为0.2~2.7μg/kg。
1.1.2 液相微萃取 常规LLE有机溶剂消耗量大,对环境及操作人员健康不友好,微型化、环境友好的液相微萃取法(Liquid-phase microetraction,LPME)在乳制品前处理中被更广泛地使用。LPME包括中空纤维液相微萃取(Hollow fiber liquid-phase microetraction,HF-LPME)、电膜萃取(Electromembrane extraction,EME)以及分散液-液微萃取(Dispersive liquid-liquid microextraction,DLLME)等[23-24]多种模式。
HF-LPME方法分为两相HF-LPME和三相HF-LPME[25-26],主要通过支撑液膜上的被动扩散和分析物分配系数来调控目标物的富集倍数和选择性,但需要较长萃取时间。Huang等[26]利用HF-LPME方法萃取牛奶样品中的黄曲霉毒素M1(Aflatoxin M1,AFM1),萃取时间为50 min,富集倍数(EF)为48。
EME中电场的引入可进一步加速带电目标物的萃取过程[27],目前已开发出许多新的膜材料来改善EME的萃取性能,包括各种复合材料、聚合物包裹物膜和凝胶膜[28]。Aghaei等[29]利用基于还原氧化石墨烯和银纳米颗粒协同作用的EME方法萃取牛奶样品中的氨苄西林,EF可达到295。
DLLME将非极性萃取溶剂和极性分散剂快速注入水性样品中以形成浑浊溶液,萃取溶剂的细小液滴可分散在水性样品中进行萃取,具有非常高的富集效果。如Alshana等[30]利用DLLME萃取牛乳和乳制品中的5种非甾体类抗炎药,EF为46~229。
一些环境友好的新型材料已被用作液相微萃取的萃取溶剂,其中超分子溶剂是最受欢迎的溶剂体系之一[31]。而离子液体(Ionic liquid,IL)[32]具有渗透性好、乳液形成少、相分离速度快和生物相容性等特性,尤其是磁性离子液体(Magnetic ionic liquid,MIL)[33],兼具IL的优点并可响应外部磁场,可利用磁铁实现样品的快速分离[34]。深共熔溶剂(Deep eutectic solvent,DES)是由安全、廉价、可再生和可生物降解化合物组成的离子液体廉价类似物,也可用作萃取溶剂[35]。将DES与磁性材料混合,利用磁场分离目标物,有助于目标物的积累[36],进一步提高样品富集效率。
1.2 基于相吸附原理的样品前处理方法
1.2.1 固相萃取 与LLE相比,固相萃取法(Solid-phase extraction,SPE)回收率高、有机溶剂用量少,并可同时萃取宽极性范围分析物。其吸附剂种类繁多,且易与分析检测技术结合,在乳制品有害物分离富集中应用广泛。传统的C8、C18等SPE吸附材料萃取选择性较低,近年来,具有高萃取能力、高表面积、多活性位点和丰富表面官能团的新型材料,如碳纳米管(Carbon nanotubes,CNTs)、石墨烯基材料和纳米材料等[37]已被广泛用于SPE。如Jiang等[38]利用还原氧化石墨烯/金纳米颗粒作为SPE吸附材料,结合UPLC-MS/MS分析了牛奶中的霉菌毒素,检出限为0.01~0.07 ng/mL。采用分子印迹聚合物(Mo⁃lecular imprinted polymer,MIPs)作为吸附剂,可实现模板分子及其类似物的选择性吸附。Samanidou等[39]将氯霉素印迹溶胶-凝胶二氧化硅基无机聚合物作为SPE吸附剂,用于牛奶中氯霉素的分离富集,其最大印迹因子为9.7。离子印迹聚合物(Ion imprinted polymer,IIP)具有离子选择性识别能力,但直接用于生物样品时表面会吸附大分子,将IIP与限进材料结合[40]可以解决该问题。
1.2.2 固相微萃取 固相微萃取(Solid-phase microextraction,SPME)装置由萃取头和手柄两部分构成,不需要溶剂,比LLE和SPE更环保,但SPME纤维的使用寿命有限,价格较高,且有样品残留问题。为了解决这些问题,近年来,越来越多的新型材料被用作SPME涂层,如共价有机骨架化合物(Covalent organic frameworks,COFs)、金属有机骨架化合物(Metal-organic frameworks,MOFs)、氧化石墨烯(Graphene oxide,GO)、MIPs等。
COFs结构多样、官能团丰富,且骨架结构便于调控,由于其疏水相互作用、π-π堆积和氢键相互作用,多用于芳族微污染物(如氯酚、双酚A和多环芳烃)的分离富集,很少用于非芳香族微污染物的萃取。Sun等[41]合成了三氟甲基COF作为SPME涂层,结合UHPLC-MS/MS检测了牛奶和奶粉中的典型非芳族全氟和多氟烷基物质,检出限为0.1~0.8 pg/g。
MOFs具有超高的孔隙率、大的表面积和可调节的孔径和形状,可以极大地提高富集性能。Jiang等[42]将羟基改性的锆基MOF材料作为SPME涂层,结合GC-MS/MS检测了牛奶中的痕量多溴联苯醚,检出限低至0.15~0.35 ng/L。
GO具有高表面积、高稳定性以及良好的电化学特性,可以有效地提高MOFs材料的吸附能力和在水溶液中的稳定性[43],将GO与作为亲水性萃取相的淀粉结合,可从牛奶样品中萃取阿莫西林、氨苄青霉素和氯西林3种抗生素[44],结合高效液相色谱法进行测定,抗生素的检出限为0.8~1.5μg/kg。
具有分子识别位点的MIPs选择性高,也被广泛应用于SPME。Liu等[45]开发了MIP修饰的木质尖端SPME纤维,可直接从牛奶中富集痕量大环内酯类抗生素,富集因子(EF)为12~82倍。聚苯胺、聚吡咯以及聚噻吩的导电聚合物是另外一种有前景的SPME涂层材料,可以高效地萃取牛奶中的孕酮、泼尼松龙和雌二醇[46]。
1.2.3 搅拌棒吸附萃取与纤维相吸附萃取 与SPME纤维相比,搅拌棒吸附萃取(Stir bar sorptive extraction,SBSE)具有更高的萃取能力,可减少竞争性吸附并能在搅拌的同时实现萃取富集[47],将各类碳基材料、MIPs等功能材料[48]用作搅拌棒萃取介质可提高其吸附性能。如Zhu等[49]采用MIP搅拌棒萃取奶粉中的三聚氰胺,发现其富集能力是非印迹搅拌棒的3倍。
纤维相吸附萃取(Fabric phase sorptive extraction,FPSE)是将杂化的有机-无机材料通过强共价键化学结合到具有溶胶-凝胶活性的底物表面,形成的一种高灵敏、快速的微萃取方法。该法可以直接将装置浸于乳制品样品内萃取青霉素[50],简化了蛋白质沉淀和溶剂蒸发步骤,大大减少了有机溶剂的使用。
1.2.4 磁性固相萃取 磁性固相萃取(Magnetic-solid phase extraction,MSPE)以功能材料包覆的磁性微粒或纳米粒子为分离介质,通过施加外部磁场将吸附有目标组分的磁性材料从样品溶液中分离出来[51],无需离心或过滤等步骤,简化了流程、减少了目标物损失。四氧化三铁(Fe3O4)是最常用的磁核[52]。Yavuz等[53]合成了核-壳型Fe3O4聚多巴胺纳米颗粒,用于牛奶样品中铜的MSPE萃取,其EF为150。与核壳结构不同,Liu等[54]制备了Fe3O4@石墨碳材料,然后将Fe3O4蚀刻形成带有腔体的蛋黄壳型材料。这种蛋黄壳型材料具有更高的比表面积和吸附位点,内部腔体大小可通过蚀刻时间控制,萃取效率高,牛奶中4种痕量磺酰胺抗生素的富集倍数可达35.1~36.8倍。
碳纳米管(Carbon nanotubes,CNTs)等碳材料、聚乙二醇等在MSPE中得到了广泛应用。如硫醇功能化的磁性CNTs可快速富集牛奶中的磺酰胺抗生素,萃取时间仅需2 min[55]。聚乙二醇(Polyethylene glycol,PEG)可以提高材料在水相中的分散性,并抑制颗粒聚集成胶束,经PEG改性后,磁性CNTs在介质中的稳定性和均一性显著提高[56]。
1.2.5 QuEChERS方法 QuEChERS(Quick,Easy,Cheap,Effective,Rugged,Safe)是水果和蔬菜等样品中农药残留的常规前处理方法,其常用的吸附剂有乙二胺-N-丙基硅烷、C18、石墨化炭黑[57]等。Hamed等[58]开发了一种名为Z-Sep+的新型分离介质,可有效避免亲脂性农药的前处理损失,在高脂干酪中的氨基甲酸酯残留分析中得到了成功应用。一般来说,QuEChERS简单快速,更适合乳制品样品的多残留分析,但其方法灵敏度较其他前处理方法低,从复杂基质中提取痕量分析物时需要结合其他萃取方法[59]。
1.3 其他前处理方法
除了常用的相分配或相吸附样品前处理方法外,一些免疫分离方法和微全分离方法也在乳制品有害物质分离富集中得到应用。
免疫亲和色谱(IAC)选择性和富集效果好且可再生使用,多用于农兽残及真菌毒素的净化和富集[60]。而免疫磁分离(Immunomagnetic separation,IMS)选择性高、设备简单,无需进行细胞培养即可富集细菌,适合现场检测的样品前处理。Srisa-Art等[61]基于免疫磁分离,采用沙门氏菌抗体包被的磁珠从全脂牛奶中捕获和分离鼠伤寒沙门氏菌(图1),并在比色纸基分析装置上分析,检出限为103CFU/mL。该方法对鼠伤寒沙门氏菌具有高度选择性,可以避免大肠杆菌等的干扰。

图1 全脂牛奶中鼠伤寒沙门氏菌的IMS过程[61]Fig.1 IMS process of Salmonella typhimurium in whole milk[61]
微全分析系统(Micro total analysis system,μ-TAS)具有体积小、便携、成本低以及易与各种类型的设备集成等多种优势,固相萃取、液相萃取等样品前处理手段均可在微全分析芯片上集成。Zhao等[62]将上样、提取、免疫亲和富集、磁分离和直接电喷雾电离质谱分析进行在线洗脱的过程集成到同一平台中(图2),研制了免疫亲和微流控芯片。该微流控芯片实现了样品分离、富集和分析检测的全自动化,可用于在线直接分析牛奶样品中的喹诺酮,检出限为0.047~0.490 ng/mL。
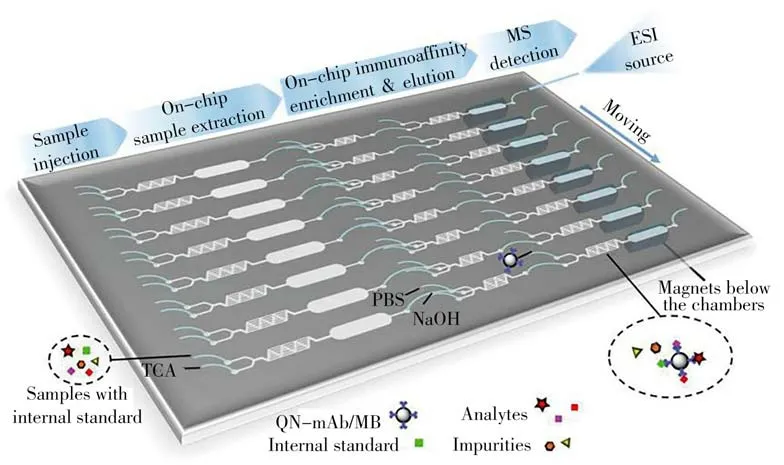
图2 高度集成的免疫亲和微流控芯片和质谱平台[62]Fig.2 An highly integrated immunoaffinity microfluidic chip and mass spectrometry platform[62]
2 乳制品中有害物质分析检测技术研究进展
2.1 实验室检测方法
实验室检测方法是指利用实验室仪器设备对样品实现分析检测的方法,方法灵敏度高、准确性好、结果可靠,能够进行低至痕量的定量分析实验,见表2。通常,能在2 h内出具检测结果的实验室检测方法即可视为实验室快速检测方法,但这个时间不能满足乳制品现场检测的需求。

表2 乳制品中有害物质分析检测方法比较Table 2 Comparison of laboratory testing methods for harmful components in dairy products
2.1.1 色谱法 气相色谱法灵敏度高、分析速度快、样品量少,是乳制品中挥发性有机化合物分析的通用方法,可同时对多种挥发性有机化合物进行鉴定。国内外乳制品检测标准中有机氯农药残留[74-75]、三聚氰胺[76]、硫氰酸钠[77]的检测方法均为气相色谱法。与质谱检测器联用后,色谱法的灵敏度将进一步提升。Cui等[78]采用气相色谱-质谱法同时检测了多类乳制品中的4种糠醛类化合物,检出限低至0.002~0.02 mg/kg。
高效液相色谱法主要用于乳制品中抗生素、农残、兽残等有害成分的分析检测。食品安全国家标准采用液相色谱-质谱法分析乳制品中多种氨基甲酸酯类农药残留[79]。Kaufmann等[80]采用高分辨率四极杆质谱与色谱联用,排除了样品中杂质产生的信号干扰,能同时检测含量为1μg/kg的8种硝基呋喃类药物残留。
2.1.2 原子光谱法 原子光谱法是乳制品中重金属元素检测的国家标准方法[81]。其中,石墨炉原子吸收光谱被广泛应用于乳制品样品中微量元素与重金属元素如铬、铅、镉[82-83]等的检测。电感耦合等离子体原子发射光谱法能大大减轻传统火焰原子发射法造成的自吸现象,Nascimento等[84]采用ICPAES同时检测了乳制品中的K、Na、Ca、Mn等多种元素,检出限范围为0.009~2.787μg/L。
原子荧光光谱法分辨率高、速度快、检测限低、线性范围宽。Costa Ferreira等[85]使用原子荧光法检测乳制品中的锑。该方法通过半胱氨酸将锑(Ⅴ)还原为锑(Ⅲ)后,用柠檬酸作为锑(Ⅴ)的掩蔽剂测定锑(Ⅲ),检出限低至0.07μg/L。
2.1.3 电化学分析法 电位分析法[86]、伏安法、电化学阻抗谱法[87]等电化学分析法因灵敏度高、仪器简便、分析速度快的优点,在乳制品检测中被广泛应用。Wong等[88]以方波伏安法实现了对多种乳制品中阿莫西林抗生素的检测,检出限为18μg/L。El-Shahawi等[89]通过间接微分脉冲伏安法检测牛奶中的三聚氰胺,采用预阳极氧化玻碳电极增强三聚氰胺的电化学响应,检出限为0.075μg/L。
对电极进行化学改性,可进一步提高电化学检测传感器性能。如H2O2在裸电极上的还原或氧化电位较大,用硫堇和镍的铁氰化物对电极进行表面改性后,可降低H2O2的反应电位[90],检出限达0.557μmol/L。Ali等[91]以二甲唑为模板分子制成结合分子印迹聚合物的改性电极,采用微分脉冲伏安法实现了对二甲唑的超灵敏检测,检出限低至0.1 nmol/L。
2.2 现场检测方法
现场检测方法是实验室常规检测方法的必要补充,通常,从样品处理到出具检测结果不超过30 min的方法可视为达到现场快速检测的要求。现场检测方法无需考虑乳制品采集和保存的问题,处理过程简单、快捷,比实验室检测方法更适用于乳制品质量的现场快速筛查。
2.2.1 生物免疫法 免疫测定技术多用于检测有抗原抗体活性的物质如粘菌素、黄曲霉毒素[92]、赭曲霉毒素[93]等。我国出入境检验检疫行业标准中采用实时荧光PCR法快速筛查沙门氏菌阳性的乳制品样品[15]。现有研究表明,光纤-表面等离子体共振生物传感器[94]对牛奶中黄体酮的检出限可达0.5 ng/mL,而便携式光流控生物免疫传感器可重复使用200次以上[95],降低了黄曲霉毒素的分析成本。Gamella等[96]基于辣根过氧化物酶与青霉素结合蛋白的竞争免疫反应构建传感器,对牛奶中β-内酰胺抗生素的检出限为4.3 ng/mL。
电活性物质、荧光基团等功能团可以非常容易地被标记在DNA序列上并应用于免疫法检测,如基于DNA适配体的生物传感器检测氯霉素的检出限为0.03 nmol/L[97],这种传感器也能区分5种乳制品中的氨基苷类抗生素[98]。Fu等[99]构建了一种特异性识别三聚氰胺的电化学-DNA(E-DNA)传感器。如图3A所示,DNA与三聚氰胺特异性结合形成三联体结构作为荧光信号的开关。Li等[100]通过进一步调节该DNA链段与三聚氰胺的结合位点数量,提高了传感器灵敏度,实现了对μmol/L浓度级别的三聚氰胺的检测,如图3B所示。
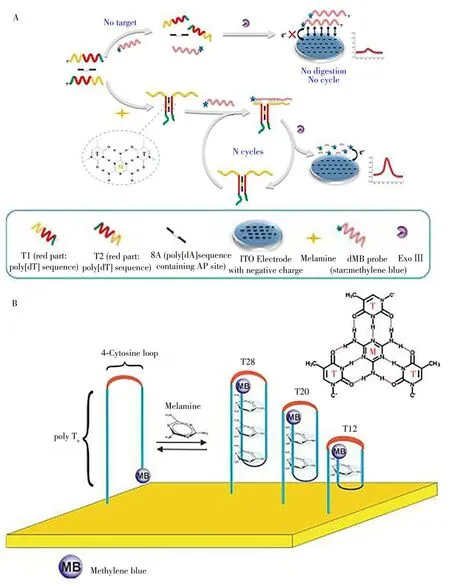
图3 基于DNA三联体结构的E-DNA传感器原理示意图(A)[99]与调节聚胸腺嘧啶片段(poly Tn)长度改变DNA三联体结构原理示意图(B)[100]Fig.3 Schematic display of E-DNA sensor based on DNA triplet structure(A)[99]and schematic display of DNA triplet structure by adjusting poly thymine fragment(poly Tn)length(B)[100]
2.2.2 分子光谱法 紫外-可见分光光度法(UV-Vis)作为最常用的分子光谱分析法,是现行国家标准[101]检测食品中锡含量的标准方法。国际标准[102]也通过测定柠檬酸盐吸光度实现干酪产品中柠檬酸类添加剂的检测。
荧光分析法(Fluorescence,FL)的检测灵敏度高,适用于乳制品中微量、痕量有害物质的定量分析。Li等[103]以钙钛矿复合材料作为探针测定三聚氰胺含量,三聚氰胺通过聚集诱导效应激活材料的荧光,检出限为0.42 nmol/L。Lin等[104]合成了光致发光性能优良的碳纳米颗粒用于构建荧光传感器,对牛奶中的卡那霉素进行分析,检出限低至5.0×10-8μg/kg。Orachorn等[105]构建了一种聚苯胺、氧化石墨烯和量子点复合的荧光探针,该探针具备了量子点的荧光性能、分子印迹聚合物的优异选择性以及氧化石墨烯和聚苯胺的高吸附亲和力,能快速检测牛奶中的洛美沙星含量,检出限为0.07μg/L。
红外光谱法通常不需要进行样品前处理,耗时少,效率高,且能实现多组分同时检测。Teixeira等[106]通过红外光谱和拉曼光谱获取物质成分信息,并经过主成分分析对牛奶样品中的多种抗生素残留进行鉴别。Balabin等[107]采用偏最小二乘回归法处理牛奶样品的近、中红外光谱数据,低成本检测出了乳制品中的三聚氰胺,检出限为0.76 mg/kg。
表面增强拉曼散射(Surface-enhanced Raman spectroscopy,SERS)较红外光谱的分析对象范围更广,同时对分析目标物的选择性更强。Li等[108]合成了一种核壳结构的金纳米球体材料用作SERS基底,该材料的表面等离子体共振效应能极大增强拉曼信号,实现对痕量四环素的快速检测,检出限为0.1μg/L。近年研究人员开发的微型热辅助清洗捕集器[109]、小型阵列气膜分离器件[110]等装置可以高效分离提取目标物,减轻分析样品对SERS基底的干扰。
化学发光法(Chemiluminescence,CL)耗时短且仪器操作相对简单,高向阳等[111]基于三聚氰胺对鲁米诺-高锰酸钾化学发光体系的抑制作用,用流动注射化学发光法检测牛奶中的三聚氰胺。Yao等[112]运用DNA探针特异性适配黄曲霉毒素B1(AFB1),探针捕捉目标分子后催化鲁米诺-H2O2发光反应,方法检出限低至0.2 ng/mL。
2.2.3 毛细管电泳法 毛细管电泳法分离效率高且占用空间体积小,开发操作简便、检测快捷的电泳芯片传感器是近年研究的热点。Bosma等[113]开发了一种使用荧光法检测环丙沙星的毛细管电泳芯片装置,可快速分离样品组分并提取纯化微流体通道内的分析物,从而实现环丙沙星的快速定性检测。Li等[114]基于电泳滴定原理构建微流体电泳芯片传感器,如图4所示,三聚氰胺对H2O2的竞争性反应可导致有色界面位移,进而实现目标物检测。
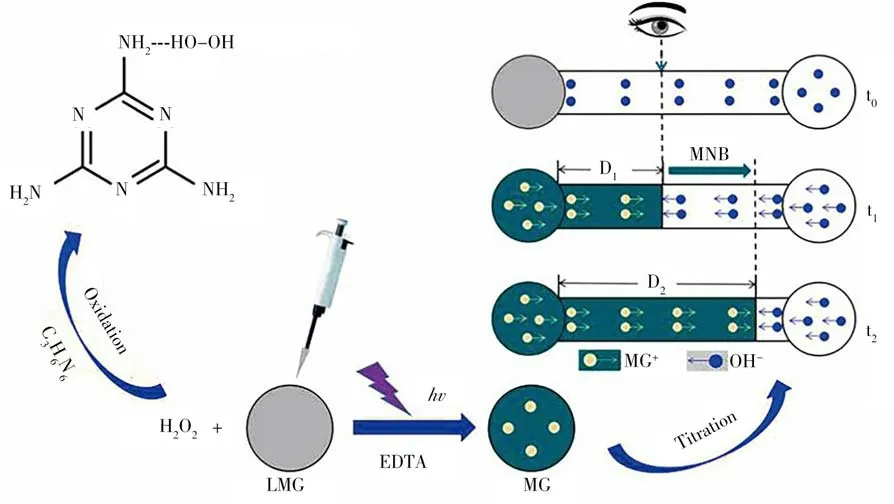
图4 微流体电泳芯片传感器原理示意图[114]Fig.4 Schematic display of micro-fluid electrophoresis chip sensor[114]
3 总结与展望
本文主要介绍了乳制品样品前处理与分析检测技术的相关研究进展。对于乳制品有害物质的分析检测过程,开发更加快速、简便的样品处理方法是提升其效率的重要手段。虽然LLE和SPE是经典的乳制品前处理方法,但需消耗大量有机溶剂,对环境不够友好。LPME和SPME等能大大降低样品消耗以及有害溶剂的用量。多种前处理技术的联用也正得到发展,与单一的萃取技术相比,将多种萃取技术结合使用将得到更好的萃取效果。
现场检测手段的特异性强,操作快速、简便,对样品的前处理很少甚至不需要进行任何处理即可进行检测。经现场检测方法初步检测后认为存在安全问题的乳制品样品,再送实验室检验,既可确证检测结果防止假阳性出现,又充分节省了实验室检测资源,使两类方法的优势互补。由于乳制品基体复杂,现有的快检方法易受样品基体干扰,选择性不高,难以准确定量,导致“检不出、检不准、检不快”等瓶颈问题,制约着对食品中化学污染物的有效快速监管。因此,研发集分离、富集、检测于一体的高灵敏、高通量与智能化的绿色快速样品前处理新方法与技术产品,构建精准、灵敏的快速检测方法,研制配套试剂与设备,有望为乳制品等食品安全监管提供良好的技术支持。

