硅酸盐岩石中氧化亚铁量测定方法的改进
帅林阳,卜道露,成俊烨
(1.中国地质调查局应用地质研究中心,四川 成都 610036;2.中国地质大学(武汉),湖北 武汉 430074)
岩石分析的主要目的在于,从其组分的含量了解元素的集中、分散,研究岩浆的来源,阐明岩石的成因等地质问题。硅酸盐岩石的组分千差万别,可以说硅酸盐岩石分析是无机物分析领域中难度最大的化学分析[1-3]。其中FeO 的测定,大型仪器无法发挥作用,依然离不开化学分析法。测定硅酸盐岩石中的氧化亚铁,主要有重铬酸钾容量法、偏钒酸铵间接滴定法和1,10-邻二氮菲光度法[4-6],溶样方式为酸溶,主要有氟化钠-盐酸和氢氟酸-硫酸2 种溶样体系[10-11]。现在各实验室大都采用国家标准GB/T 14506.14—2010 方法进行亚铁的分析[7],具有良好的精密度和准确度,但国标方法是仅对操作步骤进行了简要介绍,未对部分关键影响因素,如电热板温度选择、加热时间和如何避免溶样时的氧化还原干扰等做明确,且该方法采用铂金作为溶样工具,大大增加了测试成本,不适合大批样品的测定。生产实践中,笔者遇到了测定结果偏低、溶液浑浊难判定滴定终点等问题,经过探索,对实验条件进行改进优化,建立了以硫酸、氢氟酸为溶剂,CO2氛围保护亚铁,于聚四氟乙烯坩埚中封闭溶样,用重铬酸钾滴定法测定氧化亚铁量的新方法,经过实际样品分析,该方法经济、准确、重现性好。
1 实验部分
1.1 标准溶液和主要试剂
重铬酸钾标准滴定液c(K2Cr2O7)=0.002 319 mol·L-1:称取0.682 5 g 预先经150 ℃干燥2 h 的基准重铬酸钾,溶解于水中,移入1 000 mL 容量瓶中,用水稀释至刻度,摇匀。
二苯胺磺酸钠水溶液(5 g·L-1),磷-酸混酸,硫酸亚铁铵溶液;饱和硼酸溶液,硫酸,氢氟酸,(1+1)硫酸,(5+95)硫酸,碳酸氢钠。(所用试剂均为分析纯,实验用水为去离子水)。
1.2 实验设备
电子天平(万分之一),25 mL 酸式滴定管,电热板,烧杯,聚四氟乙烯坩埚(50 mL)。
1.3 实验方法
根据氧化亚铁含量范围称取试样于50 mL 聚四氟乙烯坩埚中,加入一定量的碳酸氢钠,用少量水润湿,加入5 mL 氢氟酸,再加10 mL 近沸的(1+1)硫酸,盖上坩埚盖,加热煮沸10 min,取下,立即将坩埚放入预先盛有200 mL 含有25 mL 饱和硼酸的新煮沸的水中,加入15 mL 磷-硫混酸,2 滴二苯胺磺酸钠溶液为指示剂,用重铬酸钾标准滴定溶液滴定至稳定的紫色为终点。
随同测定样品空白2 份,取平均值记V0,FeO含量以%表示,计算公式如(1):
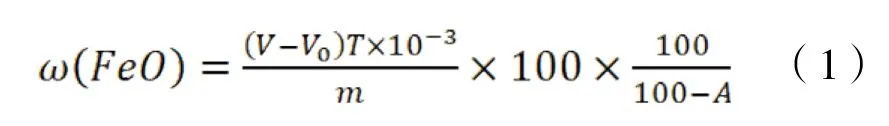
式中:V—试料消耗重铬酸钾溶液的体积,mL;
V0—空白消耗重铬酸钾溶液的体积,mL;
T—重铬酸钾标准溶液对FeO 的滴定度,mg/mL;
m—试料称样量,g;
A—试料吸附水的质量分数。
2 实验与讨论
2.1 溶样温度与时间选择
国标方法中未对溶样温度进行明确。若温度过低,达不到微沸状态,易导致溶样不充分。若温度过高,可能导致溶液过沸飞溅,不能达到准确的测量结果。聚四氟乙烯(PTFE)坩埚适用温度范围-200~250 ℃,加热温度不宜过高,否则易导致变形。有学者研究滴定法测定铁矿石中亚铁含量时,认为220 ℃为最佳[6]。考虑到硅酸盐岩石与铁矿石岩石组成有所不同,其最优的溶样温度应单独实验。以GSR-3和GSR-15为对象,对比了210、220、230 ℃的溶样条件下的滴定结果。其中230 ℃便出现了试样沸腾溅出的情况,故不再试验240 ℃及以上温度。从表1 结果判断,在220 ℃下溶样测试效果更好。

表1 溶样温度对测定FeO 的影响
由于封盖溶样,无法观察坩埚内是否已沸腾,不能确认从何时开始微沸10 min。而用氢氟酸-硫酸分解样品,长时间的加热应当避免,否则发生氧化反应:

尤其在大量氟离子存在下,亚铁更易氧化[8]。实验研究了10、12、15 min 溶样时间下的测定结果,从表2 可知,加热12~15min 样品已溶解完全,实验选择12~13 min 为溶样加热时间。

表2 溶样时间对测定FeO 的影响
2.2 碳酸氢钠用量选择
测定铁矿石中亚铁含量时,常用加入碳酸氢钠的方式保护亚铁不被氧化。加入酸后,碳酸氢钠与酸反应迅速在底部产生二氧化碳,实现将空气赶走的目的。溶解铁矿石样品时,有人认为用量2 g 效果更好,也有人认为对于300 mL 的锥形瓶,1 g 碳酸氢钠用量足够[4-5]。铁矿石分析方法对于硅酸盐岩石样品分析有一定参考意义,研究对比了0.5 g、1 g碳酸氢钠用量下的滴定结果,结果表明对于50 mL中聚四氟乙烯坩埚,0.5 g 用量足够。
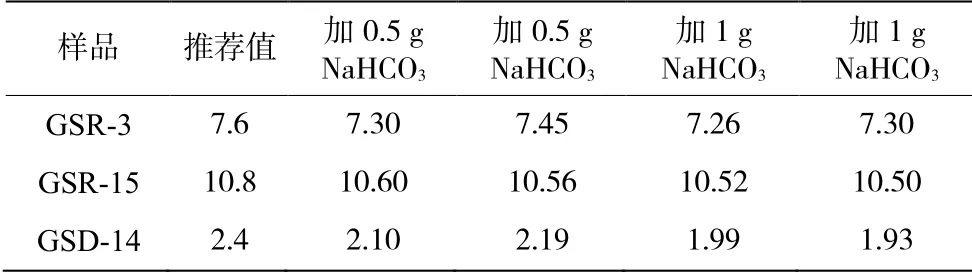
表3 碳酸氢钠用量的选择
2.3 酸用量选择
氢氟酸浓度大时,虽有利于试样分解,但由于氟离子与三价铁离子能生成稳定配合物而促进亚铁氧化,因此氢氟酸的用量不宜过大[8]。实验表明,采用国标方法,5 mL 氢氟酸和10 mL(1+1)硫酸,可充分分解试样。
2.4 滴定剂的用量
按照国标方法,每次加2 滴指示剂,但是当样品中有机质含量高时可使分解后的溶液带色,导致滴定终点难以判断,通过实验发现,加滴2 滴二苯胺磺酸钠可使滴定终点的颜色突变更加明显。指示剂本身具有氧化还原性质,会消耗重铬酸钾,加入量应保持一致。笔者建议样品和空白中均加4 滴指示剂。
2.5 溶样器皿的清洗
从经济角度考虑,PTEF 坩埚应清洗干净重复使用。实验发现溶样后,坩埚内壁易附着一些黑色物质,难以洗去。50%硝酸浸泡过夜、王水浸泡过夜和洗衣粉清洗的方法,均难以洗除。可用弱碱性肥皂水将黑色附着物洗净。
2.6 主要干扰组分及消除方法
主要有2 种组分对硅酸盐中FeO 的测定存在干扰:硫化物和高价锰。硫化物主要在黄铁矿中存在较多,在样品分解同时放出硫化氢,可将3 价铁还原为亚铁,导致亚铁结果偏高。当硫化物量大时,可加入 4%氯化高汞溶液使硫化物形成难溶复盐HgS·HgSO4,减轻其影响[8]。火成岩中,锰多以二价状态存在,对亚铁的测定无影,但在沉积岩中常见锰的高价氧化物,尤其是MnO,大量高价锰会在溶样时将亚铁氧化,使结果偏低,可用盐酸羟胺作为高价锰的选择性溶剂,减轻其影响[10]。一般硅酸盐岩石中,硫化物和锰量甚低,其干扰常可忽略。在6个不同国家标准物质的检测中,干扰元素对FeO 的测定基本无影响。
2.7 重复限性数据
为验证优化后方法的可靠性,笔者选取岩石、土壤、水系沉积物标准物质各两种,每种标准平行6 份,进行了检测。结果见下表,36 个分析结果有1 个超出重复性限,合格率 97%,满足《GB/T 14506.14—2010》的重复性限要求[5]。
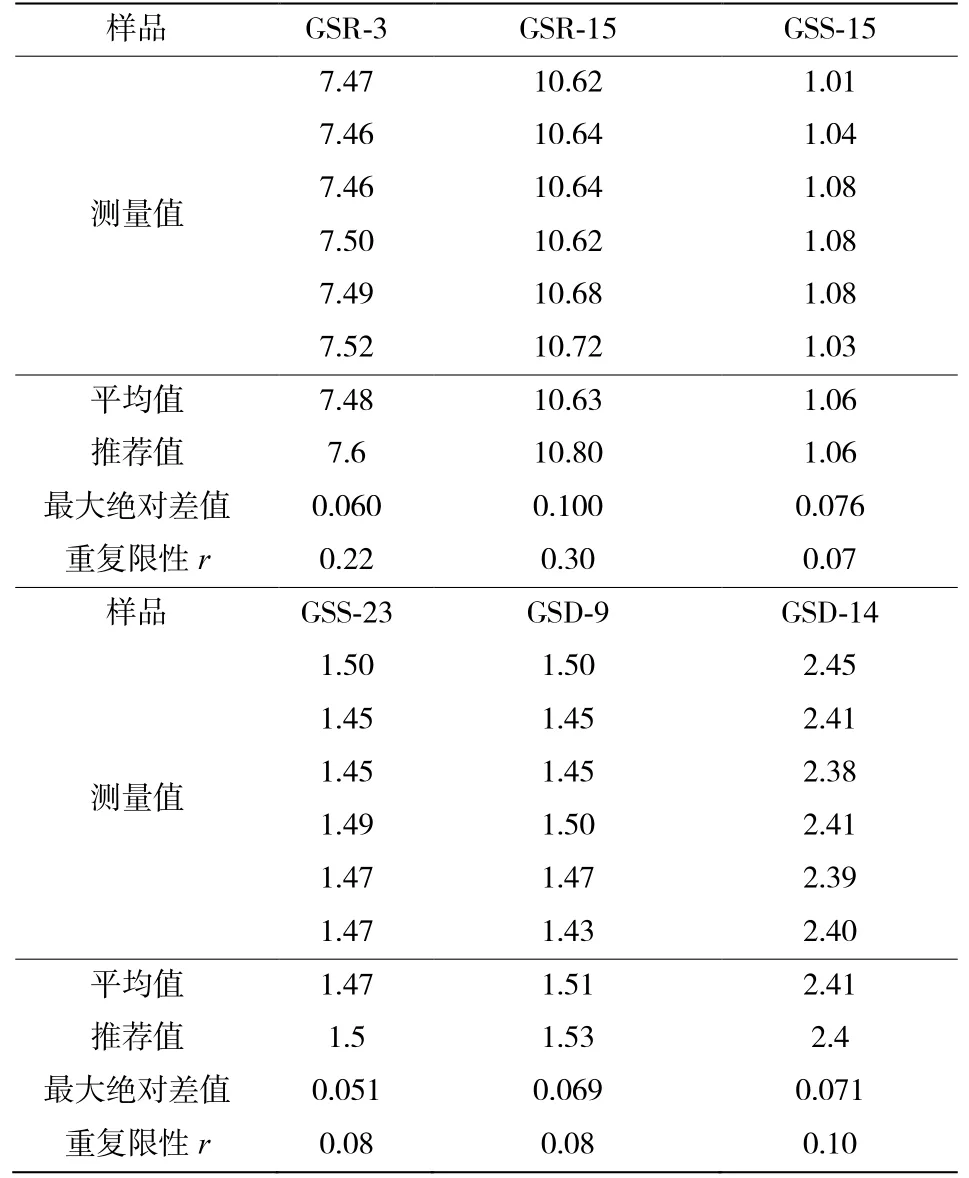
表4 实际样品中FeO 测定结果重复限性数据
根据《DZ/T 0130.3—2006 地质矿产实验室测试质量管理规范·第三部分:岩石矿物样品化学成分分析》[11],分别计算准确度要求YB、精密度要求YC。分析结果均能满足规范的准确度和精密度要求,数据见表5。
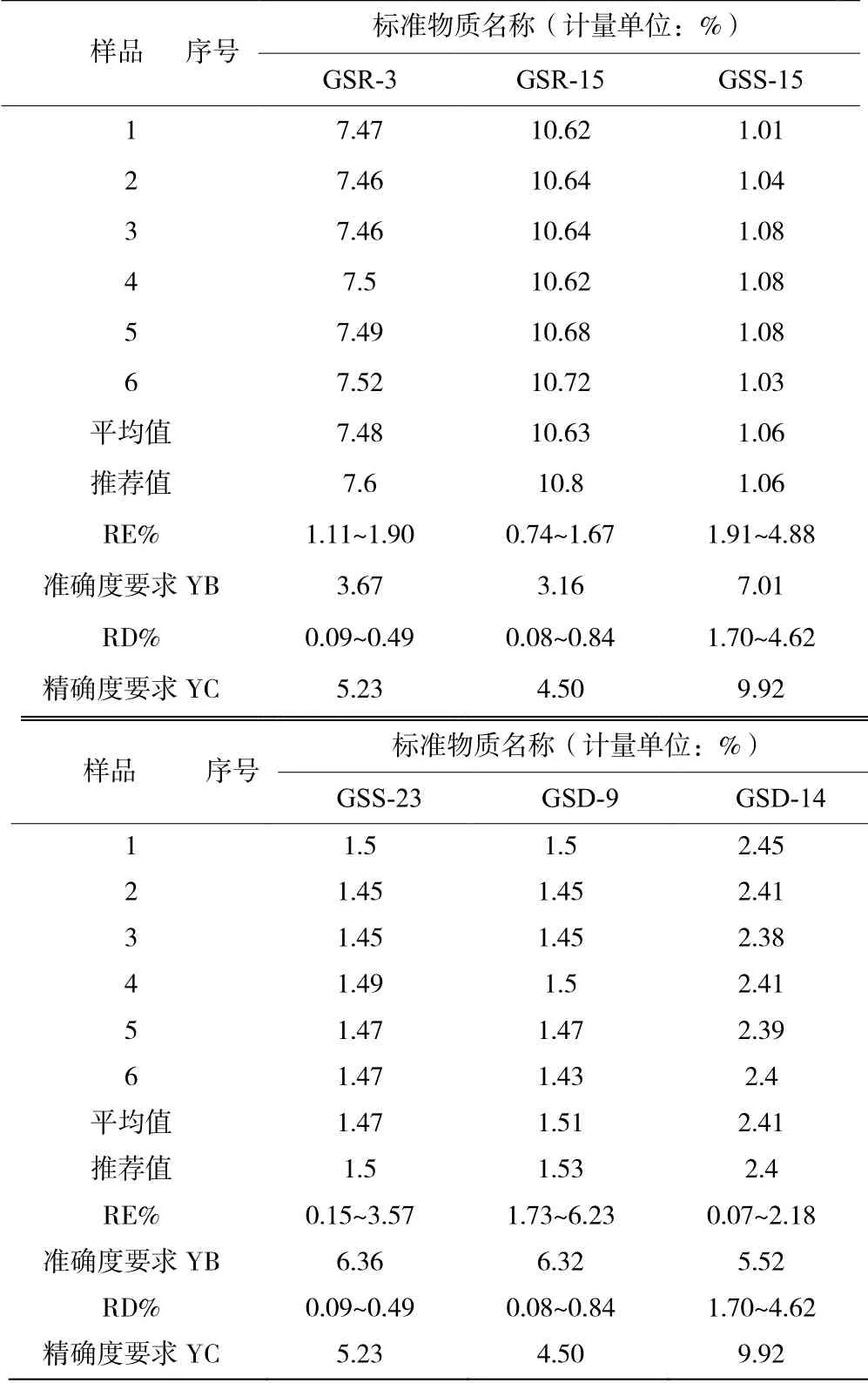
表5 实际样品中FeO 测定结果的精密度准确度
3 结论
对重铬酸钾法测定硅酸盐中亚铁量的国标方法进行了改进,优化了溶样温度、时间和防止氧化的措施,且不需要再铂金坩埚中进行溶样,更加经济。
经过实际样品分析验证,该方法准确性和精密度较好,不仅适用于硅酸盐岩石样品,对土壤和水系沉积物样品同样适用,可用于大批量生产分析。

