晚期胃癌患者联合给予化疗与贝伐珠单抗疗法的临床研究
王凤
单县东大医院肿瘤科,山东单县274300
现阶段临床针对晚期胃癌所采取的常规方案即化疗,但长此以往患者机体无法耐受,加之化疗药物毒副作用的影响,往往无法实现预期治疗目标[1-2]。贝伐珠单抗作为一种血管内皮生长因子重组人源化单克隆IgG1抗体,可以避免血管内皮生长因子结合血管内皮表现受体,从而阻断肿瘤血管内皮细胞的有丝分裂,同时作为新型抗肿瘤药物,可借助分子靶向方式有效抗肿瘤[3]。该次为探讨其临床应用价值,将2018年1月—2020年1月设为研究节点,期间该院收治的50例晚期胃癌患者作为研究病例,根据患者入院日期奇偶性以及个人意愿分作两组,通过化学药物疗法、化学药物联合贝伐珠单抗疗法展开研究,对比分析两组患者的治疗总有效率、治疗前后血清肿瘤标志物水平以及毒副反应发生情况,现报道如下。
1 资料与方法
1.1 一般资料
选取该院收治的50例晚期胃癌患者作为研究病例,纳入标准:①胃镜活检为胃癌,且TNM分期介于Ⅲb~Ⅳ期者;②KPS评分超过60分者;③预计生存周期不低于3个月者;④本人及(或)家属对该研究知情授权者。排除标准:①合并器官功能衰竭、凝血功能障碍者;②该研究之前接受姑息性化疗者;③脑转移者;④合并其他恶性肿瘤疾病者;⑤研究用药禁忌者等。
该研究由医学伦理委员会审核批准,根据患者入院日期奇偶性以及个人意愿分作两组,即对照组(25例),研究组(25例)。对照组男17例,女8例;年龄29~76岁,平均(52.65±7.21)岁。研究组男16例,女9例;年龄29~78岁,平均(53.18±7.37)岁。分析两组患者基础资料,差异无统计学意义(P>0.05),研究满足开展要求。
1.2 方法
对照组院内给予化学药物治疗(FOLFOX化疗方案):患者入组第1天,取85 mg/m2的奥沙利铂(国药准字H20093473)给予患者静脉滴注,持续2 h;第1~2天,取200 mg/m2的亚叶酸钙(国药准字H14022465)给予患者静脉滴注,持续2 h,完成滴注后取400 mg/m2的氟尿嘧啶(国药准字H21024236)给予患者静脉推注,然后取600 mg/m2的氟尿嘧啶对患者行持续静脉泵入治疗,持续22 h。
研究组院内基于对照组疗法另行贝伐珠单抗治疗:第1天取7.5 mg/kg的贝伐珠单抗(国药准字S20170035)对患者行静脉滴注治疗。
两组患者均以3周为1个疗程,共治疗3个疗程。
1.3 观察指标
①记录并对比两组患者的治疗总有效率,判定标准如下:经治疗病灶消失且持续时间超过4周为显效;经治疗病灶未消失但不存在新病灶,肿瘤最大垂径乘积下降幅度超过50%,持续时间超过4周为有效;经治疗未满足上述两个条件为无效。总有效率=(显效例数+有效例数)/总例数×100.00%[4]。
②通过电化学发光免疫法检测并对比两组患者治疗前后的血清肿瘤标志物,即糖类抗原19-9(CA199)与癌胚抗原(CEA)水平。
③记录并对比两组患者的毒副反应发生情况,包括恶心呕吐、血小板减少、白细胞减少、血红蛋白减少、周围神经毒性、肝肾功能障碍等。
1.4 统计方法
采用SPSS 19.0统计学软件进行数据分析,计量资料以(±s)表示,组间比较进行两独立样本t检验;计数资料以频数和百分比(%)表示,组间比较进行χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗总有效率对比
研究组的治疗总有效率为88.00%,相比对照组的60.00%,数据优势显著,差异有统计学意义(P<0.05)。见表1。

表1 两组患者治疗总有效率对比Table 1 Comparison of the total effective rate of treatment between the two groups of patients
2.2 两组患者治疗前后血清肿瘤标志物水平对比
治疗前两组患者的血清肿瘤标志物水平基本等同,差异无统计学意义(P>0.05),治疗后研究组的CA199、CEA水平明显低于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者治疗前后血清肿瘤标志物水平对比(±s)Table 2 Comparison of serum tumor marker levels before and after treatment between the two groups of patients(±s)
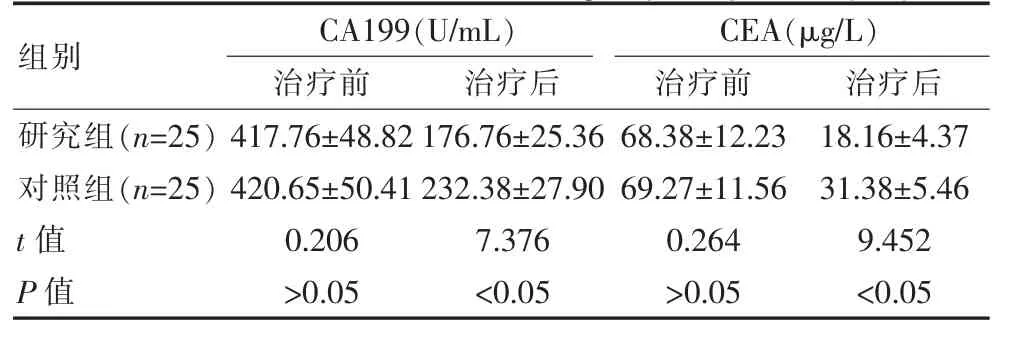
表2 两组患者治疗前后血清肿瘤标志物水平对比(±s)Table 2 Comparison of serum tumor marker levels before and after treatment between the two groups of patients(±s)
?
2.3 两组患者毒副反应情况对比
研究组患者出现毒副反应的概率低于对照组,差异有统计学意义(P<0.05)。见表3。
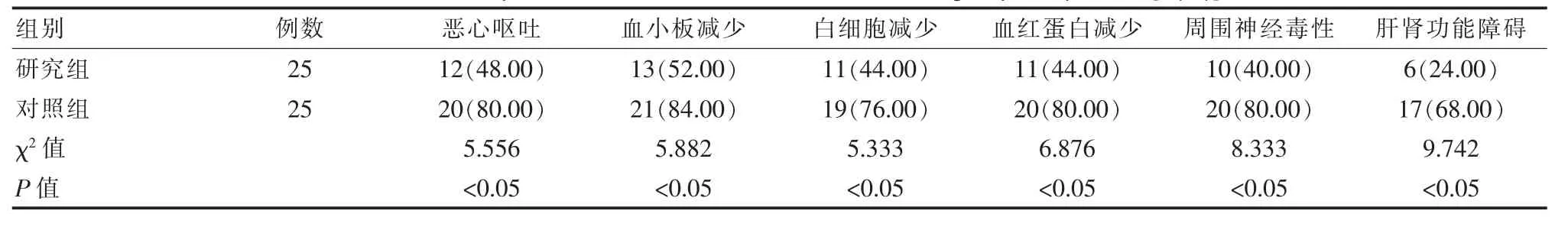
?
3 讨论
该次为探寻临床效益更为显著的治疗方案,以该院收治的50例晚期胃癌患者作为研究病例,通过对比FOLFOX化疗方案、FOLFOX化疗联合贝伐珠单抗方案展开对比分析,结果显示,研究组的治疗总有效率为88.00%,相比对照组的60.00%而言,数据优势显著(P<0.05);治疗后研究组的CA199、CEA水平(176.76±25.36)μ/mL、(18.16±4.37)μg/L明显低于对照组(P<0.05);此外,研究组患者出现毒副反应(恶心呕吐48.00%、血小板减少52.00%、白细胞减少44.00%、血红蛋白减少44.00%、周围神经毒性40.00%、肝肾功能障碍24.00%)的概率低于对照组(P<0.05)。这与许震等[5]的研究结果:治疗后试验组的CA199(157.31±5.93)U/mL明显低于对照组(231.59±9.04)U/mL(P<0.05),基本一致,可见联合用药可以进一步消除晚期胃癌患者的血清肿瘤标志物,且安全性更为可靠。
原因分析,贝伐珠单抗作为一种血管内皮生长因子重组人源化单克隆IgG1抗体,可以避免血管内皮生长因子结合血管内皮表现受体,从而阻断肿瘤血管内皮细胞的有丝分裂,同时对现存肿瘤血管进行破坏,减少肿瘤血管数量,避免继续向肿瘤组织供氧、供血[6-10];除此之外,该药物对肿瘤血管退化也有较好的促进作用,由此可以对肿瘤细胞供养途径进行切断,导致患者的肿瘤血管逐渐向正常化发展,促使肿瘤组织之间的渗透压逐渐下降,最终避免肿瘤细胞向远处发生转移[10-12]。由此可见,针对晚期胃癌患者,临床联合给予化学药物与贝伐珠单抗疗法,可以促使药物更好在肿瘤组织、细胞间发挥作用,避免肿瘤细胞进一步生长,在实现抗肿瘤治疗目标的同时,患者出现毒副反应的风险性相对较低,值得临床推广应用。
综上所述,晚期胃癌患者联合给予化学药物与贝伐珠单抗疗法可以有效降低血清肿瘤标志物水平,有利于患者获取更好的治疗效果,而且出现毒副反应的情况相对较少,安全性更为可靠。

