Forns指数、FIB-4、APRI、GPR对HBV感染合并非酒精性脂肪肝病患者肝纤维化的诊断效能分析
王燕芳,赵 杰,周少英,师艳艳
统计报道,全球慢性乙型肝炎病毒(HBV)携带者逾2亿人,其中我国慢性HBV感染人数约占1/3[1]。HBV感染可引起肝纤维化,最终可导致肝硬化及肝细胞癌[2]。一般认为肝纤维化及早期肝硬化若能得到及时有效干预病情存在可逆性,故早期确诊肝纤维化尤为重要[3]。目前肝穿刺病理检查系诊断肝纤维化的金标准,但存在有创性,且有一定的取样误差,患者可接受度低[4]。而影像学筛查虽可显示肝纤维化病灶特点,但对早期肝纤维化不敏感,尚无法替代病理检查[5]。肝纤维化血清分子生物学诊断目前缺乏统一标准,且肝纤维化病理过程复杂,单个血清标志物受其他因素干扰大,准确性不稳定[6]。现今认可度较高的无创肝纤维化诊断模型主要包括天冬氨酸转氨酶/血小板比值(APRI)模型[7]、Forns指数模型[8]等。近年也有报道指出,基于4因子的纤维化指数(FIB-4)模型适用于肝纤维化诊断与分期[9]。代倩等[10]认为,新型慢性乙型肝炎谷氨酰转移酶/血小板比值(GPR)模型可预测严重及晚期肝纤维化。故本研究旨在探究Forns指数、FIB-4、APRI、GPR无创模型诊断HBV感染合并非酒精性脂肪肝病(NAFLD)患者肝纤维化的效能。
1 资料与方法
1.1一般资料 选取2017年10月—2019年5月我院收治的HBV感染合并NAFLD 106例。入组标准:符合慢性HBV感染诊断标准[11],乙型肝炎病毒表面抗原(HBsAg)和(或)HBV DNA阳性≥6个月,属NAFLD;年龄≥18岁;有明确肝穿刺结果;临床及随访资料完善。排除标准:合并慢性阻塞性肺疾病等致外脏器官纤维化疾病者;肝穿刺前1周输注血液制品、行血液透析或服用影响凝血功能药物者;患酒精性脂肪肝病、药物性肝病、自身免疫性肝病、遗传代谢性肝病、血吸虫肝病、肝癌等全身恶性肿瘤者;合并人类免疫缺陷病毒感染、其他嗜肝病毒感染者;肝硬化失代偿期者;伴严重心、肺、肾疾病者;近6个月有苦参碱、甘草酸类、甾体激素类、核苷(酸)类药物服用史者;临床及随访资料缺失者。106例中男65例,女41例;年龄18~73(38.9±10.2)岁;HBV感染病程4~19(12.6±2.7)年;HBV DNA(6.51±1.32)lg copies/ml。
1.2肝穿刺活检 所有患者排除肝穿刺禁忌证后行肝穿刺活检,穿刺前排空膀胱,取左侧卧位,超声体表定位,常规消毒、铺巾,2%利多卡因逐层浸润麻醉,用16 G肝穿刺活检针在超声引导下垂直刺入肝包膜,避开大血管,快速完整取出2条2 cm长肝脏组织,多聚甲醛固定,送病理科检查,参照Metavir评分系统进行肝纤维化分期[12]。F0期:无纤维化;F1期:汇管区纤维性增大,但无纤维间隔形成;F2期:汇管区纤维性增大,少部分纤维间隔形成;F3期:多数纤维间隔形成,但未见硬化结节;F4期:大部分纤维间隔形成,见硬化结节。F0~F1期定义为非显著性纤维化,F2~F4期定义为显著性纤维化。
1.3实验室检查 入院次日所有患者抽取空腹外周静脉血,测定血清丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)、γ-谷氨酰转移酶(GGT)、总胆固醇(TC)、外周血小板计数(PLT)及HBsAg水平。并计算Forns指数、FIB-4、APRI与GPR。Forns指数=7.811-3.131×ln PLT(×109/L)+0.781×ln GGT(U/L)+3.467×ln年龄-0.014×TC(mg/dl)。FIB-4=年龄(岁)×AST(U/L)/[PLT(×109/L)×ALT(U/L)1/2]。APRI=[AST(U/L)/AST(ULN)×100]/PLT(×109/L)。GPR=GGT(U/L)/GGT(ULN)×100/PLT(×109/L)。
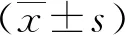
2 结果
2.1不同纤维化程度患者临床特点比较 106例肝纤维化分期F0~F1期76例(非显著组),F2~F4期30例(显著组),2组年龄、性别、吸烟史、饮酒史、家族肝病史、体质量指数(BMI)、病程、TC比较差异无统计学意义(P>0.05);显著组HBV DNA、ALT、AST、GGT均高于非显著组,PLT、白细胞计数(WBC)低于非显著组,差异有统计学意义(P<0.01)。见表1。

表1 不同纤维化程度的HBV感染合并非酒精性脂肪肝病患者临床特点比较
2.2不同纤维化程度患者Forns指数、FIB-4、APRI、GPR比较 显著组Forns指数、FIB-4、APRI、GPR均高于非显著组,差异有统计学意义(P<0.05,P<0.01),见表2。
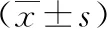
表2 不同纤维化程度的HBV感染合并非酒精性脂肪肝病患者Forns指数、FIB-4、APRI、GPR比较
2.3Forns指数、FIB-4、APRI、GPR预测HBV感染合并NAFLD患者显著性肝纤维化的效能分析 Forns指数、FIB-4、APRI、GPR中以GPR预测HBV感染合并NAFLD患者显著性肝纤维化的效能最高,其次为APRI,但4项联合诊断效能优于单独诊断,见表3与图1。
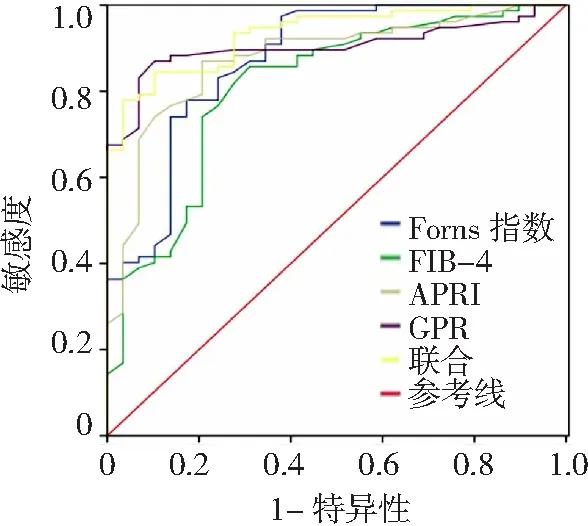
图1 Forns指数、FIB-4、APRI、GPR预测HBV感染合并NAFLD患者显著性肝纤维化的受试者工作特征曲线 FIB-4为基于4因子的纤维化指数,APRI为天冬氨酸转氨酶/血小板比值,GPR为谷氨酰转移酶/血小板比值,HBV为乙型肝炎病毒,NAFLD为非酒精性脂肪肝病
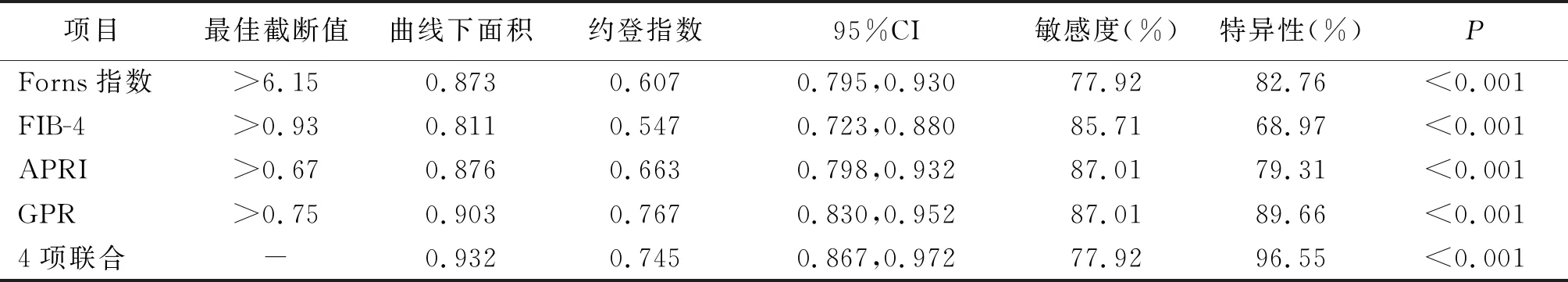
表3 Forns指数、FIB-4、APRI、GPR预测HBV感染合并NAFLD患者显著性肝纤维化的效能分析
2.4HBV感染合并NAFLD患者Forns指数、FIB-4、APRI、GPR与肝纤维化分级的关系 Spearman等级相关分析结果显示,HBV感染合并NAFLD患者Forns指数、FIB-4、APRI、GPR与肝纤维化分级均呈正相关(P<0.01),见表4与图2。
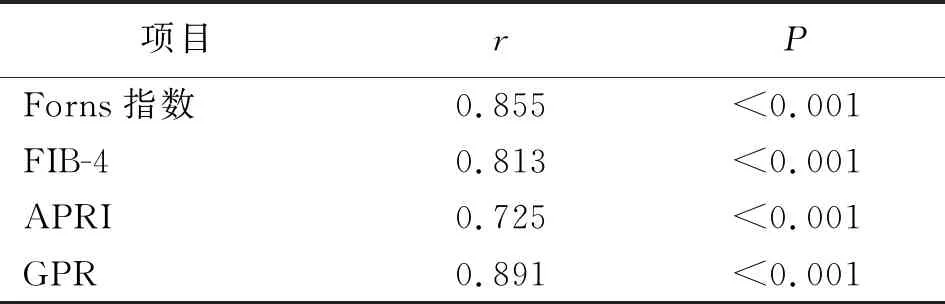
表4 HBV感染合并NAFLD患者Forns指数、FIB-4、APRI、GPR与肝纤维化分级的相关性分析
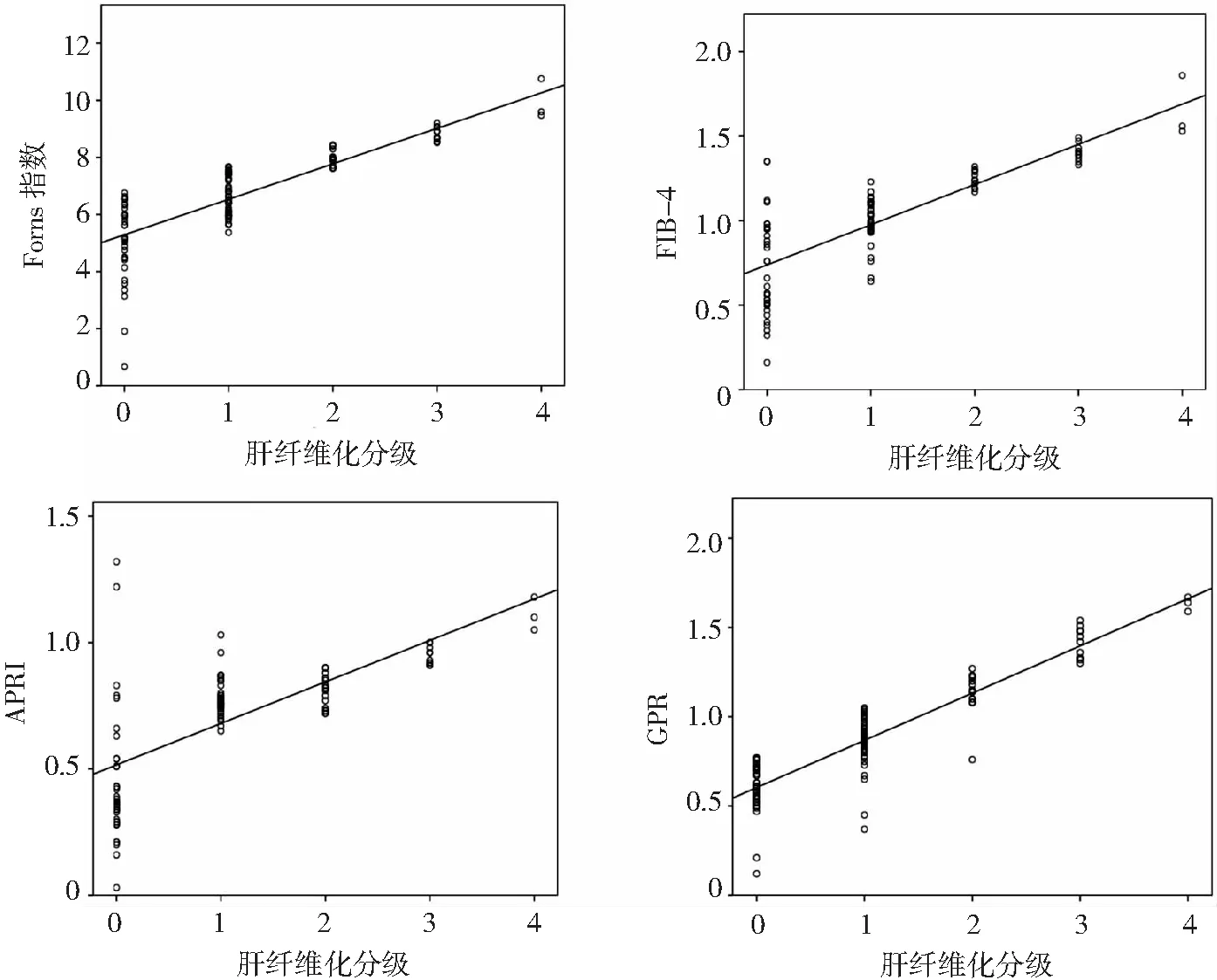
图2 HBV感染合并NAFLD患者Forns指数、FIB-4、APRI、GPR与肝纤维化分级的相关性散点图
3 讨论
NAFLD系病变主要分布于肝小叶,以肝细胞脂肪变性及脂肪堆积为病理特点,但大部分患者无过量饮酒史的临床综合征[13-17]。目前HBV感染合并NAFLD患者逐渐增多,越来越多的证据显示肝脂肪堆积可能加重肝纤维化进程[18-19]。目前肝纤维化评估主要通过影像学、病理检查、血清学及无创模型诊断等方式[20]。肝纤维化病理检查被认为是肝纤维化严重程度评估的金标准,但费用高、有创,且检查结果受病理采样及医生主观因素的影响,不适宜作为早期监测肝纤维化程度的方法[21]。而影像学筛查以超声为主,其操作简单、快捷、可重复性好、费用低廉,但对早期肝纤维化的诊断敏感度较低;超声弹性技术虽可提高肝纤维化检出率,但受肥胖、肝脏炎症程度、肝功能及胆红素等影响大,存在局限性[22]。单一血清标志物受各类因素干扰大,诊断价值不确切[23]。故为提高肝纤维化诊断准确性,多位研究者通过数学模型建立无创肝纤维化诊断模型,为肝纤维化分级提供了一定的理论依据[24-25]。
当前国内HBV感染患者肝纤维化程度评估常用诊断模型包括Forns指数、FIB-4、APRI等[26]。前期研究已证实FIB-4、APRI对各期肝纤维化均有较高的诊断敏感度[27-28]。桑潮等[29]研究发现,FIB-4不仅可预测丙型肝炎发病,还适用于乙型肝炎的诊断。且此两类无创模型仅需测定AST、ALT、PLT等数据,临床易获取,检测难度低[30]。但关于以上模型用于HBV感染合并NAFLD患者肝纤维化评估价值的研究鲜见报道。本研究按肝组织活检肝纤维化分级将患者分为非显著纤维化与显著纤维化,结果发现显著组HBV DNA、ALT、AST、GGT均高于非显著组,PLT、WBC低于非显著组,提示显著组HBV病毒载量更高,肝组织受损更严重,且伴血细胞计数明显异常,与张峰等[31]报道结果相似,提示通过以上指标建立无创肝纤维化诊断模型存在一定的科学性。同时我们还发现,显著组Forns指数、FIB-4、APRI均较非显著组高,提示以上3种模型均有助于HBV感染合并NAFLD患者肝纤维化分级。进一步行ROC曲线分析发现,以上3种模型中,以APRI预测HBV感染合并NAFLD患者显著性肝纤维化的效能最高,其次为Forns指数。Forns指数是以PLT、GGT、TC为依据计算肝纤维化程度的无创诊断模型,前期主要用于评估丙型肝炎病毒感染患者肝纤维化程度[32]。近年发现Forns指数对慢性HBV感染患者肝纤维化评估准确性较高[33]。FIB-4最早用于评定人类免疫缺陷病毒与丙型肝炎病毒重叠感染患者肝纤维化程度[34],近期被证实对NAFLD患者肝纤维化的诊断效能优于超声[35]。虽Forns指数较FIB-4预测显著性肝纤维化的效能高,但此模型计算公式复杂,难以在基层医院推广。而APRI模型中含AST与PLT指标,可排除由肝炎活动所致转氨酶水平异常升高引起的波动,较单纯肝功能指标预测更具科学性,更能准确评估肝纤维化程度。
GPR为近年来建立的新型无创肝纤维化评估模型,主要通过GGT与PLT评估肝纤维化程度,此2项指标已被证实与HBV感染患者肝纤维化进展有关[36]。本研究采用GPR模型预测慢性HBV感染合并NAFLD患者肝纤维化程度,结果发现显著组GPR明显高于非显著组,提示将其用于肝纤维化诊断具有科学性。进一步行ROC曲线分析,GPR预测显著性肝纤维化的效能较其他3种模型高,且与肝纤维化分级密切相关,随肝纤维化程度的加重,GPR逐渐升高,表明新型无创模型GPR有较高的临床应用价值,用于无创评估HBV感染合并NAFLD患者肝纤维化程度有较高的可行性。我们还发现Forns指数、FIB-4、APRI、GPR均与HBV感染合并NAFLD患者肝纤维化程度有关,随肝纤维化程度的加重,以上模型数值均升高,提示上述4种模型对肝纤维化病理改变均有较高的敏感度。此外,为验证联合模型预测肝纤维化是否存在增益效应,我们展开串联分析发现,Forns指数、FIB-4、APRI、GPR联合诊断可提高预测显著性肝纤维化的准确性。因此我们建议在单项模型无法确诊肝纤维化时可联合其他模型进行联合筛查,以提高肝纤维化检出率。
综上,Forns指数、FIB-4、APRI、GPR均可较好地预测HBV感染合并NAFLD患者显著性肝纤维化的发生,其中以GPR预测效能最高,4种检测模型与患者肝纤维化分级均有较高的相关性。但无创检查仍无法完全替代肝组织活检作为肝纤维化诊断的首选,故对无创模型单独或联合诊断仍无法确定是否存在肝纤维化的患者仍需行肝组织活检。

