茉莉酸处理对木本油料植物小桐子早期花序芽基因表达的影响
徐传佳,陈茂盛,徐增富,3*
(1.中国科学院西双版纳热带植物园,种子创新研究院,中国科学院热带植物资源可持续利用重点实验室,勐仑 666303;2.中国科学院大学生命科学学院,北京 100049;3.广西大学林学院和亚热带农业生物资源保护与利用国家重点实验室,南宁 530004)
茉莉酸 (jasmonic acid,JA)在植物花序、小花和雄器官发育过程中具有重要调控作用[1-2]。根据经典的Vick-Zimmerman途径[3-4],茉莉酸生物合成最初底物是α-亚麻酸 (α-linolenic acid,ALA),其由半乳糖脂经磷脂酶A1催化而成;磷脂酶A1包括DONGLE (DGL),DAD1(deffective in Anther Dehiscence1)和其他未被识别的脂酶[5]。ALA在一系列酶催化下转化成12-氧代植物二烯酸 [(9S,13S)-12-oxophytodienoic acid,OPDA]。这些酶包括脂氧合酶 (lipoxygenase,LOX),丙二烯氧合酶 (allene oxide synthase,AOS)和丙二烯氧化物环化酶 (allene oxide cyclase,AOC)。OPDA由过氧化物酶体ABC转运蛋白 (peroxisomal ABC transporter 1,PXA1)转运到过氧化物酶体,被OPDA还原酶 (OPDA reductase,OPR)还原成OPC-8:0,随后经过三步β氧化生成茉莉酸[6-7]。β氧化酶包括乙酰辅酶A氧化酶 (acyl-CoA oxidase,ACX),多功能酶 (multifunctional protein,MFP)和3-酮酯酰辅酶A硫解酶 (3-ketoacyl-CoA thiolase,KAT)组成[1]。
在拟南芥花药不开裂基因DAD1(defectiveinantherdehiscence1)突变体中,由于内源茉莉酸含量降低,花丝变短,花粉失活以及花药开裂缺陷,导致雄性不育[8-9]。kat2kat5双突变体表现出节间间距异常,花序长度缩短,以及花器官异位的表型[10]。在水稻 (Oryzasativa)中,与DAD1同源的基因EG1(EXTRAGLUME1)突变,会引起花分生组织决定缺陷,改变花器官数量,生成额外的类颖器官,导致小穗形态发生变化[11]。在玉米 (Zeamays)中,茉莉酸合成基因突变体ts1或opr7opr8均表现出穗状花序由雄蕊向雌蕊逆转表型,表明JA在玉米花性别决定上起着重要作用[12-13]。
在茉莉酸信号传递途径中,植物响应发育或环境信号,迅速合成具有生物活性的茉莉酸-异亮氨酸 (jasmonoyl-isoleucine,JA-Ile)[14-17]。F-box COI1(CORONATINE INSENSITIVE 1)蛋白感知JA-Ile后,募集不同的jasmonate-ZIM domain (JAZ)蛋白,经26S蛋白酶体使JAZ蛋白泛素化并降解[18-21]。JAZ蛋白降解会解除JAZ-NINJA-TPL(JAZ-NOVEL INTERACTOR OF JAZ-TOPLESS)复合物对JA响应基因的直接抑制,同时使得结合在这些响应基因启动子上的转录因子 (如MYC2)被释放,调节靶标基因的表达,从而调控植物生长发育和防御响应[19,22-23]。同时,COI1蛋白与SCF(Skp-Cullin-F-box)蛋白特异性结合,形成SCFCOI1蛋白复合体;此复合体通过结合靶向蛋白,调节转录响应,进而调控相应的生物学过程[24]。此外,作为JAZ蛋白的靶标,bHLH类转录因子中的IIIe亚群 (MYC2、MYC3、MYC4和MYC5)是茉莉酸信号通路中的正调控因子,IIId亚群 (JAM1、JAM2、JAM3和bHLH14)是负调控因子[9,25-28]。在水稻中,JAZ1与茉莉酸受体蛋白COI1b相互作用,引起茉莉酸信号抑制子JAZ1降解,启动茉莉酸信号,从而调控穗的发育[11]。拟南芥coi1突变体表现为雄性不育,而水稻OsCOI1 RNAi转基因植株的穗表型没有明显变化[29-30]。作为转录抑制子,拟南芥JAM1、JAM2和JAM3调控茉莉酸信号途径,它们的功能增强突变体雄性育性下降[31]。番茄中超量表达SlJAZ2基因引起植株早期叶片发生和开花时间提前以及株高和节间缩短[32]。茄子花药开裂相关基因SmDAD1的启动子与GUS基因在拟南芥中异源融合表达,展现出该启动子在根部、叶片和花药中的较强活性,且其受逆境和生长发育相关激素的诱导,暗示SmDAD1可能参与茄子发育和胁迫响应过程[33]。以上研究结果表明,在草本植物中,JA合成及信号途径在植物花发育中发挥着多样的功能,但是其在木本植物花发育中的调控作用却鲜有报道[2,32-34]。
小桐子 (Jatrophacurcas)是大戟科多年生木本油料植物,其种子含油率高 (30%~40%),是种很有潜力的可再生能源植物[35]。然而,小桐子是雌雄同株异花植物,雌雄花比例 (1∶13~1∶29)和种子产量低[36],限制其生产应用。因此,解析小桐子花性别决定的分子机制对小桐子遗传改良十分重要。前期通过对雄花退化的小桐子突变体与野生型植株花序的比较转录组分析,发现JA在小桐子花发育中可能发挥调控功能[37],然而其具体作用机制尚不清楚。现通过外源茉莉酸处理小桐子早期花序芽,分析JA对花发育及基因转录的影响,为进一步解析JA调控小桐子花发育的作用机制提供理论依据。
1 材料与方法
1.1 材料
三年生的小桐子种植于云南省勐腊县勐仑镇中国科学院西双版纳热带植物园苗圃 (北纬21°54′,东经101°46′;海拔580 m)。茉莉酸购于上海源叶生物科技有限公司 (Cat.No.JJ210510)。茉莉酸溶解在10%乙醇中配成10 mmol/L母液,储存在4 ℃备用,母液用10%乙醇稀释成不同浓度后使用。预实验结果表明,相比2.5 mmol/L和5 mmol/L茉莉酸处理,1 mmol/L茉莉酸处理小桐子花序芽,对花序芽无明显损伤,故选取该浓度作为处理浓度。于长势相同的小桐子上,选取出现1~7 d的花序芽 (图1)为实验材料[37],分别用1 mmol/L茉莉酸 (处理组ja1-3)和10%乙醇 (对照组ck1-3)喷施处理[38-39],24 h后取样,3~5个花序芽为一个生物学重复。采集的样品用液氮速冻,保存于-80 ℃备用。另外,用同样浓度的试剂和相同的处理方法,对同一发育时期的花序芽进行处理,连续处理3次,每次间隔1 d。25 d后,先对未完全开放小花的数量进行统计;待花完全开放后,再对花序进行形态学观察和雌雄花大小测定。

图1 出现1~7 d的小桐子花序芽Fig.1 The Jatropha inflorescence bud 1~7 days after emergence
1.2 方法
1.2.1 RNA提取和测序文库的构建
花序总RNA的提取采用文献中描述的硅胶吸附法[40]。用NanoDrop 2000分光光度计 (Thermo Scientific,Wilmington,DE,USA)测定RNA浓度,通过琼脂糖凝胶电泳鉴定RNA质量。用Agilent 2100 生物分析仪 (Agilent,Santa Clara,CA,USA)确认RNA的完整性,并通过Qiagen RNeasy kit (Venlo,Netherlands)试剂盒纯化RNA。选择RIN值 (RNA integrity number)大于7的RNA样品用于建库。建库测序由武汉菲沙基因信息有限公司DNBSEQ-G400 (MGISEQ-2000)平台完成。数据储存于国家基因库序列归档系统 (China Nucleotide Sequence Archive,CNSA),项目编号为CNP0001154。
1.2.2 转录组分析
Clean reads用Subread (version 1.6.2)软件 (http://subread.sourceforge.net/)比对到小桐子基因组,并进行基因丰度计算[41]。用edgeR软件进行差异表达基因 (differentially expressed gene,DEG)分析[42]。使用DAVID软件进行Gene Ontology (GO)和Kyoto Encyclopedia of Genes and Genomes (KEGG)的基因功能富集分析[43]。用pheatmap R软件包 (version1.0.7)(https://github.com/cran/pheatmap)完成基因的分层聚类。
1.2.3 实时荧光定量聚合酶链式反应(PCR)(qRT-PCR)
用Primer5.0软件对小桐子花序芽差异表达的候选基因设计qRT-PCR引物 (表1)。以cDNA为模板,以小桐子JcActin(GeneBank No.HM044307)基因为内参[44],参照SYBR©Premix ExTaqTMⅡ (Roche diagnostics)试剂盒说明书加样并在LightCycler480荧光定量PCR仪上进行目的基因片段的扩增。实验进行2次生物学重复和3次技术性重复。结果用2-ΔΔCT方法分析。

表1 qRT-PCR涉及的基因和引物Table 1 Genes and primers used in qRT-PCR
2 结果与分析
2.1 茉莉酸处理对早期花序芽中基因表达的影响
基于转录组测序数据 (表2),对处理和对照样品进行多维标度法 (multidimensional scaling)分析,其中一个对照样品 (ck3)出现偏离,去除后处理组与对照组能明显分开(图2),表明JA处理后,小桐子花序芽中的基因转录发生了明显变化。茉莉酸处理后,小桐子花序芽中一共1 954个基因被诱导表达,其中1 259个基因上调表达,695个基因下调表达[变化倍数≥2,错误发现率(false discovery rate,FDR)≤0.01](图3)。GO注释显示,在上调表达的DEGs中,主要富集“膜重要组分(integral component of membrane)”“质膜(plasma membrane)”“胞外区(extracellular region)”和“ATP(adenoisine-triphosphate)结合(ATP binding)”功能分类基因;在下调表达的DEGs中,主要富集“叶绿体(chloroplast)”“膜整体组分(integral component of membrane)”“膜类(membrane)”和“氧化还原过程(oxidation-reduction process)”功能分类基因(图4)。其中“响应茉莉酸(response to jasmonic acid)”功能分类基因出现在上调表达基因群中,表明在小桐子中,外施JA确实可以促进相应信号途径的基因表达。KEGG注释显示“次生代谢物生物合成(biosynthesis of secondary metabolites)”途径基因在上调和下调表达DEGs中都富集,说明外源JA可能影响小桐子花序芽中次生代谢物的合成 (图5)。

表2 小桐子花序芽转录组测序数据质量统计Table 2 Quality statistics of transcriptome sequencing data for inflorescence bud from Jatropha

ck1和ck2是对照样品的2个生物学重复;ja1、ja2和ja3是处理样品的3个生物学重复;BCV表示生物学变异系数图2 处理和对照样品关系分析Fig.2 Relationship analysis of sequencing samples based on multidimensional scaling
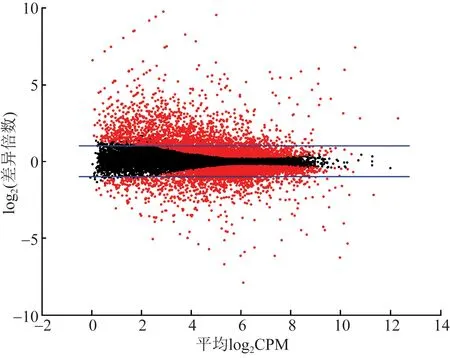
蓝线表示2倍差异表达的基因;红色点表示FDR小于0.01的差异表达基因;CPM表示每百万比对到某基因的读长数图3 小桐子花序芽中茉莉酸处理诱导的差异表达基因Fig.3 Differentially expressed genes (DEGs)induced by JA treatment in inflorescence buds of Jatropha curcas
2.2 成花转变、花器官发育以及茉莉酸合成和信号转导途径相关的DEGs分析
通过序列相似性比对,在差异表达基因中筛选到10个与成花转变相关的,8个与花器官发育相关的,8个与茉莉酸合成途径相关的和10个与茉莉酸信号转导途径相关的拟南芥同源基因(P≤ 0.05)(表3)。JA处理后,小桐子花序芽中,参与成花转变的7个基因上调表达,3个下调表达;参与花器官发育的1个基因上调表达,7个下调表达;参与茉莉酸合成途径的5个基因上调表达,3个下调表达;参与茉莉酸信号途径的8个基因上调表达,2个下调表达(图6)。其中,DAF(DAD1-ActivatingFactor)基因同时参与拟南芥茉莉酸合成和花器官发育过程[45],MYC4 (myelocytomatosisprotein4)基因同时参与拟南芥茉莉酸信号途径和成花转变过程[46-47],在小桐子花序芽中,其同源基因受JA诱导上调表达。在花器官发育相关的基因中,与拟南芥FUL、SRS、SEP1、AGL61、WOX1、TPR4和SEU同源的基因下调表达,说明JA处理可以诱导小桐子花器官发育相关基因的表达发生变化。为了验证转录组结果中候选基因的表达模式,选取2个成花转变相关基因(JcSPL4和JcSPL9)、4个花器官发育相关基因(JcFUL、JcSEP1、JcSEUSS和JcWOX1)和2个茉莉酸合成途径相关基因(JcFAD8a和JcFAD8b),进行qRT-PCR分析。结果(图7)显示,这些基因的表达模式与转录组分析结果(图6)相一致,表明转录组测序结果可靠。以上结果表明,外源JA处理可以诱导小桐子早期花序芽中JA合成和信号途径以及成花转变和花器官发育相关基因的表达,可能对小桐子花的表型产生影响。
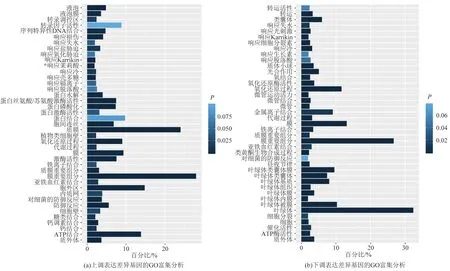
图4 茉莉酸诱导的差异表达基因的GO功能富集分析Fig.4 Enrichment analysis of GO of differentially expressed genes induced by JA treatment
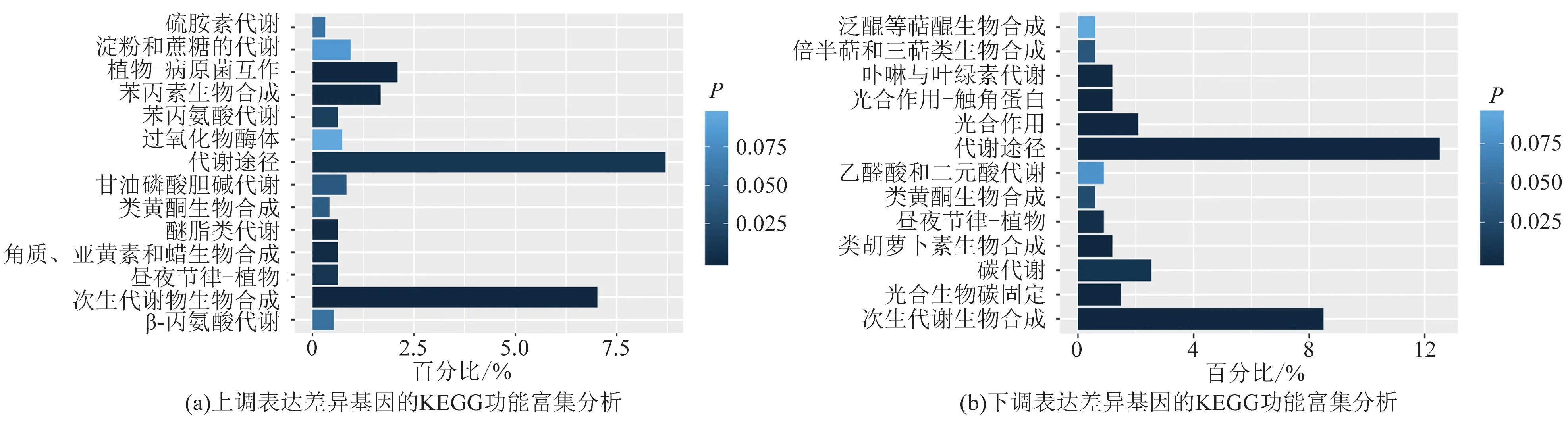
图5 茉莉酸诱导的差异表达基因的KEGG功能富集分析Fig.5 Enrichment analysis of KEGG of differentially expressed genes induced by JA treatment
3 讨论
茉莉酸生物合成和信号转导途径在花的发育过程中起着重要作用,参与拟南芥、水稻和玉米的花发育调控[13,30,69-71]。在小桐子中,不同花性别生态型小桐子比较转录组分析结果显示JA在小桐子花器官发育中可能发挥调控功能[37],且小桐子茉莉酸合成酶基因JcDAD1的沉默对花发育有明显的影响[72],但本研究结果表明外源JA处理并不显著影响花发育后期表型,表明小桐子的花发育对外源1 mmol/L JA处理不敏感。而外源茉莉酸甲酯(MeJA)可以促进油菜(Brassicanapus)开花,并且引起花器官形态的异常[73],表明JA调控不同植物花发育过程中的作用方式可能并不相同。
JA处理后,小桐子花序芽中,茉莉酸合成途径中的FAD7、FAD8、AOC4和OPR3基因下调表达(图6),表明内源JA合成受到抑制;而LOX2、LOX5、LOX6和AOS基因上调表达(图6),表明小桐子花序芽中可能存在反馈调节。JAZ蛋白是茉莉酸信号途径中的关键蛋白。JA处理后,JAZ1、JAZ2和JAZ8基因上调表达(图6),响应茉莉酸含量的增加,表明在小桐子花序芽中,JAZs基因的转录受JA正调控。在拟南芥中,JAM2和JAM3蛋白作为茉莉酸信号途径中转录抑制子,其负调控JA响应相关的胁迫响应、花的育性和叶片衰老等过程[74-75];在小桐子中,JAM2基因上调表达,JAM3基因下调表达,表明JAM2和JAM3在小桐子的花发育过程中可能有不同功能。MYC4是一个受茉莉酸激活的bHLH转录因子,拟南芥开花诱导上发挥重要功能[47]。DAD1催化茉莉酸合成途径中半乳糖脂 (18∶3)向游离的ALA的转变过程[7]。在小桐子花序芽中,MYC4基因[46-47]以及DAD1激活因子DAF[45]的同源基因表达均被上调,表明在小桐子中可能存在与拟南芥相同的茉莉酸生物合成和信号转导的调控途径。
KEGG功能富集分析显示“次生代谢物合成基因”途径基因在上调和下调表达DEGs中都富集(图5),与JA合成代谢途径中基因的表达 (图6)相一致,表明JA合成代谢途径基因在花发育过程中发挥作用。然而,KEGG并未富集JA信号转导途径和花发育相关基因,说明仅仅这些JA合成代谢途径基因的表达变化可能不足以引起花发育后期(开花期)的表型改变。

表3 成花转变、花器官发育以及茉莉酸合成和信号途径相关DEGs统计Table 3 Differentially expressed genes involved in floral transition,floral organ development and JA synthesis and signal pathway

ck为对照;ja为JA处理图6 茉莉酸信号途径和花发育相关的差异表达基因聚类分析Fig.6 Hierarchical clustering of differentially expressed genes involved in floral transition,floral organ development and JA synthesis and signal pathway
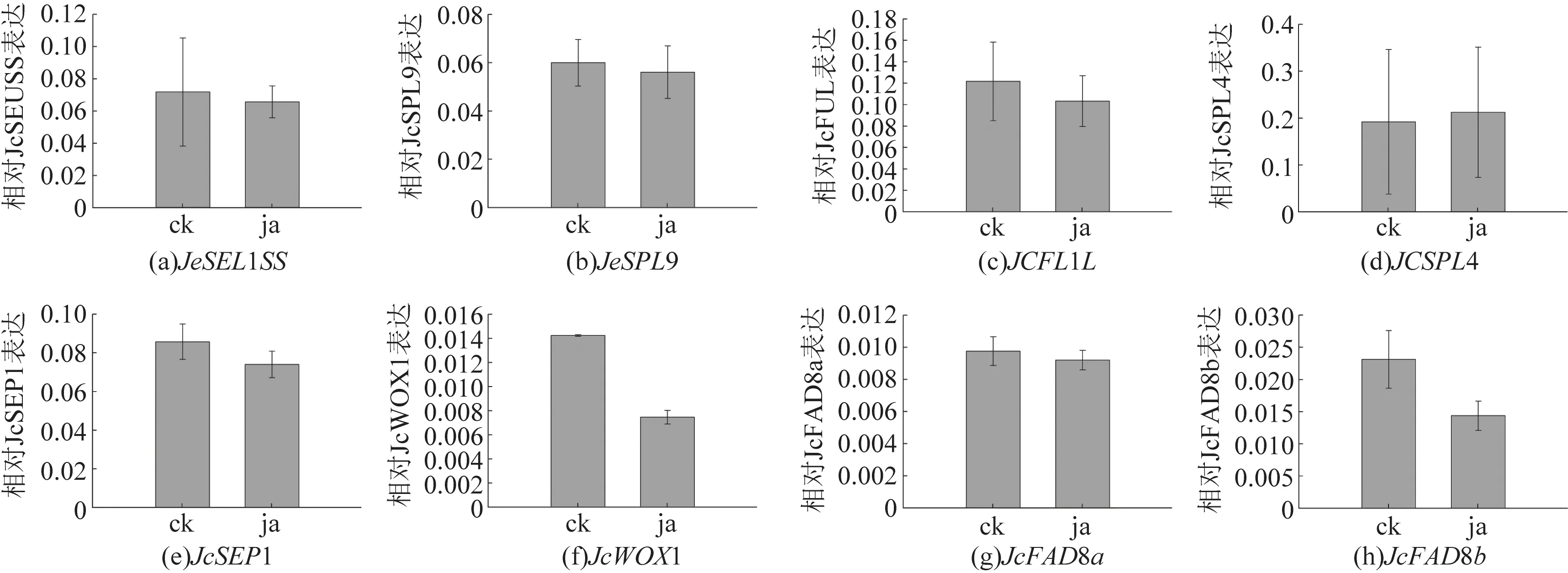
(a)~(h)分别显示JcSEUSS、JcSPL9、JcFUL、JcSPL4、JcSEP1、JcWOX1、JcFAD8a和JcFAD8b基因在对照 (ck)和茉莉酸处理 (ja)样品中的相对表达水平;误差线代表标准差(n=2)图7 小桐子中参与成花转变、花器官发育和茉莉酸合成途径的候选基因表达模式的验证Fig.7 Validation of expression profiles of candidate genes involved in floral transition and floral organ development and JA synthesis pathway in J. curcas
本次研究选取出现1~7 d的小桐子花序芽作为实验对象,事实上花序芽的分化发生在更早的肉眼不可见的时间段[76]。因此,JA处理更早期的未分化的花序芽,可能对花的后期发育影响更显著。另外,茉莉酸甲酯 (methyl jasmonate,MeJA)是茉莉酸的甲酯化形式,其作为信号分子,自由透过细胞膜,较JA不易被离子化[77],因此广泛用于植物胁迫响应和生长发育相关的JA外源处理实验。鉴于本实验在田间露天进行,而MeJA具有挥发性,为避免由于环境因素(风向、光照和温度等)引起MeJA的快速挥发,影响处理效果,故使用茉莉酸作为处理试剂[78]。今后的实验中将采用MeJA进行处理,了解采用JA与MeJA处理小桐子花序芽的效果是否存在差异。
4 结论
对茉莉酸处理的小桐子早期花序芽进行表型变化观察和转录组测序分析,发现茉莉酸处理引起早期花序芽中1 259个基因上调表达,695个基因下调表达。从转录组数据中共筛选到10个与成花转变相关,8个与花器官发育相关和18个与茉莉酸合成和信号转导途径相关的拟南芥同源基因。GO注释显示,“响应茉莉酸”功能分类基因在上调表达基因群中富集,表明外源茉莉酸可以改变小桐子花序芽中的茉莉酸信号途径。在花器官发育相关的基因中,与拟南芥FUL、SRS、SEP1、AGL61、WOX1、TPR4和SEU同源的基因表达下调,然而JA处理后小桐子花的发育后期表型没有发生显著的变化,说明茉莉酸诱发的这些基因的下调表达不足以改变小桐子的花器官发育过程。实验结果对解析茉莉酸在小桐子花发育过程中的调控作用有一定的参考价值。

