经外周静脉穿刺中心静脉置管的应用进展和并发症
吴贝贝
1 前言
中心静脉置管适用于需要长期静脉治疗的患者如重症疾病、手术及化疗患者。中心静脉导管置管术有多个部位可供选择,包括颈内静脉、锁骨下静脉、股静脉或经外周静脉穿刺中心静脉置管(peripherally inserted central catheter,PICC),其各自的特点见图1。因为PICC通过头静脉或上臂的贵要静脉入路,是留置长期静脉通路的首选。同时,选择PICC作为传统静脉输液港(totally implantable central venous access,Port)的替代方法的应用趋势不断增加,原因包括成本较低、安全性更高、易于插入,如果发生感染或血栓形成,可以轻松移除设备以进行源头控制[1,2]。尽管如此,PICC在置管、维护和使用中仍可能发生多种并发症,不能及时发现和有效处理可能导致严重后果,延长患者治疗时间和增加医疗费用。为避免此类并发症,必须了解导管插入术的优缺点、置管技术和管理要求的标准化、医院和临床部门在标准化基础上确保导管置管安全的方法和技术[3-5]。关于PICC程序、潜在并发症和预防措施已有较多的文献报告。不断了解有关置管新技术、并发症早期发现和PICC护理进展对于预防并发症具有重要意义。
2 PICC的形式和超声引导置管
通过头静脉或贵要静脉是大部分PICC入路的首选。在置管过程中一般采用超声引导技术,穿刺之前进行超声检查(预扫描)是一种有效的风险评估方法[6]。通过观察超声图像中目标静脉周围的组织结构以了解身体表面上的解剖标志的位置关系,包括:①评估静脉是否适合穿刺(目标静脉是否存在,是否存在静脉血栓形成);②评估穿刺时风险(弯曲或偏斜的静脉,与动脉的位置关系,与周围组织的关系);③术后风险评估(导管插入可减少小静脉中的血流,这可能导致血栓形成或静脉狭窄)[6,7]。患者特定的风险包括肥胖(体质指数>30)或低体重(消瘦;体质指数<20)、水肿、手术伤口、起搏器或在穿刺部位感染、放疗、凝血病(或未校正的抗凝治疗,抗血小板治疗)以及无法仰卧位[8-10]。其他评估风险的内容包括患者的体格(身高、体重、外表)、一般状况(营养不良、脱水、是否存在血容量不足)、生理发现、胸部X光片、全血细胞计数、血液生化、凝血功能、病史等。出血风险的正常安全标准是血小板计数为50 000/L或更高,凝血酶原时间国际标准化比率(PT-INR)为1.8以下,活化部分凝血活酶时间不超过正常上限的1.3倍。穿刺决定应在充分考虑患者的状况以及风险和收益后进行[5]。

表1 中心静脉置管穿刺部位特征[5]
尽管通过臂部外周血管穿刺置管是临床的常规方法,近年来中心静脉置管的形式不断改善和改进以适合患者的需要和满意度。在一些特殊情况下,如女性乳腺癌患者考虑的美容效果,置管位置需要远离可能导致感染灶或气管分泌物污染,一些部位不适合置管的情况下(如放射治疗头颈癌的放射性皮炎患者、严重后凸畸形的患者、胸部和颈部有大面积疤痕或由于皮肤增厚、无弹性、手术伤口裂开的风险),置管后的并发症发生率高,可能导致导管闭塞、上肢深静脉血栓形成、局部感染和针头脱位以及药物外渗导致4%~17%的患者移除该装置[11-13]。因此,自外周插入的中心导管输液港技术(PICC-Port)应用增加,这是一种由完全可植入组织的中心静脉导管装置,其的定位技术与PICC相同[14-16]。Bertoglio等[15]通过1年随诊观察后认为PICC-Port是一种安全的化疗血管装置,在乳腺癌患者中取得与传统长期血管通路装置相似的临床结果。Annetta等[16]报告了60例PICC-Port手术的经验,包括19例双侧手臂静脉通路和双侧锁骨下区域的禁忌症;41例有双侧插入外周中心静脉导管或股骨导管的禁忌症以及在锁骨下区域的部位禁忌症,结果认为其是一种安全、并发症少的操作,应考虑作为复杂静脉通路患者的一种选择。
3 导管的尖端位置
一旦PICC置管完成,需要确认导管是否放置在正确的位置。尖端的理想定位没有明确的共识,通常PICC导管的尖端应位于具有高血流量的宽大静脉的长轴上,远离血管壁和血管分叉处[17,18]。普遍认为尖端应位于上腔静脉和右心房的交界处(caval-atrial junction,CAJ)。在几种确认PICC定位的方法中,胸部X线检查确认导管尖端位置是公认的确认方法或金标准[19,20]。通过胸片或透视,导管的尖端应大致平行于上腔静脉壁,在锁骨下缘后部,在第三肋骨与第四/第五胸椎之间,气管分叉或右支气管。气管的分叉通常位于心包折返的上方,PICC管避免靠近心包折返是因为可以最大限度地减少临床使用过程中出现并发症的风险,如由于血管壁的侵蚀而发生穿孔,则可能发生纵隔血肿,输液可能进入心包出现心脏填塞[5,21]。
由于X线二维成像确定初始尖端放置位置是通过解剖学界标和人体测量学估计值来判定,这种方法有明显的局限性,包括测试性能的延迟、成本较大、辐射暴露,图像采集和技术要求较高,尖端位置的主观解释以及导管因呼吸运动移动(4~5 cm)[22,23]。有文献报道,胸片上识别在CAJ的PICC尖端位置不准确,最低报告的阳性预测值为14%[20]。另外,荧光检查虽然可以提供较低的辐射照射量,但其成本和需要专用成像设备限制了在常规临床的使用[24]。
计算机断层扫描(CT)能够比较准确地定位导管的远端部分是否在预期位置上[25]。如果PICC位置在正侧位胸片上看起来不典型或不确定,可能需要通过CT或导管注射少量造影剂以进行精确的放射照相定位。Roldan等[25]报告,通过右颈内静脉置管时,导管尖端可能会误入乳内静脉。从解剖学上讲,乳内静脉起源于头臂静脉,及上腔静脉上方并沿前胸壁的后部行进[26],因此,从胸片上判断,右侧乳内静脉的导管尖端位于上腔静脉内(图2)。尽管CT常规使用昂贵且不切实际,但可以提供比传统X光检查更准确地定位。
研究表明,超声检查的进步已显示出可用于验证PICC尖端定位。通过PICC注入10 mL生理盐水,右心房中气泡(视为混浊)的超声可视化可用于充分验证导管尖端的位置(图3)[27]。这种技术的重大限制包括无法可视化导管的对齐方式,以及任何异常路线的存在。尽管存在这一技术障碍,Gekle等[28]报告认为还是能够在不到2秒的时间内识别出79%的患者的中心湍流。PICC超声确认与盐水可视化的应用源于多普勒超声发泡实验。传统的气泡测试已被心脏病学用于通过生理盐水冲洗或通过导管注射微气泡来识别室间隔壁缺损[28]。先前的报告表明,盐水推注后2秒内右心房中湍流盐水的可视化证实PICC位置有96%的敏感性和93%的特异性[29]。然而,确定PICC管的标准时间尚未完全确定,在中心静脉中识别到的微气泡不等同于确认PICC管的位置。这种方法可以认为是一种简单、比较可靠的确认PICC管路位置,但确切的时间计算需要更大、更具体设计的研究中进行测试。总之,利用超声来确认PICC放置可减少患者的X线辐射暴露,通过注射盐水后心脏中可见中心气泡的存在推算气泡的出现时间,超声识别导管尖位置的总体阳性预测值为43%[27],尽管不是所有患者都可以替代胸片确认,但至少有潜力减少胸片使用。
越来越多文献提示,心电图确认导管尖端位置具有一定准确性和安全性,但这种方法是否可以减少深静脉血栓形成尚不清楚。腔内心电图导管定位系统包含一根导丝,可以获得叠加在表面心电图上的P波的跟踪。通过跟踪的P波的会聚用于验证腔室交界处的位置,如从增加的P波振幅、最大偏转和双相P的缺失开始(表明管线已插过远)判断尖端位置[30,31]。通过心电图判断尖端位置已被证明置管更快和降低成本[32],不需要进行X线检查确定,甚至与传统方法相比,这种方法被认为可以实现更准确的尖端定位[33,34]。Kleidon等[24]比较42687例PICC导管定位(21098例X线vs.21589例心电图定位)的研究中,接受心电图定位的患者中,中心导管相关的深静脉血栓形成低于X线定位患者(OR:0.74;95%CI:0.58~0.93;P=0.0098),认为使用心电图确认PICC导管尖端放置方法有助于提高患者的安全性尤其是在高危患者。但考虑操作者需要有精通心电图知识,能够熟练操作心电图仪和心电监护仪技术,这需要时间和培训。
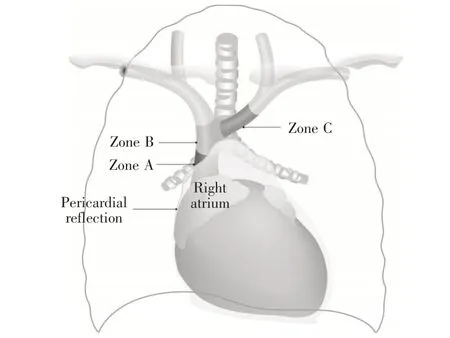
图1 最佳导管放置[5] A区,上腔静脉下段至右心房上段;B区,左、右无名静脉汇合部分和上腔静脉上部;C区,接近上腔静脉的无名静脉
4 PICC与Port的比较
近年来,PICC越来越受欢迎,原因可能是病房中经过短期专门培训的护理团队即可进行插管,而Port学习曲线较长可能使一些医院受到限制,由于需要进入手术室,Port的使用可能会延迟接下来的治疗。选择PICC或Port应以风险收益(包括不良事件风险)、设备可用性、时间、患者偏好和成本为指导。
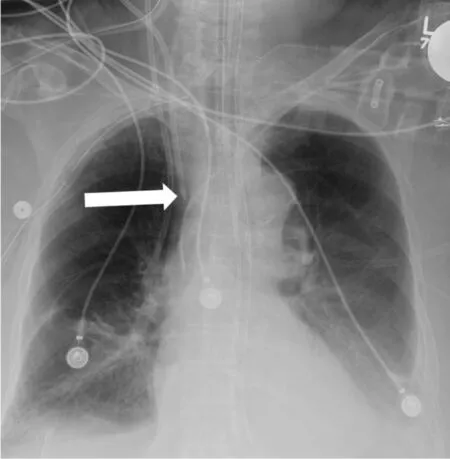
图2 右颈内中心静脉导管显示其尖端位于上腔静脉,阅X光片时显示导管“位置合适”,但导管血液回流不良,注射生理盐水时胸部灼痛[25]

图3 通过剑突下四腔心切面可观察到,推注生理盐水后右心房混浊微泡[27]
有研究报告PICC患者的导管相关深静脉血栓(DVT)发生率可能高于Port[35-38],考虑到与恶性肿瘤和使用中心静脉导管相关的DVT风险,选择使用哪种方法是必要的,尤其在癌症患者中。2015年发布的临床指南表明,当治疗持续时间超过1个月时,PICC和Port之间对于必须从中心静脉给药的治疗没有明确的偏好[39]。由于缺乏证据,欧洲协会内科肿瘤学和美国临床肿瘤学会也没有关于中心静脉置管的类型提出具体建议[40,41]。
Taxbro等[42]通过随机对照研究PICC或Port导管相关深静脉血栓形成等并发症的发生率。该研究包括来自两个瑞典肿瘤中心(主要是乳腺癌和结直肠癌),随访长达1年。主要终点是发生具有临床意义的导管相关深静脉血栓形成,次要终点是与导管相关的不良事件的复合:插入并发症、血栓形成、闭塞、感染和机械问题。结果显示,与Port患者相比,PICC者的复合不良事件的总体发生率更高(HR=2.7;95%CI:1.6-4.6;P<0.001)。这项研究与较早前Patel及其同事[35]的随机试验的结果相似。Pu等[4]Meta-分析显示,PICC的使用与更高的并发症发生率相关,包括闭塞、感染、错位、导管相关血栓形成、外渗、静脉炎和意外移除率和高成本。关于PICC与Port的成本,更多的研究显示PICC置管成本低于Port,但维护成本高于Port[43]。对于长期化疗的癌症患者,Port的成本低于PICC,PICC的成本高的主要原因是与不良事件和管理相关的成本高[44]。
一些研究表明,PICC患者的DVT率为4.3%~11.7%,Port患者为1.6%~3.3%[45-47],包括癌症患者在内的三项系统评价得出结论,PICC与其他传统中心静脉置管相比,导管相关深静脉血栓形成(DVT)的风险增加[5]。DVT的发病机制是多因素的,并且已经提出了几个危险因素。静脉导管的插入会在插入部位造成血管损伤,插入后不久纤维蛋白沉积物粘附在导管的血栓形成表面。插入导管的静脉中的血流量根据静脉与导管的直径比减少[48]。血流减慢、血管损伤以及与恶性疾病和导管本身相关的高凝状态是静脉血栓形成的典型因素(Virchow的三联征)。在一项系统评价中,PICC患者的CRBSI发生率为每1000个导管日1.8~7.7[49],在另一项比较PICC与中心静脉导管的系统评价中,报告了与中心静脉导管相关的血流感染的相对风险在癌症患者中为0.9(95%CI:0.3-2.6)[50]。Lebeaux及其同事30报道了肿瘤患者每1000导管日的PORT相关感染发生率为0.1~1.5。PICC和PORT患者的导管相关性血流感染(CRBSI)发生率非常低,为每1000个导管日0~0.05[45,51,52]。
应该强调的是,如果因为发生感染并发症而选择PICC而非Port的观点是不合理的,尽管一旦发生感染,PICC的优势是容易拔管处理,但因为两种方法的CRBSI发生率都非常低,不能为了避免潜在的CRBSI而将患者暴露于持续增加的DVT风险中。因此,针对不同患者个体选择正确的方法是关键。虽然Port较PICC有较多的局部感染,当控制时间时,差异并不显著[42]。PICC和Port导管的留置时间差异主要是治疗结束时PICC更常拔出,而Port导管往往还要保留一段时间[42]。
5 PICC并发症
从生理上讲,PICC导管占据了手臂外周静脉的部分横截面直径,易导致静脉淤滞[53],外周插入的中心导管尖端经常移位并损伤内皮[54],化疗输注也具有血栓形成风险,并且由于所有上述因素,PICC通常为血栓形成创造良好的条件。导管相关血栓形成的危险因素可分为三种类型,不同研究中的报道差异很大:①化疗类型和预防性抗凝剂的使用;②患者因素如近期外伤或手术、癌症、VTE病史、年龄较大和肾功能衰竭;③导管尺寸、类型、尖端位置、插入部位、静脉插入次数和导管停留时间[55]。
有研究报告,PICC相关DVT的发生有许多重要的危险因素,如年龄、PICC时间、既往DVT和持续超过1小时的手术[56,57]。另有研究报告,DVT风险与导管直径相关,每根导管的深静脉血栓发生率分别为0.1%和6.6%(直径<3-F、4-F和5-F)[58,59]。中心静脉通路装置和插入技术的不当是术后并发症的重要危险因素,特别是在危重病人中[60],糖尿病、慢性阻塞性肺病和晚期癌症等伴随疾病是PICC置管后发生DVT预测因素[3]。既往导管置管术、多次的插入尝试和卵巢癌与DVT发病率增加有关[61,62]。
Al-Asadi等[3]报告,高血小板计数和含氟哌啶化疗与静脉血栓栓塞症(VTE)发生有显著关系。在一项涉及32项观察研究的分析中发现吸烟与其他危险因素无关的VTE风险增加[63],这可能是促凝状态、血浆纤维蛋白原水平升高和炎症状态。在低血小板计数的癌症患者中,PICC相关DVT的风险较低,接受化疗会增加VTE风险,大约是非化疗的两倍以上[64]。
目前的指南不建议在癌症患者中设置长期PICC线路时进行血栓预防,尽管有随机对照试验(RCT)的支持[65],但目前没有证据表明血栓预防有助于预防这些事件[66,67]。此外,最近对12项临床试验的荟萃分析评估了使用中心静脉导管的癌症患者的一级预防剂量肝素或低剂量华法林,但未显示出对研究的主要终点有任何益处[68],至少抗凝治疗应在减少血栓栓塞并发症的可能益处与抗凝剂可能的危害和负担之间取得平衡[69]。根据最新美国血液学会2021年静脉血栓栓塞管理指南,强烈建议包括在接受癌症化疗的VTE风险较低的门诊患者中不使用血栓预防,并使用低分子量肝素(LMWH)对癌症患者的VTE进行初始治疗[70]。考虑使用抗凝剂的患者应在减少血栓栓塞并发症的可能益处与抗凝剂可能的危害和负担之间取得平衡[67,69]。
中心静脉导管相关血流感染(CLABSI)的一个主要危险因素是中心静脉导管的长期维持。然而,长期的PICC维持而不会导致CLABSI的确切持续时间尚未确定。大多数支持PICC比传统深静脉置管在血流感染方面更安全的观点,然而一项前瞻性队列研究认为,在高危住院患者中使用PICC导致的血流感染率与传统中心静脉置管的血流感染率相似[50]。Chopra等[71]分析显示,PICC住院患者和其他类型CVC住院患者的血流感染率相似。最常引起PICC导管相关感染的CLABSI的已知病原体是凝固阴性葡萄球菌、金黄色葡萄球菌、念珠菌属和肠道革兰氏阴性杆菌。由于插入部位和中心是微生物的主要来源[72]。至于导管维护的持续时间,目前的指南建议仅在不再需要导管时才需要拔除导管[5],不推荐常规更换导管来预防血流感染[5,73]。根据Cobb等[74]的研究,推荐的平均导管维护时间为10~17天,Park等[75]的报告最佳截止为25天。另外导管相关感染可能还与PICC导管的材质、操作者的经验有关[76,77]。不管争议如何,采用适当的策略来预防PICC患者的血流感染是必不可少的,因为这些感染可能会产生致命的后果。
6 总结
PICC是一项适用于各个医学领域的基本技能,适用于需要长期静脉治疗的患者如化疗、肠外营养、输液或输血的患者。导管头静脉或贵要静脉置管位置提高了患者的生活质量,其并发症包括感染、导管血栓形成发生率并不高或者应对手段、效果良好,PICC总体安全性高。但是,尽管发生概率很低,PICC的置管和应用过程可能会产生严重后果。因此,PICC的操作者必须熟悉相关基本知识如影像学知识和基本技能,不但要充分了解PICC应用安全性和风险,而且能够妥善处理,通过不断跟踪PICC的使用、维护和并发症处理的发展现状,能够做到无论一般原则还是特定病例的个性化处理的最理想状态。

