甲烷氧化菌素-纳米金修饰金电极溶出伏安法对Cu2+的检测
薛 也,王 艳,,赵 宁,窦博鑫,辛嘉英,2,韩 烨
(1.哈尔滨商业大学食品工程学院,黑龙江省普通高校食品科学与工程重点实验室,黑龙江 哈尔滨 150076;2.中国科学院兰州化学物理研究所,羰基合成与选择氧化国家重点实验室,甘肃 兰州 730000)
Cu2+在工业和农业上有广泛应用[1],常被用作保鲜剂、保色剂、杀菌剂,有防止果蔬变质、保持农作物颜色以及杀菌的作用,并且Cu2+也是人体内必不可缺少的微量元素,摄入过多或缺乏都会危害健康[2-3]。因此,Cu2+是食品分析及食品安全检测中的重要指标[4-6]。
Cu2+常用检测方法主要有原子吸收光谱法、电感耦合等离子体质谱法、荧光光谱法等,但这些方法都存在着耗时较长、需要专业操作人员、不利于实际应用等问题[7-12]。近几年随着电化学技术的不断完善,其灵敏度高、制作简易、检测速度快等优点备受国内外学者的关注[13],常被用于重金属检测工作中。Peng Donglai等[14]研制了罗丹明B肼修饰纳米金的电化学传感器,并将其应用于检测水中Cu2+,检出限为12.5 µmol/L。Kaur等[15]合成了螯合型二硫醇并将其自组装到金电极表面,形成能够吸附金属离子的大环,用于检测Cu2+,线性范围为1.0×10-12~1.0×10-5mol/L(r2=0.990),检出限可达到9.7×10-13mol/L。朱浩嘉等[16]利用同位镀汞阳极溶出伏安法对牛奶样品中Cd2+、Pb2+和Cu2+元素含量进行同时测定,其中Cu2+的线性范围为0.5~100 μg/L,检出限为0.1 μg/L。
甲烷氧化菌素(methanobactin,Mb),是一种由甲烷氧化菌(Methylosinus trichosporiumOB3b)产生的具有极高铜亲和力的蛋白活性肽,在Mb结构中含有2 个4-亚硫酰-5-羟基咪唑基团,通过2 个咪唑N、2 个硫酰S与铜络合,能特异性捕获环境中的铜,对Cu2+具有较强的专一性[17-18]。纳米金(gold nanoparticles,AuNPs)具有较大的表面积、好的生物相容性和表面等离子体增强效应等优点,可以在局部形成增强的电磁场,吸附生物大分子,常用于电化学实验[19-21]。由于AuNPs表面容易功能化,易与生物分子相互结合,通过在柠檬酸钠还原法合成的AuNPs(粒径16 nm)中引入Mb,可使Mb的生物活性被赋予在AuNPs上,有利于生物分子的稳定结合,增强特异性结合,颗粒分散均匀,可以抑制纳米颗粒的团聚[22-23](图1A)。因此本实验借助AuNPs与裸金电子之间的强吸附特性、Mb中L-半胱氨酸巯基与AuNPs通过金硫键键合的特性,制备Mb-AuNPs修饰电极(图1B),通过Mb对Cu2+特异性捕捉的作用(图1C),利用溶出伏安法检测Cu2+具有检出限低、灵敏度高、简便快速的优势。

图1 Mb-AuNPs修饰电极检测原理图Fig.1 Schematic diagram of copper ion detection with Mb-AuNP-modified electrode
1 材料与方法
1.1 材料与试剂
甲基弯菌IMV 3011 俄罗斯科学院催化研究所;无水乙醇 天津富宇精细化工有限公司;氯金酸、CuSO4、PbCl2、HgCl2、Ag(NO3)2、FeCl3、CrO3、CuCl国药集团上海试剂有限公司;柠檬酸钠、氢氧化钠、浓硫酸 天津市天力化学试剂有限公司。
1.2 仪器与设备
PB-10 pH计 赛多利斯(上海)贸易有限公司;生化发酵罐 上海保兴生物设备工程公司;CHI630电化学工作站、金盘电极、铂丝电极、Ag/AgCl电极(3 mol/L KCl溶液) 上海辰华仪器公司。
1.3 方法
1.3.1 Mb-AuNPs修饰电极的制备
参照文献[24-25],对甲烷氧化菌进行培养并提取Mb(1×10-4mol/L),制备Mb-AuNPs;本实验使用固体三电极体系(工作电极:金电极;参比电极:Ag/AgCl;对电极:Pt电极),参考文献[26-27]的方式稍作调整对金电极进行预处理。配制食人鱼溶液(浓硫酸-过氧化氢(7∶3,V/V)),将金电极泡制在其中8 min后,用去离子水洗净;在0.3、0.1、0.05 μm氧化铝粉末上抛光后,分别用无水乙醇和二次蒸馏水在超声中清洗各3 min;吹干后,在0.5 mol/L H2SO4溶液中循环伏安法扫描15 圈进行活化。将电极浸泡在已配制好的pH 6.5的Mb-AuNPs中8 h,4 ℃避光保存,制得Mb-AuNPs修饰电极。
1.3.2 溶出伏安法检测Cu2+
取出已经修饰好的金电极,去离子水冲洗20 s后吹干,吸附待测浓度的Cu2+溶液50 min,同1.3.1节冲洗吹干,随后利用溶出伏安法在0.05 mol/L且pH 5.5的磷酸盐缓冲液(phosphate buffered saline,PBS)中进行检测,电沉积时间40 s,频率10 Hz,振幅25 mV。
1.3.3 干扰程度计算

2 结果与分析
2.1 金电极活化
如图2所示,经过硫酸活化后,其还原峰增加,且有多重氧化峰的出现,说明金电极的灵敏度增加,有助于Mb-AuNPs充分修饰电极。
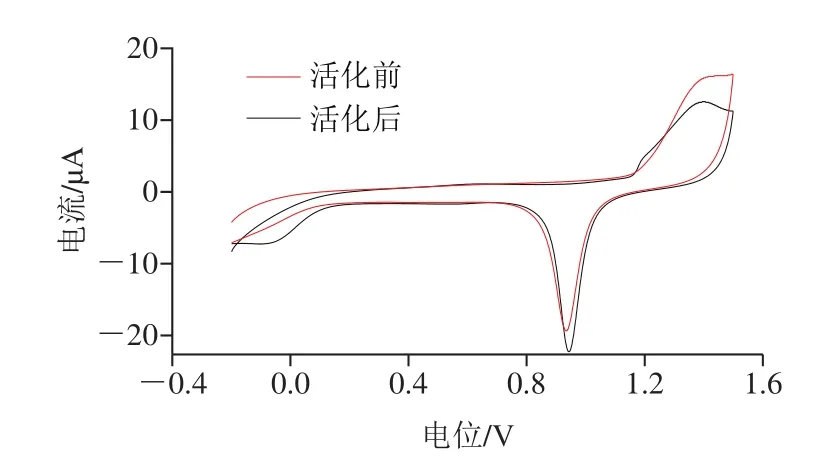
图2 金电极硫酸活化前后对比图Fig.2 Effect of H2SO4 activation on electrode sensitivity
2.2 电极一致性的检测
为保证实验严谨且因实验所使用的金电极数量多,对预处理后的电极进行一致性考察[24]。如图3所示,6 根电极扫描出的曲线重合性较好,说明实验时金电极基本一致。

图3 金电极的一致性考察Fig.3 Consistency of electrodes
2.3 Mb-AuNPs修饰电极的表征
如图4所示,Mb-AuNPs修饰电极较空白电极相比,多出2 个还原峰,-0.7 V处的峰所代表的是金硫键的特征峰,Mb与纳米金完全结合可能是导致其峰形较小的原因。-1.1 V处峰代表的可能是Mb-AuNPs的扩散特性[21],由此判断,Mb-AuNPs已修饰在电极表面[26,28]。
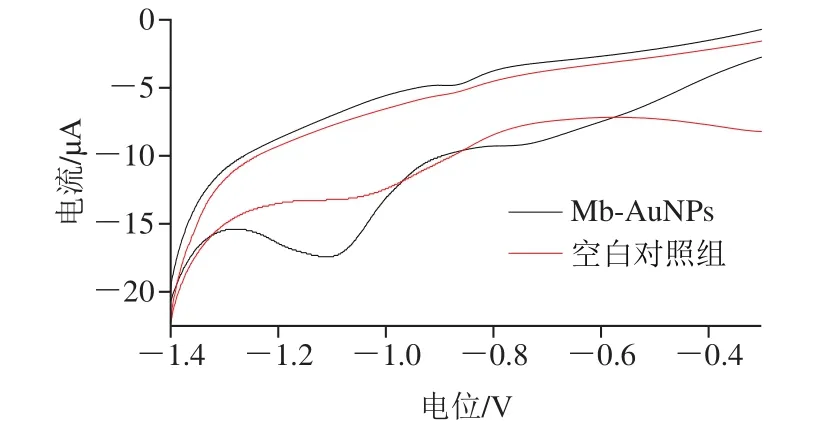
图4 Mb-AuNPs修饰电极表征图Fig.4 Characterization of Mb-AuNP-modified electrode
2.4 溶出伏安法检测Cu2+
2.4.1 Mb-AuNPs修饰电极时间的影响
已处理好且一致性良好的电极分别在Mb-AuNPs溶液中浸泡2、4、6、8、10、12 h后,对100 nmol/L的Cu2+待测液进行检测。如图5所示,检测的Cu2+峰电流值与金电极在Mb-AuNPs溶液的浸泡时间呈一定相关性。金电极浸泡在功能化纳米金复合物溶液中时长为8 h时,Cu2+检测的电信号强度最大。当浸泡时间从2 h增加到8 h时,峰值电流不断增大。8 h后再继续增加浸泡时间,峰值电流减小。这说明当浸泡时间为8 h时,电极上的Mb-AuNPs已接近饱和状态。

图5 Mb-AuNPs修饰时间对检测Cu2+的影响Fig.5 Effect of Mb-AuNP modification time on the detection of copper ions
2.4.2 Cu2+吸附时间的影响
在检测Cu2+前,需要将Cu2+吸附在已修饰好的电极上,即将已修饰好的Mb-AuNPs电极浸泡在Cu2+溶液中。如图6所示,吸附时间在10~50 min时,峰电流值随着吸附Cu2+溶液时间的延长而增加。这说明吸附时间越长,与Mb-AuNPs作用的Cu2+量就越多,即Cu2+在电极表面的吸附量就越大,检测到的信号就越强,溶出峰电流值越高。吸附时间在50 min之后,随着吸附时间的延长,Cu2+的峰电流值减小,这可能是由于Mb-AuNPs和Cu2+之间的键合作用虽然较强,但随着吸附溶液时间延长,部分Cu2+脱落,断开了与Mb-AuNPs的连接,最终检测出的峰电流值减小。

图6 Mb-AuNPs修饰电极吸附Cu2+时间对检测的影响Fig.6 Effect of adsorption time of Cu2+ onto Mb-AuNP-modified electrode on detection efficiency
2.4.3 电沉积时间的影响
如图7所示,10~40 s的峰电流值逐渐增长,这可能是由于沉积时间比较短,Cu2+在电极表面沉积还原的量小于富集的量,因此电信号呈现出随沉积时间延长而增大的趋势。在40 s时,沉积时间使Mb-AuNPs配位的Cu2+全部还原。随着时间的延长,可能是电极表面的Mb-AuNPs部分脱落,从而导致电信号降低。综上,沉积时间选择40 s。
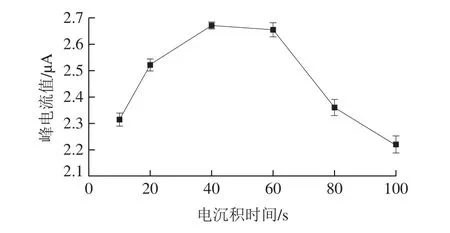
图7 沉积时间对Mb-AuNPs修饰电极检测Cu2+的影响Fig.7 Effect of deposition time on detection efficiencyof copper ions
2.4.4 PBS pH值的影响
如图8所示,在pH 4.5~5.5时,随着pH值的增加,峰电流增大。pH值大于5.5时,峰电流减小可能是由于随着pH值升高,Mb-AuNPs与Cu2+的相互作用减弱,Cu2+脱落。故选择pH值为5.5的PBS作为检测条件。

图8 pH值对Mb-AuNPs修饰电极检测Cu2+的影响Fig.8 Effect of pH on detection efficiency of copper ions
2.5 线性关系与检出限
采用方波溶出伏安法,利用Mb-AuNPs修饰电极对不同浓度Cu2+进行检测。由图9可知,随着Cu2+浓度的增加,其溶出峰也在升高。以lgc为横坐标(c为Cu2+浓度),相应的峰电流(μA)为纵坐标,作标准曲线,峰电流值与Cu2+浓度的对数呈一定线性相关。通过线性拟合在10 nmol/L~100 μmol/L范围内的9 种Cu2+浓度的对应峰电流值回归方程为:I=0.385 44lgc+2.007 53(R2=0.960 09,n=6)说明线性关系良好。经计算,检出限为1.15 nmol/L。

图9 方波溶出伏安法检测Cu2+Fig.9 Detection of copper ions by square wave soluble voltammetry
2.6 干扰离子检测
在100 nmol/L的待测溶液中加入10 倍其他离子,分别是Pb2+、Hg2+、Ag2+、Fe3+、Cr6+、Ni2+、Al3+、Zn2+、Cu+,对检测体系的特异性进行测定,每组测定5 次,结果如表1所示,各离子对检测Cu2+时的干扰程度均小于2%,可忽略不计。因此Cu2+的检测浓度在10 nmol/L~100 µmol/L时,不受其他离子的干扰,由此可以证明Mb对捕捉Cu2+具有较强的专一性[17,22]。
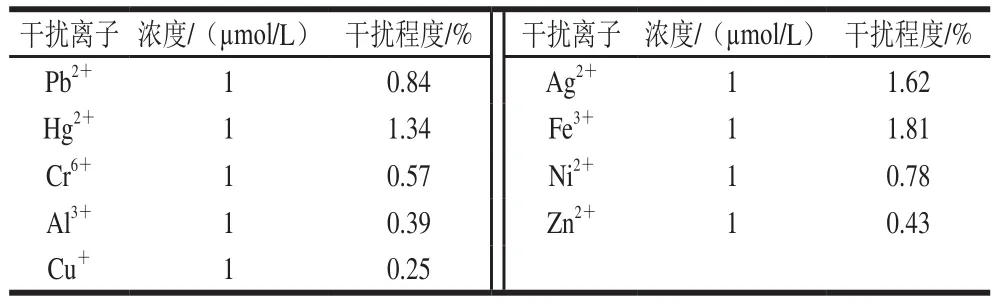
表1 其他离子对检测的影响Table 1 Interfering effects of coexisting ions on Cu2+ detection
2.7 重复性与稳定性
为了检验实验结果的一致性和电极的稳定性,进行重复性实验。在PBS里对检测Cu2+的电极连续10 次扫描,平行测定5 次,相对标准偏差为8.9%。将制备好的修饰电极保存于4 ℃冰箱中,分别存放2、4、6、8、10、12、14 d后取出对Cu2+检测,重复5 次实验,结果如表2所示,在第14天对Cu2+的响应电流强度达到84.24%,表明该修饰电极稳定性良好。

表2 Mb-AuNPs修饰电极Cu2+检测稳定性Table 2Stability of Mb-AuNP-modified electrode for detection of copper ions
3 结 论
用Mb-AuNPs修饰金电极建立了检测Cu2+的新方法,金电极修饰时间8 h、检测时间50 min、电沉积40 s、PBS(pH 5.5)的溶出伏安法对Cu2+检测呈现良好线性关系,检出限可达到1.15 nmol/L,均低于文献报道[17,23,29-30],说明敏感性好。10 倍浓度的9 种其他金属离子的干扰实验均显示对检测结果无明显影响,说明特异性好。通过重复性、稳定性实验,表明此Mb-AuNPs修饰电极检测Cu2+准确性高且稳定性良好。因此,本方法对运用在食品中进行痕量的Cu2+检测具有参考应用价值。
- 食品科学的其它文章
- 基于氮稳定同位素比例质谱和液相色谱-高分辨质谱的有机番茄鉴别
- 气相色谱-负化学源电离-质谱法测定蔬菜中氟虫腈及其代谢物残留
- 脂质去除分散固相萃取-气相色谱-串联质谱测定鸡蛋中62 种农药残留
- 咪鲜胺及其代谢物2,4,6-三氯苯酚在金柑防腐保鲜贮藏中的残留动态及风险评估
- QuEChERS-高效液相色谱-串联质谱法测定稻田水产品中氟虫腈及其代谢物残留
- Analysis of Acetanilide Herbicide Residues in Adzuki Beans(Vigna angularis) by Aqueous Two-Phase Extraction Coupled with High Performance Liquid Chromatography

