锂硫电池的正极与负极研究进展
苏春阳,景航昆
(1.宏启胜精密电子(秦皇岛)有限公司,河北秦皇岛 066000;2.北京航天试验技术研究所,北京 100074)
1 概述
由于全球的石油等化石类能源被日渐消耗,以及石油汽油等燃烧向空气中大量排放二氧化碳导致气候变暖,人们迫切需要寻找下一类可持续的,价格低廉并且环境友好的能源存储系统[1]。在所有的电化学存储系统中,锂离子电池在二次充电系统中占据着非常重要的地位。然而锂离子电池最大能量密度为240Wh/kg,且锂离子价格贵,并有过充的安全问题。这些都限制了锂离子电池在市场上的应用[2]。锂硫电池因为其较高的理论能量密度和理论比容量而在近些年被广泛研究。锂硫电池的理论比容量为1 675mAh /g,理论能量密度为2 600Wh kg-1,远高于锂离子电池。锂硫电池是由锂负极和硫正极组成,通过S-S键的断裂-重组来实现电能与化学能的相互转变[3]。
尽管锂硫电池能量密度高,硫正极材料价格低廉且环境友好,然而仍然有很有因素限制了锂硫电池的实际应用[4]。
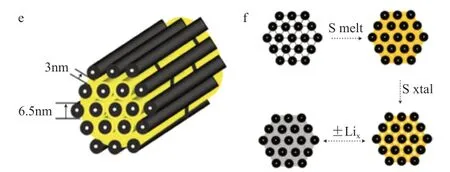
1)硫正极在放电过程中生成可溶性多硫化物Li2Sn(3 2)硫和硫化锂的密度分别为2.03g/cm3和 1.66g/cm3,在放电过程中硫会生成硫化锂,造成电池的体积膨胀,从而导致活性物质硫从导电结构上脱落,使锂硫电池的比容量受到损失。由于硫和硫化锂均为绝缘物质,因此硫化锂在正极导电框架上的生成会影响正极活性物质的溶解,从而降低锂硫电池的反应效率和比容量。 3)锂负极在电池多次充放电的过程中会形成锂枝晶,锂枝晶会穿透隔膜,导致电池短路,从而发生着火或爆炸[5]。这些不足限制了锂硫电池的商业化应用。 为了改善或解决上述问题,科研人员针对锂硫电池的结构设计尝试了很多种方法。分别对锂硫电池的正极[6]、负极[7]、电解液[8]、隔膜[9]等进行了详细研究,本文主要介绍了锂硫电池正极和负极的研究进展。 锂硫电池的硫正极保护主要思路为使用多孔材料构建导电网络结构,使用包覆等方法将可溶性多硫化物限定在正极区域内,避免多硫化物穿梭至负极形成“穿梭效应”,同时增强电子在正极的传输。常用的多孔材料有碳材料,导电高分子聚合物,导电金属氧化物等。 用于锂硫电池正极碳框架的碳种类有多孔碳、石墨烯、碳纳米管等。多孔碳由于其自身无毒,稳定性好,容易获得等优点被广泛应用。多孔碳材料用于锂硫电池时,首先,由于多孔碳本身具有高比表面积和吸附性,通过对其孔道结构和孔容的调整,可有效防止可溶多硫化物向负极扩散;其次,碳本身的导电性可以帮助电子的传输,加速正极绝缘物质硫的反应。2009年,滑铁卢大学的Linda Nazar课题组Ji等使用有序介孔碳CMK-3作为碳导电框架,制备了CMK-3/硫复合材料,如图1所示;其中复合材料中的硫含量达到80%。由于CMK-3的高比表面积,大孔容和特殊的孔道结构,碳材料为正极反应提供了导电网络框架和反应活性位点,极大促进了正极硫向多硫化物的反应速率,从而提升了电池的比容量和循环性能。导电高分子聚合物PEG用于包覆材料包覆在正极表面,进一步限制了多硫化物向电解液和负极的扩散,增加了反应的比容量和循环稳定性。该项研究成果对于锂硫电池整个研究进程的影响意义重大,极大地推动了锂硫电池的研究进程[6]。2010年,张等设计了微孔碳球结构,并使用酯类电解液,目的是通过在微孔孔径内生成小分子硫来限制长链多硫化物的形成[10]。2016年,Jin等[11]通过对大孔碳进行氮元素与钴元素的修饰,与硫复合后用做锂硫电池正极,电池的比容量与循环性能良好。在1C的充放电倍率下,正极在300圈循环后仍然可以保持600mAh/g的比容量。 图1 CMK-3/S复合正极材料结构示意图和氧化还原反应过程示意图 石墨烯作为一种二维材料,具有sp2的蜂巢结构和高比表面积,用作锂硫电池的正极材料时,可通过杂原子修饰后用作正极导电网络,或用于正极与隔膜中间的夹层,通过将硫固定在其表面或者卷入石墨烯内部的方式与硫复合制备正极材料。2016年,Deng等设计了一种全石墨烯碳材料用作正极的锂硫电池。该正极材料中硫含量高达80%(w),石墨烯的孔容高达3.51cm3/g,单位面积的硫含量高达5mg/cm2。其次,高导电石墨烯结构可看作是一个集流体,由于其质量较轻,因此增强了电池的能量密度。并且石墨烯夹层状结构可以有效吸附生成的多硫化物,从而将多硫化物限定在电池的正极,防止其向负极的扩散,从而抑制了穿梭效应的发生。该电池的初始比容量达到了1 500mAh/g,循环400圈后单位面积的比容量仍可以保持4.2mAh/cm2[12]。 由于碳纳米管优异的导电性,良好的机械性能和独特的线状结构,碳纳米管作为硫正极的导电载体被广泛应用。用于正极材料中的碳纳米管制备方法和种类很多,如CVD法原位制备,使用氮、氧等掺杂的碳纳米管等。2017年,Jin等使用B2O3作为B源和O源,制备了B,O掺杂的多壁碳纳米管用于锂硫正极的碳材料。通过在碳纳米管上引入杂原子,创造出更多的反应活性位点和缺陷,提升了正极材料的导电性。B,O等杂原子的存在同时增强了碳纳米管与多硫化物之间的吸附作用。因此,B,O掺杂的碳纳米管有助于减弱穿梭效应的发生,从而提高正极材料的利用率,提升反应的比容量和循环性能[13]。 2016年,Xue等使用中空的SiO2小球做载体,并在其表面包覆了一层TiO2。介孔SiO2结构的小球能够负载80%(w)的硫,并可以在1C倍率下稳定循环1 000次[14]。2017年,Lei等在纳米纤维上沉积了二维的WS2,沉积的WS2非常紧实地存在于碳纳米纤维的表面,WS2具有极性,可将多硫化物吸附于正极,从而防止多硫化物向负极扩散,减少了穿梭效应的发生,增强了反应的比容量和循环性能。当硫含量为2mg/cm2时,在2C倍率下,该电极初始比容量为1.2mAh/cm2,循环1 500圈后仍可保持1mAh/cm2的比容量[15]。 锂硫电池使用金属锂作为电池的负极,金属锂的空间密度只有0.59g/cm3,且理论比容量为3 860mAh/g,负氧化还原电势为-3.040V(相比标准氢电极)。这些优点对于锂硫电池成为高能量密度电池具有重大意义。但同时金属锂作为锂硫电池的负极又有一些缺点,限制了锂硫电池的商业化应用。首先,金属锂在不断的充放电过程中容易形成锂枝晶,锂枝晶很容易穿透隔膜,造成电池的短路、着火等,同时,锂枝晶的溶解并不均匀,因此容易产生死锂,造成电池比容量的下降,并且由于锂枝晶的高活性,能够与电解液反应并消耗电解液[16];其次,金属锂活性较高,容易与多硫化物发生反应,从而导致穿梭效应的形成,降低电池的比容量与循环效率[17-18]。 为了解决上述问题,科研人员尝试各种办法保护锂负极,并对锂枝晶的形成机理进行研究。如通过在电解液中添加盐类物质使负极表面生成SEI膜,在负极表面涂覆保护层或使用碳夹层等。Mikhaylik等发现,通过添加含有N-O键的添加剂,如有机硝酸盐或者无机硝酸盐等,可以极大提高电池的比容量和循环性能。其中,硝酸锂是保护锂负极最有效的添加剂[19-20]。除了在电解液中加入盐类物质等添加剂,还可以通过在金属锂表面通过涂覆,磁控溅射或CVD等方法形成人工SEI膜,保护金属锂负极表面。人工SEI膜首先需要在电化学反应过程中机械结构和化学组成保持稳定,允许锂离子通过,并且对电子绝缘,可以使锂离子沉积在锂片表面。2015年,Jing等通过旋转涂覆的方法,在金属锂片表面涂覆了一层多孔Al2O3涂层,如图2所示;通过在锂片表面涂覆Al2O3涂层,有效保护了金属锂负极表面。将金属锂片表面涂层刮掉后,与未涂覆涂层的锂片表面做对比,发现Al2O3保护过的锂片表面相对更平滑,而未被保护的金属锂片表面有更多裂痕。Al2O3涂层能够有效阻止多硫化物与锂负极的接触,从而减弱穿梭效应的发生,同时,Al2O3涂层的存在使锂负极表面在充电过程中形成离子流,使锂离子更均匀地沉积在金属锂的表面,有效减少了锂枝晶的生成。通过Al2O3涂层对锂负极的修饰,电池的比容量和循环稳定性有了极大的提高[7]。 图2 50圈循环后金属锂片表面形貌和元素分布图对比 2017年,Wang等通过RF磁控溅射的方法,在金属锂片表面覆盖了一层0~200nm的无定形状Li3PO4。涂覆Li3PO4的金属锂片相比于未涂覆的锂片而言,锂片表面更加平整和紧实,涂覆的Li3PO4可以有效减少金属锂和电解液之间的反应,并防止锂枝晶的生成。Li3PO4的存在有效提高了电池的循环稳定性[21]。2016年,Cao等使用原子层沉积(ALD)的方法,在金属锂表面沉积了一层超薄的离子导电性化合物LixAlyS。该沉积层能够有效防止锂枝晶的生成,同时使金属锂表面更平整,LixAlyS的离子导电性降低了电池的阻抗,提高了电池的比容量和循环性能[22]。 通过对锂硫电池正极材料的结构改进和锂负极的保护,极大程度解决了锂硫电池在充放电过程中由于多硫化物溶解所导致的穿梭效应,减弱了由于硫绝缘性所导致的正极电荷传输速率缓慢的问题,并减少了锂枝晶的生成,增强了金属锂表面的平整性,使得锂硫电池的比容量和循环性能均有了明显的提高。然而,锂硫电池未来的商业化应用仍然需要更多科研人员的努力,从成本、活性、安全性等角度做更多改进。2 锂硫电池的硫正极
3 锂硫电池对锂负极的改进

4 结束语

