三氯生通过ERK/NF-κB/MMP-2/-9途径促进卵巢癌细胞迁移和侵袭
张瑛瑜 徐宏仙 杨林峰 陈芳
(1三亚市中医院妇产科,海南 三亚 572000;2中南大学湘雅医学院附属海口医院妇产科)
卵巢肿瘤是全世界女性最常见的恶性肿瘤之一,该病常在晚期被诊断,并有腹腔内转移〔1〕,死亡率高达60%~65%〔2〕。当病变局限于卵巢时,5年生存率高于90%,但当病变在腹腔内播散时,生存率低于20%〔3〕。因此,明确该病发病机制,将为该病的诊断与治疗提供极大帮助。内分泌干扰物(EDCs)是环境中天然或人工合成的制剂,可干扰体内激素正常功能,从而对内分泌系统产生干扰作用〔4〕。而人体内正常激素的循环水平可能与几种生殖系统癌症的风险密切相关。如雌激素水平异常与卵巢、乳腺及宫颈肿瘤的发生发展有关〔5~7〕,这些肿瘤是高雌激素受体阳性或雌激素反应性肿瘤。因此,具有雌激素或雌激素活性的EDCs可能是发生雌激素反应性癌症的重要危险因素。三氯生(TCS)是一种合成的氯化苯醚双酚,用作广谱抗菌剂〔8〕。TCS是肥皂、除臭剂、牙膏等卫生产品的常见成分,使用浓度高达0.3%〔9〕。尽管TCS尚未被归类为EDCs,但已被认为是一种潜在EDC〔10〕。既往有研究发现,TCS可通过雌激素受体依赖途径调节卵巢癌细胞周期和凋亡相关基因的表达,从而刺激细胞生长〔11〕,然而TCS对卵巢癌细胞其他恶性生物学功能的影响尚未被阐明。本研究旨在分析TCS对卵巢癌细胞迁移和侵袭功能的作用及其潜在机制。
1 材料与方法
1.1一般资料 细胞培养卵巢癌细胞系A2780购自美国ATCC,使用含10%胎牛血清和1%双抗的DMEM培养基(Gibco,美国),在37℃、5% CO2的培养箱中培养。
1.2CCK-8 检测细胞活性以1×104个/孔的密度将A2780细胞接种于96孔板中,以不同浓度TCS(Sigma Aldrich,美国)(0、10-10、10-9、10-8、10-7、10-6mol/L)暴露细胞24 h,随后向每孔加入10 μl CCK-8试剂(Dojindo,日本),放回培养箱继续孵育2 h后置于分光光度计中测定450 nm波长处的吸光度(OD)。细胞相对活性=(处理组OD450-背景组OD450)/(对照组OD450-背景组OD450)。每组设置4个复孔。
1.3细胞划痕实验 检测细胞迁移能力以5×105/孔的密度将A2780细胞接种于6孔板中,待细胞融合至90%时,用20 μl移液管尖刮除细胞,用无血清DMEM冲洗细胞2次。分别将细胞暴露于含0、10-8、10-6mol/L TCS的无血清DMEM中再培养24 h,培养结束后对划痕区域进行显微镜观察和成像,使用Image J计算划痕面积(Area)。细胞相对迁移活性(%)=(处理组Area 24 h-处理组Area 0 h)/(对照组Area 24 h-对照组Area 0 h)×100%。
1.4细胞侵袭实验(Transwell) 测定细胞侵袭能力在Transwell(Corning,美国)小室上层涂抹40 μl的基质胶(Corning,美国),制备2×105/孔的密度、不含血清的A2780细胞悬液,分别给予0、10-8、10-6mol/L TCS刺激,取200 μl滴加于Transwell上室中,下室加入600 μl含10%血清的DMEM培养基。培养24 h后用4%多聚甲醛固定Transwell下层细胞,用0.1%结晶紫染色,后在显微镜下观察计数穿过膜的细胞数。
1.5ERK信号通路验证实验 在对A2780细胞进行TCS暴露前,用50 μmol/L的ERK抑制剂PD98059预处理细胞24 h。
1.6Western印迹测定蛋白表达水平用预冷的磷酸盐缓冲液(PBS)洗涤细胞2次,加入含蛋白酶抑制剂的RIPA裂解液(碧云天,中国)中冰裂30 min,然后4℃ 15 000 r/min离心收集上清液,使用二喹啉甲酸(BCA)蛋白浓度测定试剂盒(碧云天,中国)进行蛋白定量,随后取40 μg总蛋白100℃加热10 min变性,用10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离,后转移到聚偏氟甲酸(PVDF)膜(Millipore,美国)上。用封闭液(碧云天,中国)室温封闭PVDF膜2 h。然后在4℃将膜与以下主要抗体孵育过夜:p-ERK、ERK、p-NF-κB p65、NF-κB p65、基质金属蛋白酶(MMP)-2、MMP-9及GAPDH(以上抗体均购自Cell signaling technology,美国)。以GAPDH作为内参蛋白。孵育后用TBST清洗膜3次,后在室温下用辣根过氧化物酶(HRP)结合的二抗孵育PVDF膜1 h。使用增强化学发光检测试剂盒(碧云天,中国)对蛋白荧光信号进行显像。
1.7统计学分析 使用Graphpad Prism软件进行t检验及单因素方差分析。
2 结 果
2.1TCS对卵巢癌细胞活性的影响 不同浓度TCS(0、10-10、10-9、10-8、10-7、10-6mol/L)暴露24 h对A2780细胞活性(1.00±0.04、1.07±0.05、1.02±0.04、1.04±0.08、1.03±0.10、1.01±0.06)无明显影响(P>0.05)。从中选择了10-8和10-6mol/L TCS暴露浓度进行后续实验。
2.2TCS对卵巢癌细胞迁移和侵袭的影响 与(TCS 0 mol/L)相比,TCS暴露显著促进A2780细胞发生迁移(均P<0.05),且TCS 10-8mol/L的促进作用较10-6mol/L更为明显(P<0.05)。侵袭实验的结果与划痕实验一致(均P<0.05)。见图1,图2。

图1 TCS对卵巢癌细胞迁移的影响(×40)

图2 TCS对卵巢癌细胞侵袭的影响(结晶紫染色,×100)
2.3TCS诱导卵巢癌细胞表达MMP-2/-9增加 TCS处理可显著提高MMP-2和MMP-9的蛋白水平(均P<0.05),且10-8mol/L处理组的促进效果更为明显(均P<0.05)。见图3。
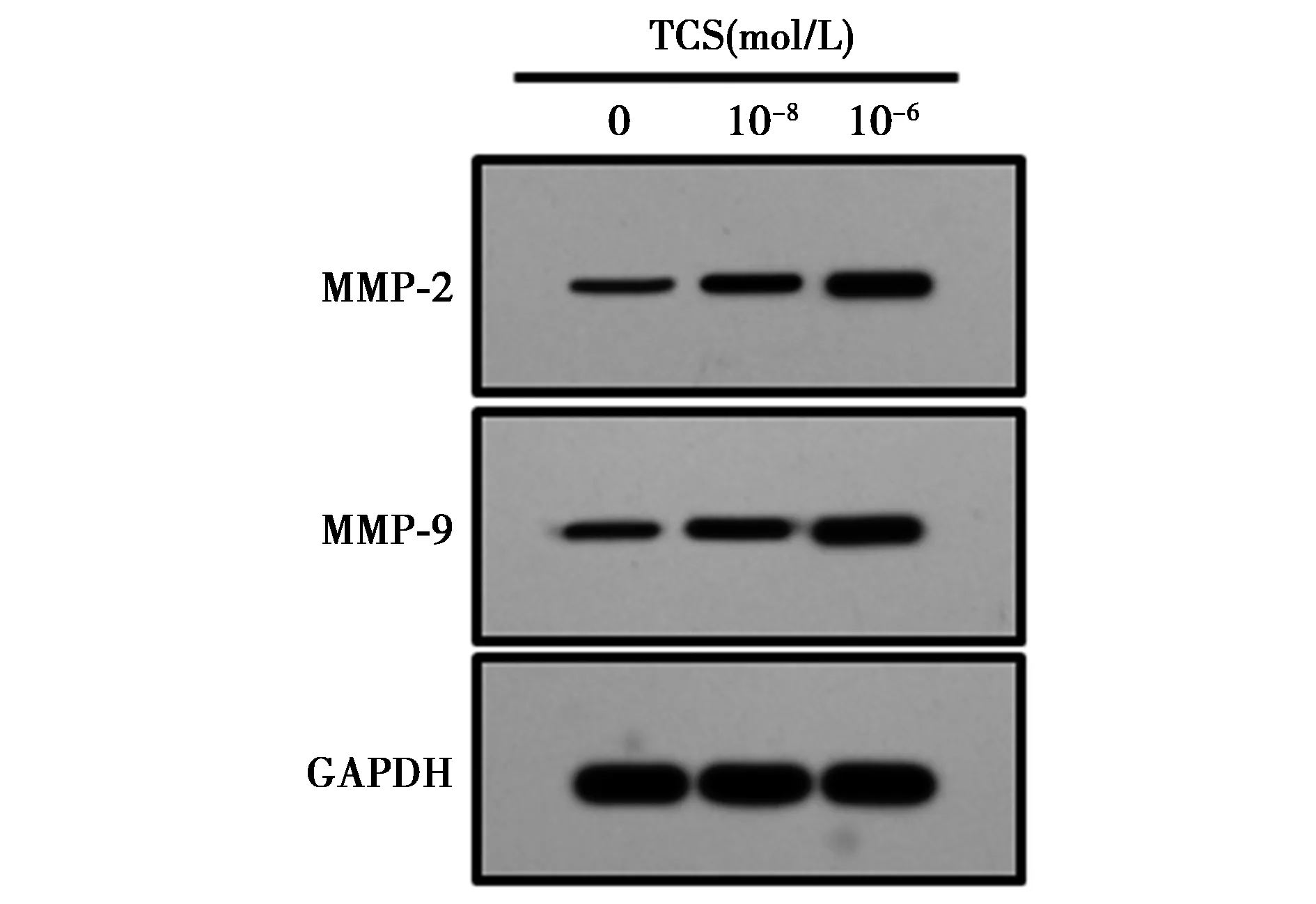
图3 TCS诱导卵巢癌细胞表达MMP-2及 MMP-9增加
2.4TCS通过诱导ERK磷酸化而促进NF-κB活化 TCS处理可显著促进ERK和NF-κB蛋白发生磷酸化(均P<0.05)。为进一步验证TCS对ERK/NF-κB信号通路的激活作用,使用ERK/NF-κB抑制剂PD98059预处理A2780细胞,而后暴露于TCS,前者特异性地阻断ERK/NF-κB磷酸化。见图4。

图4 TCS通过诱导ERK磷酸化而促进NF-κB活化
3 讨 论
近几十年来,EDCs及其对肿瘤细胞迁移和侵袭能力的影响越来越受到重视〔12〕。尽管已有研究表明TCS可促进乳腺癌细胞〔13〕和肺癌细胞〔14〕的迁移和侵袭。在卵巢癌中,仅有报道证实TCS可促进卵巢癌细胞增殖,但尚无关于TCS暴露与卵巢癌细胞迁移和信息能力的研究。本研究发现TCS几乎不影响卵巢癌细胞活性,但显著增强卵巢癌细胞A2780的迁移和侵袭,这与之前在其他癌细胞系的研究一致。因此,本研究结果提示TCS可能也是一种促进卵巢癌进展的致癌物质。
关于TCS诱导卵巢癌细胞迁移和侵袭的潜在机制研究,首先发现了TCS可促进MMP-2/-9的表达增加。MMP-2/-9是MMPs家族的重要成员,鉴于其具有降解细胞外基质的作用,MMP-2/-9的高表达被证明与卵巢癌的高转移潜能有关〔15〕。MMP-2/-9在TCS暴露后的表达在其他癌细胞中也有上调,例如乳腺癌细胞〔13〕。本研究发现TCS诱导卵巢癌细胞MMP-2/-9表达增加可能有助于癌细胞迁移和侵袭。
已有研究证实在多种癌细胞中ERK/NF-κB信号通路的激活对于调节MMP-2/-9的活性非常重要〔16〕。本研究结果表明MMP-2/-9的激活趋势与ERK/NF-κB途径的激活趋势一致。既往有研究发现TCS可通过ERK/NF-κB信号途径发挥作用。如Cheng等〔17〕发现TCS可特异性活化ERK干扰小鼠胚胎干细胞成骨分化;Kim等〔18〕证实TCS可通过活化ERK途径乳腺癌细胞增殖。本研究结果提示TCS确实通过ERK/NF-κB通路发挥作用。
综上,TCS暴露可能通过激活ERK/NF-κB信号通路而促进卵巢癌细胞的迁移和侵袭,提示TCS作为潜在的EDC,有可能加速卵巢癌的进展,并对人类健康构成威胁,有必要加以重视。

