磁性氧化石墨烯纳米复合材料固相萃取-高效液相色谱法测定水果、蔬菜和水样中农药利谷隆
◎ 陈松庆,陈思伊,朱霞石,
(1.扬州大学化学化工学院,江苏 扬州 225002;2.扬州大学广陵学院,江苏 扬州 225128)
利谷隆是一种合成苯基脲除草剂,具有良好的触杀活性,在农业生产中得到广泛应用[1]。利谷隆对杂草有一定的杀灭作用,但能长期稳定地存在于环境中,污染土壤和地表水,严重破坏地下水和生物[2]。毒理学研究表明,这类除草剂对人体有不同程度的毒性,甚至具有致癌作用[3]。因此,准确、灵敏、快速地检测果蔬中利谷隆残留量具有十分重要的意义[4]。
本文建立以磁性氧化石墨烯纳米复合材料(Fe3O4@SiO2-GO)为萃取剂,联合高效液相色谱法分离分析农药利谷隆的新方法。用扫描电镜、透射电镜和红外光谱等对制备的Fe3O4@SiO2-GO进行表征,研究影响利谷隆萃取和洗脱的各种因素。
1 材料与方法
1.1 仪器和设备
DK-S22电热恒温水浴锅(常州国华电器有限公司)、ZK-82B真空干燥箱(上海试验仪器厂)、SH-C恒温振荡器(常州国华电器有限公司)、Agilent 1220高效液相色谱仪(安捷伦科技有限公司)、Bruker tensor 27傅里叶变换红外光谱仪(德国Bruker公司)、S-4800Ⅱ扫描电镜(日本日立公司)、Tecnai-12透射电镜(荷兰Philips公司)、A300-10/12电子顺磁共振波谱仪(德国Bruker公司)。
1.2 药品和试剂
六水硫酸亚铁氨、十二水硫酸铁氨、氢氧化铵、无水乙醇、正硅酸四乙酯、异丙醇、丙酮、乙腈、正己烷、N-羟基丁二酰亚胺、1-(3-二甲基氨基丙基)-3-乙基碳二亚胺、精对苯二甲酸、氢氧化钠、氯化钠、N,N-二甲基甲酰胺、(3-氨基丙基)三乙氧基硅烷、甲醇、聚乙二醇、高锰酸钾、石墨粉和利谷隆。药品和试剂是分析纯,来自国药集团化学试剂有限公司。
1.3 Fe3O4@SiO2-GO制备
根据已报道的方法制备Fe3O4@SiO2-GO[5];0.2 g氧化石墨烯在超声作用下分散在50.0 mL N,N-二甲基甲酰胺中。在上述溶液中加入0.1 g NHS和0.2 g EDC,室温下搅拌2 h。将0.5 g Fe3O4@SiO2-NH2加入到上述混合物中搅拌12 h,洗涤后用水分散即可得到产品。最终产物Fe3O4@SiO2-GO经多次水洗,在80 ℃真空干燥。
1.4 样品处理
新鲜苹果和马铃薯样品来自扬州当地菜市场。水样取自扬州西湖。将样品剥皮并研磨均匀,取10.0 g样品于烧杯中,加20 mL去离子,超声15 min,过滤,并将滤液稀释至50.0 mL。用0.45 μm的膜过滤样品溶液,在4 ℃下储存备用。
1.5 色谱条件
色谱柱:Shin-pack VP-ODS C18(250 mm×4.6 mm,5 μm),流动相:乙腈:水(30:70,V/V),流速:0.8 mL min-1,柱温:25 ℃,检测波长:248 nm,保留时间:9.20 min。
1.6 实验过程
优化萃取条件和洗脱条件,MSPE在优化的实验条件下进行。
MSPE过程如图1所示。①将适量的利谷隆溶液和pH=7.0缓冲溶液加入到50.0 mL离心管中,定容至刻度线。②将12.0 mg Fe3O4@SiO2-GO纳米复合材料加入烧杯中,室温下振荡10 min。③在离心管底部放置一个磁铁,将上层溶液倒出。④加入3.5 mL丙酮洗脱,室温下振荡5 min。通过磁分离,收集上层清液。⑤将20.0 μL洗脱液注入高效液相色谱仪进行测定(λ=254 nm)。

图1 实验流程图
2 结果与分析
2.1 Fe3O4@SiO2-GO表征
通过扫描电镜、透射电镜、红外光谱和振动样品磁强计对制备的材料进行表征,结果表明Fe3O4@SiO2-GO制备成功。
2.2 萃取条件优化
优化萃取剂种类和用量、溶液pH、萃取时间和萃取温度对萃取率的影响。
2.2.1 萃取剂的选择
本 实 验 选 择 Fe3O4、Fe3O4@SiO2、Fe3O4@SiO2-GO 3种材料分别萃取利谷隆,萃取率分别为35.1%、54.8%和95.1%,结果显示Fe3O4@SiO2-GO的萃取率最高,见图2。

图2 萃取剂的选择图
2.2.2 萃取剂用量对萃取率的影响
当萃取剂用量从2.0 mg增加到12.0 mg时,萃取率随萃取剂用量的增加而增加,从12.0 mg到14.0 mg萃取率基本保持不变,见图3。因此,选择萃取剂用量为12.0 mg。

图3 萃取剂用量对萃取率的影响图
2.2.3 pH对萃取率的影响
研究了pH在3.0~12.0范围内对利谷隆吸附性能的影响,萃取率随pH的增大呈现先上升后下降的趋势,见图4,在pH为7.0时萃取率达到最大值,故选择pH=7.0。

图4 pH对萃取率的影响图
2.2.4 萃取时间对萃取率的影响
对萃取时间在1~30 min范围内的影响进行研究,萃取率随着时间的增加而增加,在10 min后趋于稳定,见图5。因此,萃取时间选择10 min。
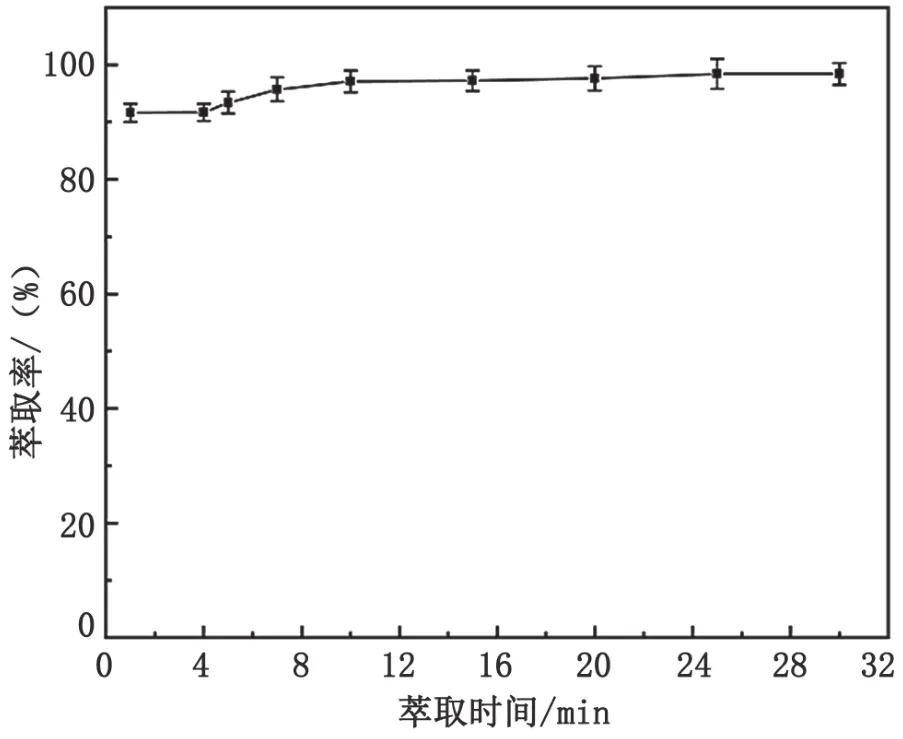
图5 萃取时间对萃取率的影响图
2.2.5 温度对萃取率的影响
研究5~50 ℃范围内温度对萃取率的影响,萃取率随着温度的升高而增加,在25 ℃时达到最大值,随后基本保持不变,见图6。因此,选择在25 ℃下进行萃取。
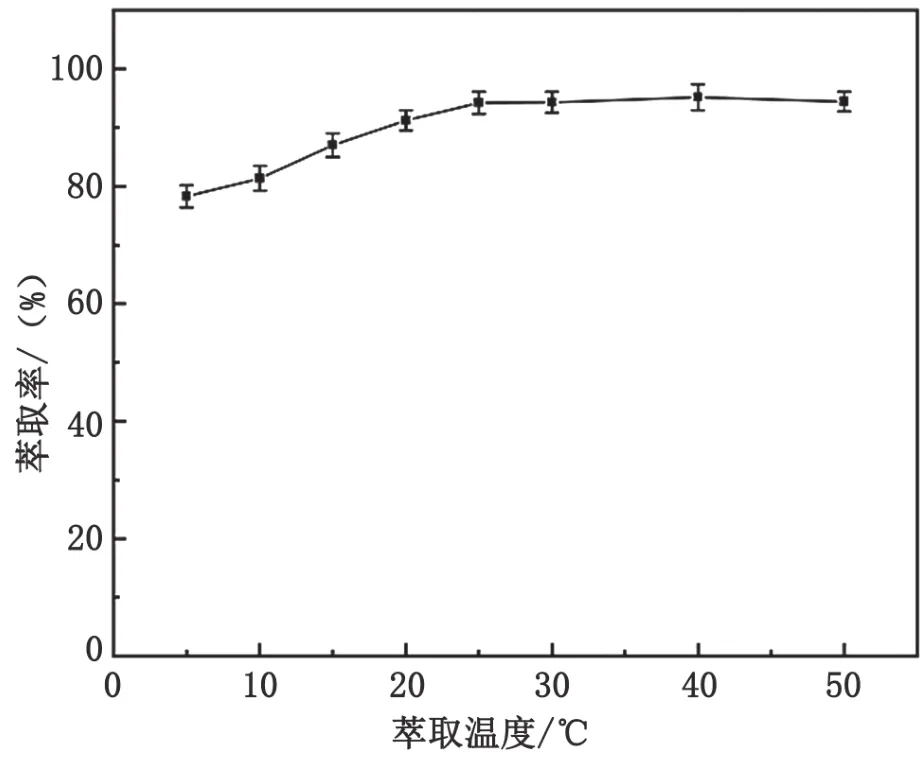
图6 萃取温度对萃取率的影响图
2.3 洗脱条件优化
研究甲醇、乙醇、乙腈和丙酮作为洗脱剂对洗脱率的影响,结果表明,甲醇洗脱率为68.0%,乙醇为71.3%,乙腈为93.0%,丙酮为100.0%,见图7。丙酮的洗脱率最高,因此选择丙酮作为洗脱液。
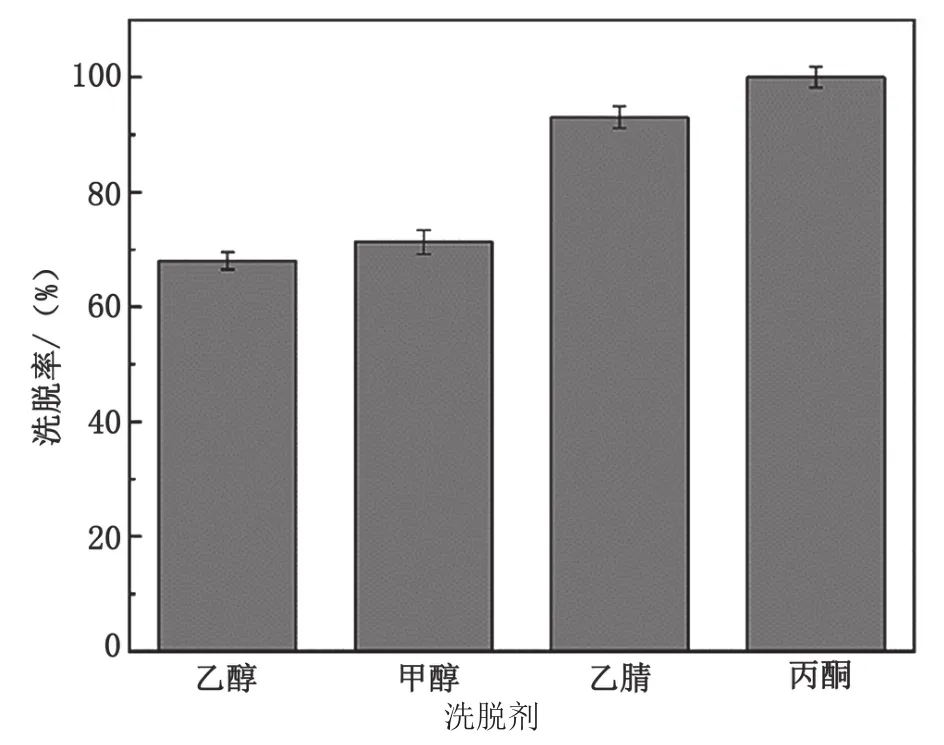
图7 洗脱剂对洗脱率的影响图
在0.5~4.0 mL范围内考察洗脱剂体积对洗脱率的影响,丙酮的最佳用量在3.5 mL,见图8。因此,选用丙酮体积为3.5 mL。
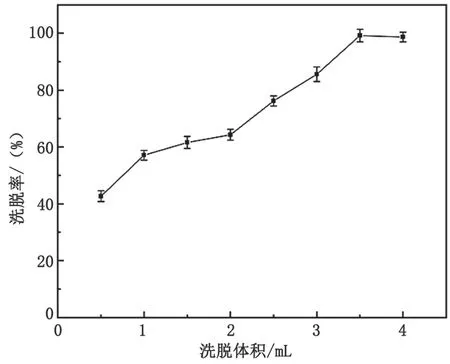
图8 洗脱剂体积对洗脱率的影响图
2.4 性能分析
在最优条件下,方法的线性范围为0.008~0.120 μg mL-1,线性回归方程为y=259.064c+342.16,相关系数为0.999 3,检测限(LOD)为0.001 μg mL-1。相对标准偏差(RSD)为 1.9%(c=0.020 μg mL-1,n=3)。富集因子(EF)定义为萃取前后体积比,本实验的富集因子为14。萃取剂可重复使用11次。
2.5 样品分析
应用本方法测定苹果、马铃薯和河水样品中的利谷隆,结果如表1所示。实际样品中未检测到利谷隆残留,回收率在92.5%~105.0%,结果令人满意。
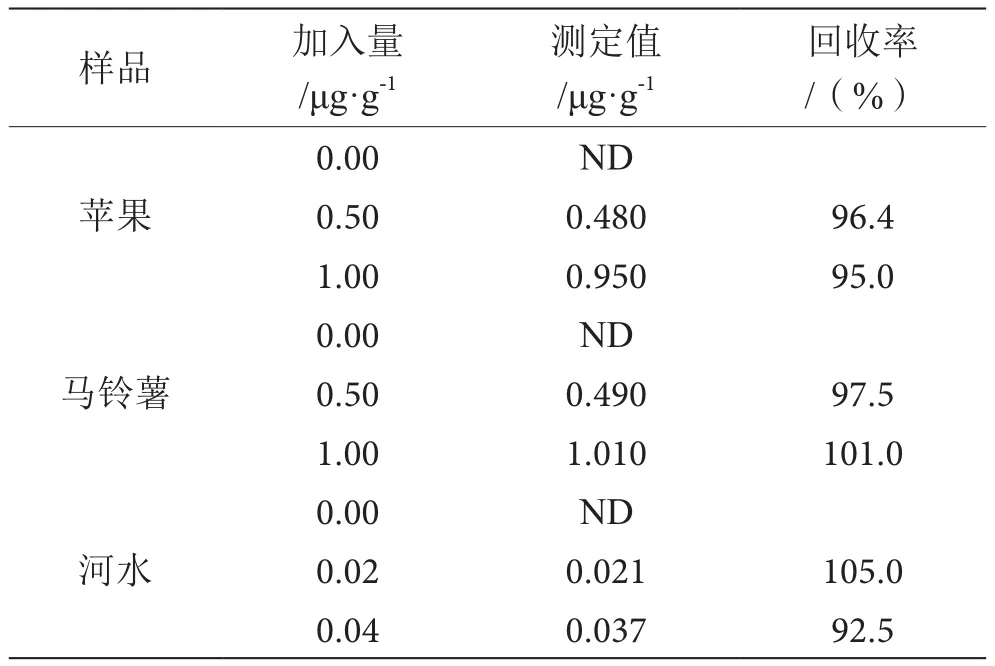
表1 水果、蔬和水样中利谷隆的测定比表
3 结论
本文建立以磁性氧化石墨烯纳米复合材料(Fe3O4@SiO2-GO)为萃取剂,联合高效液相色谱法分离分析利谷隆的新方法。该方法用于测定水果、蔬菜和水样中的利谷隆,回收率在92.5%~105.0%,结果令人满意。

