重度子痫前期患者血小板计数、D-二聚体值变化的临床意义
李淑玲,王瑞,曾晓岚
(广东省佛山市南海区人民医院 产科,广东 佛山 528200)
0 引言
妊娠期高血压疾病是临床常见的产科合并症,同时可增加新生儿和孕产妇的死亡、发病风险。我国的妊娠期高血压病变的平均发病率约为9.39%,近年来随着妊娠期检查的增强及普及,妊娠期高血压疾病的发病率逐年降低[1]。重度子痫前期是妊娠期高血压病变的类型之一,重度子痫前期可引发孕妇肾小管小血管痉挛加重,同时可出现肝酶升高、毛细血管溶血、血小板下降等异常凝血功能。研究表明,重度子痫前期时可增加血管促凝因子和收缩因子,同时可损伤血管内皮细胞,免疫介导的滋养细胞对胎盘螺旋动脉造成侵蚀而发病。研究指出,对重度子痫前期病人可严密监测其D-二聚体指标和血小板指标有助于评估病变的严重程度和评估预后[2]。本研究选择2018年3月至2021年3月在本院接受诊治的重度子痫前期病人70例,同期选择无妊娠合并症正常妊娠组70例为研究对照,分析两组的D-二聚体、血小板计数指标变化,现报道如下。
1 资料与方法
1.1 一般资料。临床选择2018年3月至2021年3月在本院接受诊治的重度子痫前期病人70例,同期选择无妊娠合并症正常妊娠组70例为研究对照,纳入标准:符合世界卫生组织制定的重度子痫前期的诊断标准[3];患者出现持续性上腹痛、持续性视觉障碍、持续性头痛或其他中枢神经系统临床特征、谷草转氨酶(AST)升高、谷丙转氨酶(ALT)升高、毛细血管溶血(乳酸脱氢酶升高)、血小板计数低于100×109/L、血清肌酐超过1.2 mg/dl,尿蛋白(++)或超过2.0 g/24 h,血压>160/110 mmHg。排除标准:多胎妊娠、癫痫、妊娠期肝内胆汁淤积症、妊娠期糖尿病(A2级或以上)、妊娠合并慢性高血压、妊娠合并慢性肾炎。本研究重度子痫前期组及正常妊娠组情况如下:重度子痫前期组年龄19~40岁,平均(34.6±2.1)岁;产次1~2次,平均(1.3±0.3)次;孕周30~34周,平均(32.7±1.2)周;体质量指数25~30 kg/cm2,平均(26.7±1.2)kg/cm2;正常妊娠组年龄20~37岁,平均(34.3±2.0)岁;产次1~2次,平均(1.2±0.2)次;孕周30~34周,平均(32.4±1.1)周;体质量指数25~30 kg/cm2,平均(26.5±1.0)kg/cm2;两组的平均年龄、产次、平均孕周等临床资料大体一致(P>0.05),具有可比性。
1.2 方法。全部研究对象采集2 mL肘部静脉血,置于枸橼酸钠真空抗凝管内,震荡充分混匀,标本采集2 h后即刻检测。应用凝血分析系统、全自动血液分析仪检测,严格根据操作使用说明书进行。应用电阻抗法检测血小板计数(PLT),免疫比浊法检测D-二聚体指标,因采集数据时发现孕周越大,D二聚体越高,故当正常妊娠组分娩孕周较大时,采集了孕周30~34周的D二聚体、PLT数据(与重度子痫前期组的分娩孕周大致相当);比较重度子痫前期组、正常妊娠组的D-二聚体、血小板计数、体质量指数、平均孕周等指标变化;比较重度子痫前期组、正常妊娠组妊娠结局分析。
1.3 仪器与试剂。日本Sysmex CS-5100凝血分析系统及配套试剂盒,日本Sysmex XN-9000全自动血液分析仪及配套试剂盒。
1.4 评估标准。D-二聚体指标超过500 ng/mL为异常,而血小板计数(PLT)低于100×109/L为异常[4]。
1.5 统计学处理分析。全部数据传输至SPSS 21.0软件系统处理,计量资料为t检验,均数±标准差表示,计数资料为卡方检验,[n(%)]表示,P<0.05为差异有统计学意义。
2 结果
2.1 重度子痫前期组、正常妊娠组各项临床指标变化分析。重度子痫前期组的D-二聚体指标、体质量指数显著高于正常妊娠组,差异有统计学意义(P<0.05);而重度子痫前期组的血小板计数指标显著低于对照组,差异有统计学意义(P<0.05)。见表1。
表1 重度子痫前期组、正常妊娠组各项临床指标变化分析(±s)
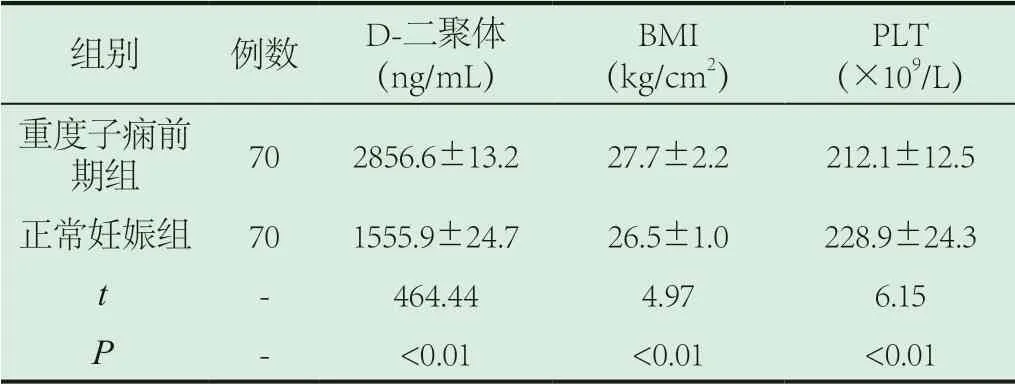
表1 重度子痫前期组、正常妊娠组各项临床指标变化分析(±s)
PLT(×109/L)重度子痫前期组 70 2856.6±13.2 27.7±2.2 212.1±12.5正常妊娠组 70 1555.9±24.7 26.5±1.0 228.9±24.3 t - 464.44 4.97 6.15 P - <0.01 <0.01 <0.01组别 例数 D-二聚体(ng/mL)BMI(kg/cm2)
2.2 两组妊娠结局分析。重度子痫前期组发生胎膜早破、胎儿宫内窘迫、新生儿窒息等、早产不良妊娠结局的发病情况显著高于正常妊娠组,差异有统计学意义(P<0.05)。见表2。

表2 两组妊娠结局分析[n(%)]
3 讨论
重度子痫前期病人母体在孕期纤维蛋白原增高,可能维持纤容和凝血的平衡,同时在胎儿与母体之间对子宫胎盘纤维蛋白层的稳定,对于形成卵黄囊和胎盘起到关键性保护功能[5]。纤维蛋白原下降不会对胚胎发育造成影响,但可导致子宫蜕膜和胎盘的分离,进而引发严重的内出血,出现胎盘早剥[6]。若子痫前期病人纤维蛋白原下降,说明胎死宫内或胎盘早剥,约有五分之一病人纤维蛋白降解产物,D-二聚体增高,可促使发生微血管性溶血性贫血,而凝血因子下降,监测血液D-二聚体指标对于评估病情预后、病情的动态发展变化、凝血功能状态具有重要的临床意义[7]。D-二聚体作为反馈纤溶系统的敏感指标,用于评估患者妊娠期高血压疾病的孕妇病情进展有指导意义,目前并未明确孕妇D-二聚体的正常范围,应根据医生临床经验评估孕妇D-二聚体水平[8]。
本研究观察监测重度子痫前期病人的D-二聚体和血小板计数指标变化的临床价值分析,结果显示:重度子痫前期组的D-二聚体指标、体质量指数显著高于正常妊娠组,差异有统计学意义(P<0.05);而重度子痫前期组的血小板计数指标显著低于对照组,差异有统计学意义(P<0.05);重度子痫前期组发生胎膜早破、胎儿宫内窘迫、新生儿窒息等不良妊娠结局的发病情况显著高于正常妊娠组,差异有统计学意义(P<0.05),与李丽红等[9]的研究结果大体一致,研究发现,血管内皮损伤可增加血管的通透性,进而引发肾小球蛋白渗出、血液浓缩、组织水肿,血管收缩因子、促凝血因子指标增高[10],血管扩张因子、抗凝血因子指标下降,损伤部位引发促凝血因子指标增多,最终引发血小板集聚、血栓形成,进而对有丝分裂原进行释放[11]。当重度子痫前期时血管促凝因子、收缩因子指标均增高,是自身和血管内皮细胞受损共同作用的结果。妊娠期高血压的发病形成机制为滋养细胞经免疫介导后对胎盘螺旋动脉造成侵蚀[12],进而引发胎盘单位内血流灌注缺乏,某些炎性因子分泌进入母体血液内,促使血管内皮活化,广泛改变了血管内皮细胞的功能,进而发病[13]。研究发现,重度子痫前期病人的凝血功能的变化包括血小板下降、红细胞被破坏、血管内凝血改变,其中最常见者为血小板计数显著下降,约有30%重度子痫前期病人出现凝血酶原时间延长[14]。血小板计数下降的原因尚在进一步研究中,可能与下列因素密切相关:子痫前期重度病人出现血小板下降者,而血小板生成因子增高,可促进产生血小板,但在生成血小板增高的同时,血小板的消耗和活化也逐渐增高,释放血清素指标增高,对血栓素A2进行激活,促使小血管痉挛,血小板集聚及凝集,诱发血小板下降;血小板在内皮受损部位出现沉积现象[14];重度子痫前期病人自身免疫过程出现免疫球蛋白结合血小板增高;血小板释放下降,凝集增高[15]。重度子痫前期血小板的消耗由单纯的血小板下降到微血管性溶血性贫血,甚至出现弥散性血管内凝血。重度子痫前期病人的血小板计数下降,伴随着严重的凝血功能异常,说明病情十分严重,母体和新生儿的病死率也逐渐增高,与血小板计数的下降程度呈反比。D-二聚体是纤维蛋白原与凝血酶发生作用进而产生交联纤维蛋白,经纤溶酶降解后生成的一种特异性降解产物,血液中D-二聚体含量增高说明形成血栓,且出现溶解,D-二聚体指标的高低可反应继发性纤容性的强度,是机体出现继发性纤容亢进和高凝状态的分子标志物之一[16]。重度子痫前期病人出现血管内皮细胞受损、胎盘缺血改变,进而对继发性纤维蛋白溶解系统进行启动,对子宫静脉窦和螺旋动脉内的血栓进行清除,子宫内膜的修复及再生加速,进而引发D-二聚体指标增高显著。严密监测重度子痫前期病人的血小板计数、D-二聚体指标变化有助于评估胎膜早破、新生儿窒息、胎儿宫内窘迫、早产等不良妊娠结局的发生。综上所述,重度子痫前期病人的D-二聚体指标显著增高,而血小板计数显著降低,极易发生胎膜早破、胎儿宫内窘迫、胎盘早剥、早产等不良妊娠结局,监测D-二聚体、血小板计数对于评估重度子痫前期的病情严重程度具有重要的临床价值。

