麦冬多糖对转化生长因子-β1 诱导的人胚胎肺成纤维细胞表型转化的影响
郑凌歆 王金丹 何超翔 郑兰芝
特发性肺纤维化是一种以肺成纤维细胞增殖、细胞外基质过度聚集及肺泡上皮损伤为特征的间质性肺疾病[1-2],发病机制未明,愈后差,缺乏有效的预防和治疗方法。目前认为成纤维细胞向肌成纤维细胞分化在纤维化进程中起至关重要的作用,其分化的标志是α-平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)的大量表达[3]。研究发现,转化生长因子-β1(transforming growth factor,TGF-β1)可诱导成纤维细胞向肌成纤维细胞分化[4],并可通过Smads信号通路调控纤维化进程[5]。因此,药物若能干预成纤维细胞向肌成纤维细胞分化的进程,则可为特发性肺纤维化的治疗提供新思路。麦冬具有养阴生津、润肺清心的功效。麦冬多糖(Ophiopogon japonicus polysaccharides,OJP)是其主要化学活性成分,主要药理作用为免疫调节、抗炎及降血糖等[6]。研究表明,麦冬注射液可有效抑制腹膜间皮细胞TGF-β1 及肿瘤坏死因子-α(tumor necrosis factor,TNF-α)的过度表达,从而阻止或延缓腹膜纤维化的发生[7],具有一定的抗纤维化作用。本研究观察OJP 对TGF-β1诱导的人胚胎肺成纤维(HEL)细胞表型转化的影响及初步机制进行探讨,报道如下。
1 实验材料
1.1 细 胞 HEL 细胞购自中国科学院昆明细胞库(KCB 86019)。
1.2 主要试剂及仪器 OJP(纯度98%,购自上海融禾医药科技发展有限公司),TGF-β1(购自艾美捷科技有限公司,4342-5),α-SMA(购自Abcam 公司,ab5694),胶原蛋白Ⅰ(COLⅠ)抗体(购自戴格公司,db517),Smad2、p-Smad2 抗体(购自Cell signaling technology 公司,5678S,3101S),胎牛血清(购自Gibco 公司,1903220),CCK-8(购自碧云天生物技术公司,C0037),CFX 96 Touch 实时荧光定量PCR 仪(美国伯乐),TS-1000 脱色摇床(海门其林贝尔仪器公司),Bio-RadMINI-P 垂直电泳系统(美国伯乐),S-3000N 扫描电镜(日本日立),AIR 激光共聚焦显微镜(浙江赛因)。
2 实验方法
2.1 细胞分组及给药方法 将对数生长期的HEL细胞分为对照组、模型组和OJP 干预组。模型组于TGF-β1 6ng/mL 处理2h 后继续培养24h。OJP 干预组于TGF-β1 6ng/mL 处理2h 后,再加入25、50、100μg/mL OJP 继续培养24h。
2.2 细胞增殖实验 将1×105/L 各处理组细胞悬液100μL 加置96 孔细胞培养板里,每组设5 个重复孔,同时设空白孔。每孔加入CCK-8 溶液培养2h后,用酶标仪于450nm 处测定吸光度值。
2.3 电镜观察 根据CCK-8 实验结果收集各处理组细胞悬液和爬片,分别加入2.5%戊二醛前固定,再以1%四氧化锇后固定2h,丙酮梯度脱水,618 环氧树脂包埋,超薄切片机进行切片,醋酸铀、柠檬酸铅染色,采用扫描电镜和透射电镜进行观察并拍照。
2.4 免疫荧光检测α-SMA 蛋白 将各处理组细胞爬片用4%多聚甲醛固定15min,0.3% TritonX-100室温通透15min,4%牛奶封闭2h,一抗4℃孵育过夜,FITC 绿色荧光二抗37℃避光孵育1h,滴加DAPI避光作用5min,50%甘油封片,激光共聚焦显微镜观察细胞中α-SMA 蛋白的分布定位。
2.5 实时荧光定量PCR 检测 收集各处理组细胞提取总RNA,逆转录成cDNA,并以其为模板进行PCR 扩增。引物由南京金斯瑞生物科技有限公司设计合成。引物序列为:α-SMA 正义5′-AGCGTGGCTATTCCTTCGTT-3′,反义5′-TCAGGCAACTCGTAACTCTTCT-3′;COLⅠ正义5′-TTCCTGCGCCTGATGTCC-3′,反义5′-GGTTCAGTTTGGGTTGCTTGT-3′。反应条件为:95℃预变性30s;95℃变性5s;60℃退火30s 后采集荧光信号,重复40 个循环。以GAPDH为内参,用所得Ct 值计算出相关蛋白的相对表达量。
2.6 Western blot 检测 收集各处理组细胞,加入蛋白裂解液提取蛋白并测定浓度,变性后进行SDSPAGE 电泳,300mA 电流转膜80min,5%脱脂奶粉封闭1h,加入一抗4℃孵育过夜,然后加入二抗孵育1h,Odyssey 近红外双色激光成像系统扫描、拍照成像,分析相关蛋白的表达情况。
2.7 统计学方法 应用SPSS 17.0 统计软件分析,实验数据用均数±标准差()表示,采用单因素方差分析,方差齐性则采用Bonferroni 法,方差不齐者用Dunnet's T3 法,P<0.05 为差异有统计学意义。
3 实验结果
3.1 不同浓度OJP 对TGF-β1 诱导的HEL 细胞增殖的影响 25、50、100μg/mL 的OJP 可抑制TGF-β1诱导的HEL 细胞增殖,且随着OJP 浓度的增加而增强(P<0.05),呈剂量依赖趋势。因此,后续实验选取100μg/mL 的OJP 进行干预。见表1。
表1 不同OJP 浓度对TGF-β1 诱导的HEL 细胞增殖的影响(%,)
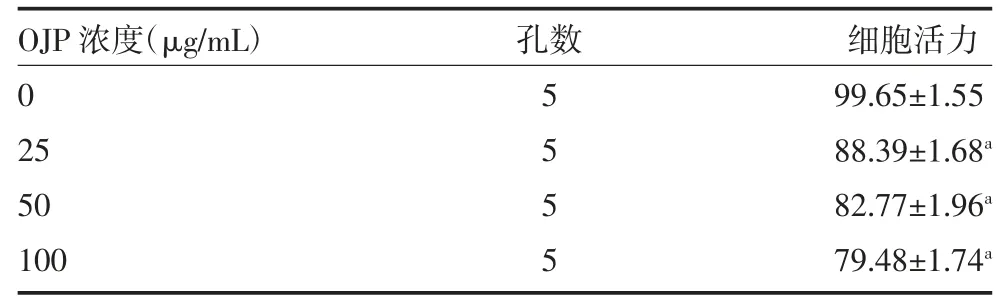
表1 不同OJP 浓度对TGF-β1 诱导的HEL 细胞增殖的影响(%,)
注:OJP 为麦冬多糖;TGF-β1 为转化生长因子-β1;HEL 为人胚胎肺成纤维;与0μg/mL 比较,aP<0.05
3.2 OJP 对TGF-β1 诱导的HEL 细胞超微结构的影响 通过扫描电镜(图1A)和透射电镜(图1B)分别观察TGF-β1 诱导的HEL 细胞超微结构发现,与模型组相比,100μg/mL OJP 干预组细胞表面微绒毛减少、微丝变短,胞浆内线粒体数目下降,粗面内质网减少。

图1 OJP 对HEL 细胞表面微观结构和细胞器的影响
3.3 OJP 对TGF-β1 诱导的HEL 细胞α-SMA 蛋白表达的影响 免疫荧光结果显示,对照组α-SMA 多不表达或很少表达,模型组α-SMA 在细胞核与胞浆内均表达且表达量增加,而100μg/mL OJP 干预组α-SMA 蛋白表达量明显降低,见图2。

图2 OJP 对TGF-β1 诱导的HEL 细胞中α-SMA 表达的影响(免疫荧光×200)
3.4 OJP 对TGF-β1 诱导的HEL 细胞α-SMA 和COLⅠmRNA 表达的影响 模型组α-SMA 和COLⅠ mRNA 相对表达量较对照组均明显增加(P<0.05),100μg/mL OJP 干 预 组α-SMA 和COL ⅠmRNA 相对表达量较模型组均明显下降(P<0.05),见表2。
表2 各组细胞α-SMA 和COLⅠmRNA 表达比较()
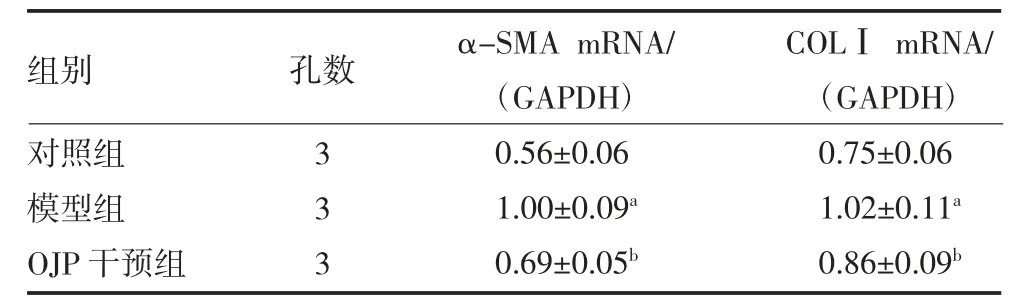
表2 各组细胞α-SMA 和COLⅠmRNA 表达比较()
注:对照组为HEL 细胞未经处理;模型组为HEL 细胞经TGF-β1 6ng/mL 处理2h 后继续培养24h;OJP 干预组为HEL 细胞经TGF-β1 6ng/mL 处理2h 后再加入100μg/mL 的OJP 继续培养24h;OJP 为麦冬多糖;TGF-β1 为转化生长因子-β1;HEL 为人胚胎肺成纤维;α-SMA 为α 平滑肌肌动蛋白;COLⅠ为Ⅰ型胶原蛋白;与对照组比较,aP<0.05;与模型组比较,bP<0.05
3.5 OJP 对TGF-β1 诱导的HEL 细胞α-SMA、COLⅠ、Smad2、p-Smad2 表达的影响 模型组α-SMA、COLⅠ、Smad2 和p-Smad2 蛋白表达较对照组均显著增加(P<0.01),而100μg/mL 的OJP 干预组α-SMA、COLⅠ、Smad2 和p-Smad2 蛋白表达较模型组均显著下降(P<0.01),见表3,图3。
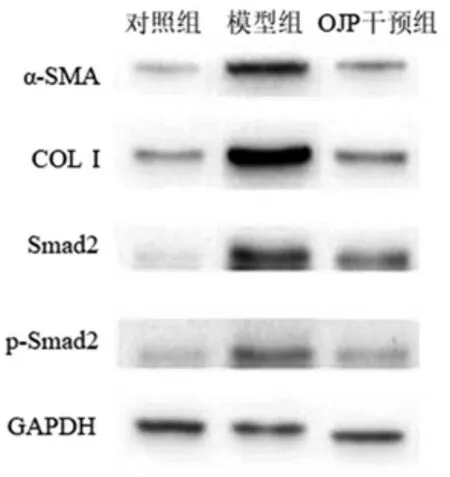
图3 Western blot 检测OJP 对TGF-β1 诱导HEL 细胞α-SMA、COLⅠ、Smad2、p-Smad2 蛋白表达
表3 各组细胞α-SMA、COLⅠ、Smad2、p-Smad2 蛋白表达比较()
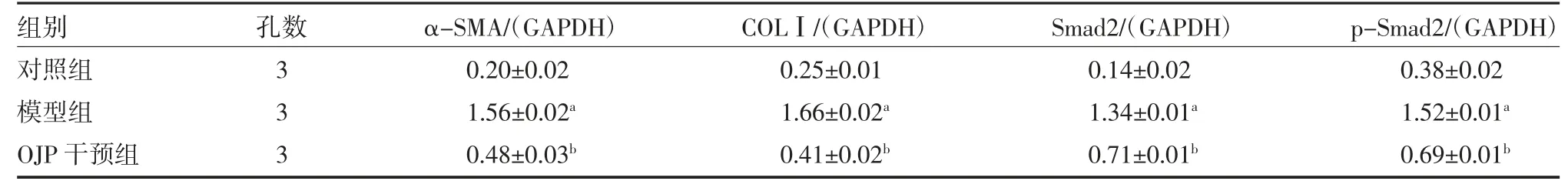
表3 各组细胞α-SMA、COLⅠ、Smad2、p-Smad2 蛋白表达比较()
注:对照组为HEL 细胞未经处理;模型组为HEL 细胞经TGF-β1 6ng/mL 处理2h 后继续培养24h;OJP 干预组为HEL 细胞经TGF-β1 6ng/mL处理2h 后再加入100μg/mL 的OJP 继续培养24h;OJP 为麦冬多糖;TGF-β1 为转化生长因子-β1;HEL 为人胚胎肺成纤维;α-SMA 为α 平滑肌肌动蛋白;COLⅠ为Ⅰ型胶原蛋白;Smad2 为信号转导蛋白;p-Smad2 为磷酸化信号转导蛋白;与对照组比较,aP<0.01;与模型组比较,bP<0.01
4 讨论
肺纤维化病因目前尚未明确,HEL 的活化被认为是其发生的核心环节。HEL 已被证实可造成细胞外基质大量沉积,促进上皮细胞损伤并诱导其凋亡,加重炎症反应,降低肺的顺应性[8]。肌成纤维细胞的迁移和分化可能是肺纤维化起始和进展中关键步骤之一[9]。TGF-β1 可通过Smads 蛋白通路使正常的成纤维细胞发生表型转化为肌成纤维细胞,α-SMA 和胶原蛋白的表达增强且抑制降解,从而促进细胞外基质沉积[10]。若能抑制成纤维细胞向肌成纤维细胞分化这一过程,则有望成为治疗纤维化疾病的新靶点。
研究表明,OJP 对某些纤维化疾病、糖尿病、心血管疾病及增强机体免疫力上有一定防治作用[7]。OJP 可干预氧自由基的损伤,改善细胞外基质(ECM)代谢,从而对肺间质纤维化的治疗起一定作用[7,11]。宁萌等[12]发现,OJP 能促进脂肪细胞对葡萄糖的转运和利用,在治疗2 型糖尿病大鼠过程中能降低其空腹血糖和改善胰岛素抵抗作用。Fan 等[13]研究表明,经OJP 对异丙肾上腺素诱导的大鼠具有心脏保护作用,同时还能降低ET-1 的水平并增加NO 的水平,重建血管舒张和收缩的平衡。此外OJP 及其脂质体已被证实可以显著改善巨噬细胞的吞噬活性,在机体免疫反应中发挥重要作用[14]。本实验选用TGF-β1进行诱导造模,方便快速可控。结果表明,一定浓度的OJP 可抑制HEL 细胞向肌成纤维细胞的转化。
TGF-β 主要通过Smads 信号通路实现调节功能,其与细胞膜上的TGF-β 受体(TβRⅡ)结合,诱发其磷酸化,继而与Ⅰ型受体(TβRⅠ)结合形成三聚体,诱导Smad2/3 的丝氨酸残基发生磷酸化形成p-Smad2/3,离开TβRⅠ受体后与Smad4 结合形成复合体,入核调控靶基因转录,导致正常的成纤维细胞转化为肌成纤维细胞,产生大量细胞外基质蛋白成分α-SMA、COLⅠ等,从而加强TGF-β 的诱导效果[15]。本实验结果显示,HEL 细胞受TGF-β1 刺激后Smad2 和p-Smad2 蛋白表达量增加;不同浓度的OJP 干预后,Smad2 和p-Smad2 蛋白的表达量减少,提示OJP 可能是通过TGF-β/Smads 信号通路,下调HEL 细胞中Smad2 和p-Smad2 蛋白的表达,从而抑制成纤维细胞向肌成纤维细胞的转化。
综上所述,本实验结果显示,OJP 对TGF-β1 诱导的HEL 细胞向肌成纤维细胞转化的进程有一定的抑制作用,并与TGF-β/Smads 信号通路相关。

